Forebyggelse og håndtering
2004 og 2006: Birgit Bødker (tovholder), Lisbeth Eriksen, Lone Hvidman, Lars Høj, Birgitte Bruun Nielsen, Yvonne Rasmussen (DASAIM), Benny Sørensen (Klin. Imm.), Jette Led Sørensen.
2012 og 2013: Charlotte Albrechsen (DASAIM), Lise Lotte Torvin Andersen, Birgit Bødker (tovholder), Caroline Clausen, Hellen Edwards, Laura Faber, Linn Helleland, Lone Hvidman, Lars Høj, Anja Kirstein, Jens Langhoff-Roos, Thea Lousen, Jakob Stensballe (DASAIM), Marie Søgaard.
2016 og 2017 (revison af uterotonika): Lise Lotte Torvin Andersen, Birgit Bødker (tovholder), Hellen Edwards, Lone Hvidman, Lars Høj, Eva Ostenfeld, Jesper Friis Petersen, Jens Langhoff Roos, Märta Fink Topsøe,
GUIDELINE
For at lette overskueligheden er retningslinierne nedenfor inddelt i naturligt sammenhørende ’pakker’/moduler af aktiviteter. PPH kan imidlertid have flere sammenvirkende årsager, hvorfor der oftest må foregå flere aktiviteter samtidigt. Der er altså ikke nogen tidslinie i guidelinen som skal følges, men rekommandationerne står i den rækkefølge de oftest opleves i et klinisk forløb. Diagnostik er afgørende for korrekt behandling. Derfor er det vigtigt at diagnostik og behandling foregår sideløbende.
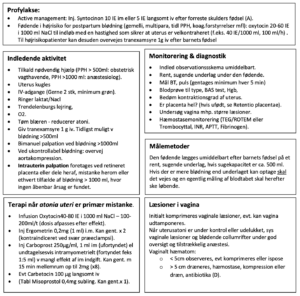
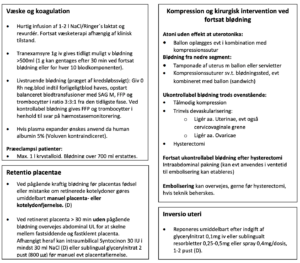
Alarmering – tid er afgørende!
Tidlig alarmering er afgørende for håndtering af sPPH. Mange aktiviteter foregår sideløbende se nøglepunkter i oversigtsform i nedestående Flowchart. Syntocinon er givet som profylakse:
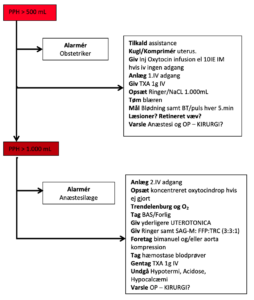
BAGGRUND
Postpartum blødning (PPH) defineres som blødning ≥ 500 ml.
Svær PPH defineres som blødning ≥ 1000 ml.
PPH ses hos 5 – 15 % af fødende. PPH >1000ml forekommer Jvf den Danske Kvalitetsdatabase for fødsler i 6-7% af alle fødsler i Danmark. På trods af forbedrede muligheder for behandling af postpartum blødning er det stadig en væsentlig årsag til maternel morbiditet og mortalitet. Blødning der opstår indenfor 24 timer efter fødslen, betegnes som tidlig postpartum blødning, og efterfølgende blødning betegnes som sen postpartum blødning. Tidlig postpartum blødning er sædvanligvis mest akut og er forbundet med størst morbiditet. Profylakse, tidlig diagnose og hurtig behandling er nøglebegreber i indsatsen mod postpartum blødning.
Målemetoder vs. estimering af blodtab
Målemetoder ved vaginal fødsel
Blodtabet efter barnets fødsel er målt dels i rene observationelle studier (1, 2, 12, 14, 15), dels som placebo-delen i kontrollerede studier (3-6, 9). Målemetoderne har været
I. Placering af den fødende på fladt bækken eller glat plasticunderlag hvorfra blodet ledes til en beholder og senere måles i målebæger eller vejes. Er i et studie i Angola kombineret med at den fødende herefter ligger på en koleraseng (3). På lignende måde er der flere studier der opsamler blodet vha. en speciel designet plastik pose. Her rapporteres om en korrelations koefficient på 0,928 i forhold til fotospektrometri (9, 10).
II. Placering af sugende underlag under den fødende, underlaget vejet (4-6)
III. Placering af sugende underlag under den fødende, underlaget + anvendte swaps og servietter lægges i 0.1N saltsyre, som omdanner alt hæmoglobin til hematin. Ved fortynding og spektrofotometri kan blodtabet hermed estimeres. Der rapporteres en måleusikkerhed på 0-10 % (1, 11, 14)
IV. Måling af totalt blodvolumen før og efter fødsel vha radiochrom-mærkede røde blodlegemer. Rapporteret måleusikkerhed 6 % (2).
I et review fra 2010 (13) er de forskellige metoder sammenlignet, hvor fotospektrometri angives som værende den mest nøjagtige, men er ikke praktisk at bruge i den kliniske hverdag. Den metode de anbefaler, der lettest kan implementeres og samtidig være pålidelig, er opsamling af blod samt vejning af underlag mm.
Fysiologisk blodtab
Studier med omhyggeligt målt blodtab af passivt/placebo-behandlet efterbyrdsperiode har rapporteret blodtabet som angivet i nedenfor viste tabeller.
Blødningsmængde
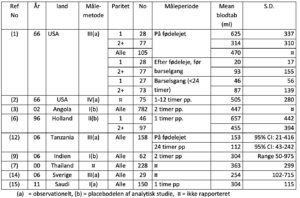
Incidens af PPH 500ml og 1000ml
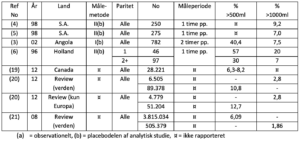
Estimering af blodtab:
Der findes flere studier der vurderer forholdet mellem estimeret og målt blodtab. Et amerikansk studie fra 1966 (1) viste at trænede obstetrikere/jordemødre skønnede 20 % for lavt, når blodtabet var 400-499 ml og 34 % for lavt ved et blodtab > 500 ml. I et studie fra Thailand (7) blev blodtabet skønnet 27 % lavere end det faktisk målte og incidensen af PPH (> 500ml) blev skønnet til 5,7 %, mens det ved måling viste sig at det faktisk var 27,6 % af de fødende, der havde blødt mere end denne mængde. 8 (3,5 %) fødende havde blødt mere end 1000 ml, hvilket kun var blevet ´gættet´ i 1 tilfælde. Tilsvarende var der i et australsk studie (8) kun én ud af ni med blødning > 500 ml, der korrekt blev diagnosticeret som PPH. Man kunne her vise at dogmet om at en blødningen efter fødsel var 200-300ml betød at blodtab under dette niveau blev overestimeret og tab over dette niveau blev underestimeret.
Flere andre studier har også vist at nøjagtigheden ved estimering af blodvolumen er volumenafhængig, hvor man har tendens til at overestimere ved mindre blodvolumen og underestimere ved større blødning.
I et studie fra England (16) så man en tendens til at overestimere blodtab ved volumen under 200ml (op til 540 %) med test-retest forskelle på op til 300 %. Der var ingen signifikant forskelle mellem specialister, kursister og jordemødre i estimering af mindre blodvolumen. Man fandt i samme studie at vejning af servietter/underlag var det mest nøjagtige og reproducerbare måde at måle blodtab på, med en reproducerbarheds coefficient på 7,57 %. Ligeledes finder A. Patel et el (9) at estimeret blodtab blev underestimeret med 33 % ift måling vha opsamlingspose. I et review fra 2010 (13) fandtes ligeledes tendens til underestimering, og ofte værre jo mere blødning, men at simulations øvelser kunne mindske denne unøjagtighed.
Et studie viste at træning af helsepersonel i estimering af blodtab førte til en gennemsnitlig forbedring på 34 % ved sammenligning af præ – og post trænings test (95 % konfidens interval, 10–57 %; P_.001). Men der var kun estimering af materiale på billeder. Man viste samtidig at der ikke var nogen signifikant forskel på at få ”live” undervisning (scenario) sammenholdt med webbaseret træning (kursus 20 min) (17).
Men der ses en forringelse i evnerne til at vurdere blodtab 9 måneder efter træning/undervisning. Der var ingen signifikant forskel på evnen til at vurdere blodtab når man så på personalegruppe (anæstesiolog, obstetriker, sygeplejerske), erfaring (<3, 4-10, >10 år) eller tidligere træning i at vurdere blodtab (p = 0,12,0,16 og 0,35) (18).
Sammenfatning
På baggrund af ovenstående anbefales det at den fødende umiddelbart efter barnets fødsel lægges på en rent, sugende underlag, hvis sugekapacitet er ca 500 ml. Hvis dette ikke overskrides kan underlaget kasseres og blodtabet blot estimeres. Hvis der er mere blødning end underlaget kan optage skal det vejes og en egentlig måling af blodtabet skal herefter ske 8 løbende (Evidensgrad II). Der bør på fødegangen foreligge en liste over tørvægten at krøller, servietter og lign., der bruges til optørring af blod. Ligeledes bør alle faggrupper regelmæssigt trænes i estimering af blodvolumen evt vha billeder af forskellige scenarier.
Referencer
1. Newton M. Postpartum hemorrhage. Am.J.Obstet.Gynecol. 1966;94(5):711-7.
2. Pritchard JA, Baldwin RM, Dickey JC, Wiggins KM. Blood volume changes in pregnancy and the puerperium: 2. Red blood cell loss and changes in apparent blood volume during and following vaginal delivery, cesarean section, and cesarean section plus total hysterectomy. Am.J.Obstet.Gynecol. 1962;84(10):1271-82.
3. Strand, R. T., da Silva, F., Jangsten, E., and Bergstrom, S. A new disposable device for oxytocin administration in active management of the third stage of labour: a prospective comparative study in Angola. 2002. Ref Type: Unpublished Work
4. Hofmeyr GJ, Nikodem VC, de Jager M, Gelbart BR. A randomised placebo controlled trial of oral misoprostol in the third stage of labour. Br.J.Obstet.Gynaecol. 1998;105(9):971-5.
5. Bamigboye AA, Hofmeyr GJ, Merrell DA. Rectal misoprostol in the prevention of postpartum hemorrhage: a placebo-controlled trial. Am.J.Obstet.Gynecol. 1998;179(4):1043-6.
6. de Groot AN, van Roosmalen J, van Dongen PW, Borm GF. A placebo-controlled trial of oral ergometrine to reduce postpartum hemorrhage. Acta Obstet.Gynecol.Scand. 1996;75(5):464-8.
7. Prasertcharoensuk W, Swadpanich U, Lumbiganon P. Accuracy of the blood loss estimation in the third stage of labor. Int.J.Gynaecol.Obstet. 2000;71(1):69-70.
8. Razvi K, Chua S, Arulkumaran S, Ratnam SS. A comparison between visual estimation and laboratory determination of blood loss during the third stage of labour. Aust.N.Z.J.Obstet.Gynaecol. 1996;36(2):152-4.
9. Patel A, Goudar S.S, Geller S.E. Drape estimation vs. visual assessment for estimating postpartum hemorrhage. Int.J.Gynaecol.Obstet. 2006;93; 220-24.
10. Zhang W, Deneux-Tharaux C, Brocklehurst P. Effect of a collector bag for measurement of postpartum blood loss after vaginal delivery: cluster randomised trial in 13 European countries. BMJ. 2010;340;293
11. Chua S, Ho L.M, Vanaja K. Validation of a laboratory method of measuring postpartum blood loss. Gynecol.Obstet.Invest. 1998;46;31-33
12. Kavle J.A, Khalfan S.S, Stotzfus R.J, Measurement of blood loss at childbirth and postpartum. Int.J.Gynaecol.Obstet. 2006; 95; 24-28
13. 13.Schorn Mavis. Measurement of blood loss: Review of the literature. J.Midwifery.Womens.Health. 2010; 55; 20-27.
14. Larsson C, Saltvedt S, Wiklund I. Estimation of blood loss after caesarean section and vaginal delivery has low validity with a tendency to exaggeration. Acta Obstet.Gynecol. 2006;85;1448-1452.
15. Al Kadri H.M.F, Al Anazi B.K, Tamim H.M. Visual estimation versus gravimetric measurement of postpartum blood loss: a prosepctive cohort study. Arch.Gynecol.Obstet. 2011;283;1207-1213.
16. Yoong W, Karavlos S, Damodaram M. Observer acuuracy and reproducibility of visual estimation of blood loss in obstetrics: how accurate and consistent are health-care professionals?. Arch.Gynecol.Obstet. 2010; 281; 207- 213.
17. Toledo, P et al, The effect of live and web based education on the accuracy of blood loss estimation in simulated obstetric scenarios. Am J obstet Gynecol 2010;202:400.el-e5.
18. Toledo, P et al. Decay in Blood Loss Estimation Skills After Web-Based Didactic Training Sim Healtcare (2012) 7:18-21.
19. Mehrabadi A, Hutcheon J.A, Lee L. Trends in postpartum hemorrhage from 2000-2009: a population-based study. BMC.Pregnancy.Childbirth. 2012;12;108.
20. Calvert C, Thomas S.L, Ronsmans C. Identifying regional variation in the prevalence of postpartum haemorrhage: A systematic review and meta-analysis. PLoS.One. 2012;7;e.41114.
21. Carroli G, Cuesta C, Abalos E. Epidemiology of postpartum haemorrhage: a systematic review. Best.pract.res.clin.obstet.gynaecol. 2008;22;999-1012.
Målemetode ved sectio
Visuel estimering af blødning er en unøjagtig metode (1-5). Ved større blødninger over 1000ml er unøjagtigheden større, med fare for underestimering (3). Dette er kendt ved vaginal fødsel, men gælder også ved sectio (3). Postpartum blødning ved sectio er i litteraturen ofte defineret som blødning over 1000ml (6).
Metoder til måling af blod tab ved sectio:
- Visuel estimering af blodtab (5).
- Vejning af servietter etc. og mål af opsuget volumen (7-8).
- Hemo Cue photometer til at måle hæmoglobin koncentrationen i suget ved elektivt sectio (4).
- Beregnet blodtab ud fra en modificeret formel til at beregne den gravides blodvolumen (man bruger moderens vægt, højde samt præ – og postpartum hæmatokrit værdier) (3).
- Pictogram med billeder af kendt blødningsmængde på div. kirurgisk materiale, brugt til at forbedre evnen til at estimere blodtabet ved sectio (9).
Sammenfatning
Der er stor usikkerhed forbundet med visuel estimering af blod tab. Men ud fra litteraturen må anbefalingen være at bruge visuel estimering sammen med beregnet blødning. Dette ud fra mængden af væske opsuget under sectio, samt ved at veje servietter og andet opsugende materiale. Det kan være svært at skille blod fra amnionvæske, som en hjælp kan man bruge Hemo Cue men der kræves noget udstyr samt forberedelse. Som støtte til den visuelle estimering kan man bruge pictogram samt beregne blodtab ud fra højde, vægt og hæmatokritværdier.
Referencer
1. Schorn et al. 2010, J Midwifery Womens health Womens Health 2010;55:20-27.
2. Patton et al, Accuracy of estimation of external blood loss by EMS personnel. J Trauma 2001;50:914-6.
3. Stafford,Irene et al. Visually estimated and calculated blood loss in vaginal and cesarean delivery. Am J Obstet Gynecol 2008;199:519.e1-519.e7.
4. Gupta, A et al, Use of HemoCue near patient testing device to measure the concentration of haemoglobin in suction fluid at elective Caesarean section, Anaesthesia, 2008, 63, p 531-534.
5. Larsson et al, Estimation of blood loss after cesarean section and vaginal delivery has low validity with a tendency to exaggeration.
6. Pritchard et al Blood volume changes in pregnancy and the puerperium. II Red blood cell loss and changes in apparent blood volume during and following vaginal delivery, cesarean section, and cesarean plus total hysterectomy. Am J Obstet Gynecol 1962;84:1271-1282.
7. Magann et al, Postpartum Hemorrhage After Cesarean Delivery: An Analysis of RiskFactors, Southern Medical Journal, 2005, Vol.98, 7, p 681-685.
8. Sheenan, S. et al , A prospective cohort study evaluating bloodloss estimation at cesarean section and the risk factors for major obstetric haemorrhage. Irish Journal of Medical Science, Vol 180, 141-141, supplement 4, Apr 2011.
9. Cheerranichanunth, Poolnoi, using Blood loss Pictogram for Visual Blood Loss Estimation in Cesarean section, J med Assoc Thai 2012;95 (4): 550-6.
Forebyggelse af postpartum blødning
Risikofaktorer
Følgende risikogrupper har særligt høj risiko for PPH (alfabetisk)1,2,3,4,5:
Evidens 2a
Kendt før fødsel
- Abruptio placentae, kendt eller mistænkt
- Alder over 40
- Anæmi
- Asiatisk oprindelse
- Gemelli eller andre flerfold
- Hydramnios
- Hypertension
- Overvægt (BMI > 35)
- Paritet, høj (5 eller flere) og lav (1 eller 0)
- Placenta prævia
- Præeklampsi
- Tidligere PPH
- Von Willebrand’s syge
Opstået under fødsel
- Episiotomi
- Fastsiddende moderkage
- Feber under fødslen
- Kejsersnit, akut eller planlagt
- Kop- eller tang-forløsning
- Langvarig fødsel (aktiv fase over 12 timer)
- PP.Med. herunder HSP
- Stort foster (LGA eller over 4 kg)
- Ve-stimulation
Forebyggelse af PPH
Forebyggelse af PPH behandles i flere Cochrane reviews og i RCOG Green-top Guideline (GTGL) no.52. RCOGs GTGL er fra 2009 og har ikke de nyeste Cochrane-opdateringer med.
RCOG anbefaler1 aktiv håndtering af fødslens tredje stadie dvs:
- Ved forreste skulders fødsel (eller lige efter barnets fødsel) gives uterotonikum. o 5-10 IE Syntocinon(Oxytocin) im.
- Let træk på navlesnoren.
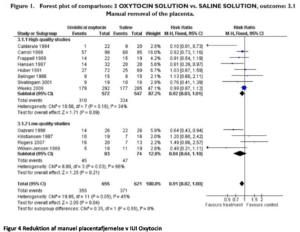
McDonald SJ et al6 sammenligner brug af Oxytocin alene med kombinationspræparater ErgometrinOxytocin som del af aktiv håndtering af fødslens tredje stadie og omfatter 6 studier med 9332 kvinder. Forfatterne konkluderer, at kombinationspræparaterne medfører en lille men statistisk signifikant reduktion i PPH mellem 500 og 1000 ml ved sammenligning med Oxytocin alene. Der var ingen forskel mellem præparaterne ved blodtab over 1000 ml. Kombinationspræparaterne førte til flere maternelle bivirkninger (blodtryksstigning, kvalme, opkastninger) end Oxytocin alene. Forfatterne konkluderer, at fordelen ved at reducere PPH mellem 500-1000 ml skal vejes op imod risikoen for uønskede bivirkninger.
Evidens 1a
Cotter AM et al7 undersøger effekten af profylaktisk Oxytocin givet i fødslens tredje stadie. 7 af 14 studier (over 3000 kvinder) sammenligner Oxytocin med ingen uterotonika. Profylaktisk Oxytocin fører til lavere risiko for blødning over 500 ml og lavere behov for terapeutiske uterotonica.
Evidens 1a
6 af 14 studier (over 2800 kvinder) sammenligner Oxytocin med Ergot-alkaloider. Ringe evidens for forskel mellem grupperne, men færre manuelle placentaløsninger og lavere risiko for blodtryksstigning ved Oxytocin.
Evidens 1a
5 af 14 studier (over 2800 kvinder) finder ringe evidens for synergistisk effekt af at supplere Ergometrin med Oxytocin sammenlignet med Ergometrin alene. Evidens 1a Forfatternes samlede konklusion er, at Oxytocin kan være gavnligt til at forebygge PPH. Der er ringe information om andre udkom og bivirkninger. Der er lille evidens baseret på sparsomme data til fordel for Ergometrin alene både sammenlignet med Oxyocin alene og kombinationspræparater.
Evidens 1a
Begley et al8 sammenligner aktiv og afventende/konservativ/fysiologisk håndtering af fødslens tredje stadie. Aktiv håndtering er som beskrevet i RCOG GTGL.
Fysiologisk håndtering består af følgende: Roligt og trygt miljø; så lidt berøring som muligt; sen afnavling (enten ved pulsophør eller efter placentas fødsel); observation for separationstegn; placenta fødes spontant evt. med hjælp af tyngdekraft; der gives ikke uterotonica, men anvendes gerne brystvortestimulation fx ved at lægge barnet til brystet. I alt 7 studier med 8247 kvinder. 4 af 7 studier (4829) sammenlignede aktiv og fysiologisk metode.
De 3 øvrige sammenlignede aktiv håndtering med en blanding af håndteringsmetoder. Forfatterne konkluderer at for kvinder med varierende risiko for PPH viste aktiv håndtering signifikant reduktion i risiko for: PPH over 500 og over 1000 ml, lav hæmoglobin, behov for transfusion og behov for terapeutisk uterotonikum efter fødslen. Ingen forskelle i indlæggelse på neonatal afdeling eller behandling for gulsot hos den nyfødte. Aktiv håndtering førte til flere bivirkninger end fysiologisk håndtering: blodtryksstigning, opkastning, efterveer, øget behov for analgetika, og flere genindlæggelser som følge af blødning.
Evidens 1a
I en subgruppe af kvinder med lav risiko for PPH (2941) var der lignende fund bortset fra at der ikke var nogen signifikant forskel i antallet af kvinder med alvorlig PPH eller lav hæmoglobin efter fødslen (ikke-signifikant pga lavt antal).
Forfatterne opfordrer til, at kvinder med vurderet lav risiko for PPH som føder i lav-risko-settings informeres om fordele og ulemper ved aktiv og fysiologisk håndtering og inddrages i beslutning om metodevalg.
Evidens 1a
Oxytocin anvendt som PPH profylakse, tilføjelse 2017
(Westhoff et al fandt i et Cochraine review at profylaktisk oxytocin i 3. stadie af fødslen reducerede den relative risiko for PPH >500 ml med 50% (6 RCT, N=4203) sammenlignet med placebo.9 Ved indirekte sammenligning var effekten af oxytocin signifikant for varierende doser (3/5/10 IU) og administrationsform (IV eller IM). Profylaktisk oxytocin reducerede ligeledes behov for anden uterotonika med ca 50% sammenlignet med placebo (4 RCT, N=3174) men effekten var kun til stede ved anvendelse af 10 IU administreret IV. Administration IM viste en trend mod reduceret behov for anden uterotonika (3 RCT, N=2174), som ved analyse af det største RCT (N=1901) var signifikant. Sammenlignet med ergometrin reducerede oxytocin ikke overbevisende PPH >500 ml, men medførte signifikant færre bivirkninger. Forfatterne fandt ingen gevinst på PPH ved at kombinationsbehandling med oxytocin plus ergometrin sammenlignet med ergometrin alene. Sammenfattende fandt forfatterne god evidens for anvendelse af oxytocin ved 3. stadie af fødslen for forebyggelse af PPH og anbefalede administration af 10 IU IV, alternativt IM såfremt IV ikke umiddelbart var muligt.
Et mindre RCT (N=100) fandt ingen signifikant forskel på andelen af atoni eller PPH >500 ml efter anvendelse af PPH profylakse med oxytocin 10 IE IV sammenlignet med injektion IM.10 Data vedrørende bivirkninger var ikke vist. RCT var begrænset ved et meget lille antal cases.
Sammenfatning
Alle fødende anbefales blødningsprofylakse med: Oxytocin (5-)10 IE im efter forreste skulders fødsel, enten alene eller som del af aktiv håndtering af efterbyrdsperioden
Rekommandationsgrad A
- Evt ve-stimulerende drop kan øges i dråbehastighed Navlesnorsprøver til pH tages uden afklemning 14
- Alternativt dobbeltafnavling efter ca 30 sekunder
- Navlesnoren klippes efter pulsophør, før ved pågående blødning
- Ved tegn på separation trækkes let på navlesnoren og kvinden opfordres til at presse
Fysiologisk håndtering af efterbyrdsperioden bør kun anvendes, hvis den fødende er rask, ikke har nogen risikofaktorer og har født normalt. Det er arbejdsgruppens opfattelse, at fysiologisk håndtering primært har sin plads hos fødende, som frabeder sig behandling med Syntocinon. Metoden er skønsmæssigt kun egnet hos ca. 10 % af danske fødende, når man tager højde for risikofaktorer før og under fødslen. Metodevalg og ændring af metodevalg under fødslen stiller krav om risikovurdering før og under fødslen.
Særlig høj risiko for postpartum blødning
Ved særlig høj risiko for postpartum blødning jvf liste ovenfor skal profylaktiske tiltag som opsætning af et profylaktisk oxytocin-drop samt evt sikring af tilgængelige blodprodukter altid overvejes.
Referencer
1. RCOG Green-top 52: Postpartum Haemorrhage, Prevention and Management. 2009.
2. Combs CA, Murphy EL, Laros RK Jr. Factors associated with postpartum hemorrhage with vaginal birth. Obstet Gynecol. 1991 Jan;77(1):69-76.
3. Stones RW, Paterson CM, Saunders NJ. Risk factors for major obstetric haemorrhage. Eur J Obstet Gynecol Reprod Biol. 1993 Jan;48(1):15-8.
4. Al-Zirqi I, Vangen S, Forsen L, Stray-Pedersen B. Prevalence and risk factors of severe obstetric haemorrhage. BJOG. 2008 Sep;115(10):1265-72.
5. Tsu VD. Postpartum haemorrhage in Zimbabwe: a risk factor analysis. Br J Obstet Gynaecol. 1993 Apr;100(4):327-33.
6. McDonald S, Abbott JM, Higgins SP. Prophylactic ergometrine-oxytocin versus oxytocin for the third stage of labour. Cochrane Database Syst Rev. 2004;(1): Review.
7. Cotter AM, Ness A, Tolosa JE. Prophylactic oxytocin for the third stage of labour. Cochrane Database Syst Rev. Published Online: 17 FEB 2010.
8. Begley CM, Gyte GML, Devane D, Mcguire W, Weeks A. Active versus expectant management for women in the third stage of labour. Cochrane Database Syst Rev. Published Online: 9 NOV 2011
9. Westhoff, G., Cotter, A. M. & Tolosa, J. E. in Cochrane Database of Systematic Reviews (ed. Westhoff, G.) (John Wiley & Sons, Ltd, 2013). doi:10.1002/14651858.CD001808.pub2
10. Dagdeviren, H. et al. Intramuscular versus intravenous prophylactic oxytocin for postpartum hemorrhage after vaginal delivery: a randomized controlled study. Arch. Gynecol. Obstet. 294, 911–916 (2016).
Retentio placenta efter vaginal fødsel
Definition
Retentio placenta (RP): Når placenta ikke er født 30 minutter efter barnets fødsel.
Afgrænsning
Vaginal fødsel efter uge 24 hvor diagnosen accret/percret/incret ikke er stillet i forvejen. Der skelnes mellem RP uden blødning (RPUB) når den fødende er hæmodynamisk stabil med blødning < 1000 ml og RP med blødning (RPB) hvor der er pågående blødning, blødning > 1000 ml og/eller hæmodynamisk ustabilitet.
Diagnose
Ved RPUB er det af værdi at lave abdominal UL forud for yderligere intervention. Dette for at skelne mellem fastsiddende og fastklemt placenta. (Rekommandationsgrad C)
Behandling ved Retention placentae med blødning
Ved RPB er der indikation for manuel placentafjernelse uden yderligere diagnostik. (Rekommandationsgrad D)
Behandling ved Retention placentae uden blødning
Ved RPUB og mistanke om fastsiddende placenta kan jordemoderen anvende uterin massage og akupunktur for at fremme placentas fødsel. (Rekommandationsgrad D)
Ved RPUB og manglende effekt af ovenstående kan intraumbilical injektion via babyfeeding tube/navlevenekateter forsøges. Der anvendes 30 IU Syntocinon i mindst 30 ml NaCl. (Rekommandationsgrad D)
I udvalgte tilfælde af RPUB og manglende effekt af IUI kan placenta herefter forsøges løsnet med sublingual nitroglycerin 2 pust (800 µg) (Rekommandationsgrad D)
Hvis placenta mistænkes fastklemt forsøges primært med nitroglycerin sublingualt 2 pust (800 µg) (Rekommandationsgrad C)
Baggrund
Incidensen af retineret placenta varierer i forskellige populationer1 . Definitionen er ikke enslydende hos WHO2 og f.eks. NICE3 ; og endelig er der både national som international variation i hvornår og hvorledes en retineret placenta hos en fødende uden blødning håndteres aktivt af fødselshjælperen. En europæisk undersøgelse fra 2009, der bl.a. indbefattede 23 fødesteder i Danmark4, viste at Danmark sammen med Norge, Holland og Finland tilhørte den ’afventende’ gruppe, idet 79 % af fødestederne ventede i mere end 60 minutter inden intervention (89 %, hvis den fødende havde epidural). I Central- og Sydeuropa blev der ofte interveneret aktivt før 30 min og for flertallets vedkommende mellem 30 og 60 min.
Observationelle studier viser en positiv relation mellem længden af efterbyrdsfasen (tid for 3.stadie = TSL) og mængden af PPH5;6. I en undersøgelse af 6588 vaginalt fødende5 , der blev håndteret med AMSTL (active management of third stage of labour), var risikoen forPPH > 1000ml allerede forhøjet efter 10 minutters TSL (OR 2.1, 95% CI 1.6 –2.6); efter 20 minutter var OR 4.3 (95% CI 3.3–5.5) og efter 30 minutter var OR 6.2 (95% CI 4.6–8.2). Den bedste prædiktor for PPH var en ventetid på 18 minutter før fødsel af placenta.
Dette er ikke ensbetydende med en kausal sammenhæng, idet nedsat kontraktilitet i uterus disponerer for begge faktorer. Da efterbyrdsfasen desuden er en travl periode med mange andre vigtige aktiviteter (mor/barn kontakt, måling af navlesnors-pH, K-vitamin osv.) er det vigtigt ikke at introducere procedurer uden sikker effekt. Da manuel placentafjernelse er ressourcekrævende, skræmmende for den fødende og i sig selv disponerer for blødning og infektion, er det sandsynligvis fornuftigt at forsøge sig med mindre invasive metoder inden dette.
Hensigten med denne gennemgang er derfor at forsøge at fastslå det optimale tidspunkt at overgå fra afventende til aktiv håndtering af den retinerede placenta. Desuden gennemgås evidensen for en række mulige interventioner forud for manuel placentafjernelse.
Definition
Rententio placenta = Manglende løsning af placenta 30 min efter barnets fødsel. Denne definition er valgt på baggrund af ovenstående studier over sammenhæng mellem TSL og PPH og i overensstemmelse med National Institute for Health and Clinical Excellence3
Efterbyrdsfasen= Third Stage of Labour = TSL. Intervallet mellem fødsel af barn og fødsel af placenta.
Diagnose
’Retineret placenta’ er et klinisk begreb som dækker over at placenta – set fra fødselshjælpenren side – endnu ikke er født. Dette kan både betyde at den har løsnet sig, men er fanget bag en velkontraheret cervix (trapped placent/fastklemt placenta), og at den reelt er fastsiddende i uterus (placenta adherens). Sidstnævnte tilstand betyder at den naturlige separationsmekanisme endnu ikke har fundet sted og man vil ved manuel placentafjernelse i denne gruppe finde at en lille andel er accret (placenta accreta) (Den accrete tilstand vil ikke blive behandlet her; men i guidelinen ’Abnorm placentation’) LINK.
Et kohortestudie med 287 tilfælde af TSL>30 min fandt at 81% var af typen placenta adherens, 6% havde accrete områder og 13% var ’trapped’7 . I Hinchingbrooke-studiet over AMSTl fandt man at 51% af de retinerede placentae var trapped8.
En erfaren jordemoder kan med et vist sandsynlighed skelne mellem de to tilstande; men bedre diagnose forud for evt. intervention fås ved abdominal ultralydsskanning9. Ved en fastklemt placenta er myometriet tykt hele vejen rundt om en placenta, der ofte sidder sv.t. isthmus eller cervix; mens en fastsiddende placenta er kendetegnet ved et meget tynd myometrium over placentalejet og tykt i andre områder.
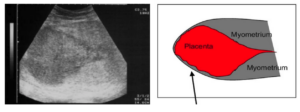
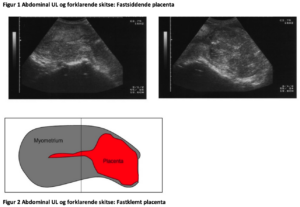
Håndtering
Active Management of third stage of labour
Består af syntocinon injektion efter forreste skulders fødsel, træk på navlesnor og afklemning af navlesnor. Det er påvist at forkorte efterbyrdsfasen og er standardpraksis i DK (se afsnit om profylakse ovenfor). Dette anses derfor for at forudgå nedenstående interventioner.
Ikke-medicinsk behandling:
Uterusmassage
Stimulation af brystvorter
Det eneste fundne studie, der behandler tidlig postnatal stimulation af brystvorter viser ingen forskel på retinerede placentae i interventions- og kontrolgruppe (2104 vs 2123 fødende)10. Det bemærkes at studiet størrelse var for lille til statistisk analyse af dette effektmål.
Akupunktur
Der er kun fundet ét studie over akupunktur og retineret placenta11; men dette fandt at akupunktur var en effektiv og sikker metode til fjernelse af placenta. Der indgik 75 fødsler i studiet og 45 ptt fik foretaget manuel placentafjernelse og 30 fik akupunktur. I akupunkturgruppen kvitterede 83% inden for 20 min, 47% af disse indenfor 5 min. Af 6 der ikke kunne fjernes v akupunktur vuderedes de 4 som accrete. I akupunkturgruppen blødte 13% > 500ml, i manuel placentafjernelse-gruppen var det 47%.
Medicinsk behandling
Uterotonica
Oxytocin
Der findes ikke randomiserede trials hvor intravenøs oxytocin sammenlignes med placebo i behandlingen af retentio placenta. Da det er blevet sandsynliggjort at der opnås bedst effekt med færrest bivirkninger, hvis den myometrie-kontraherende medicin indsprøjtes i selve placenta12 har de fleste studier koncentreret sig omkring intraumbilical injektion (IUI).
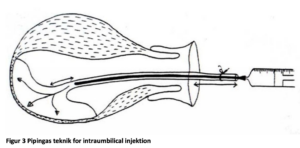
Et Cochrane-review med samlet 1118 fødende har undersøgt forskellige blandinger oxytocin og saltvand og disses effekt ved rutinemæssig IUI efter fødsel13. Konklusionen er at rutinemæssig brug ikke anbefales.
Det nyeste Cochrane review omhandlende håndtering af ufødte placentae efter 30 min inkluderer 15 trials med 1704 fødende14, hvor forskellige former for IUI af uterotonica og væske er undersøgt. Her findes ingen effekt af saltvand og plasmaexpander alene og en netop ikke-signifikant effekt af Oxytocin sammenlignet med saltvand (RR 0.91; 95% CI 0.82 – 1.00).
Da der ikke fandtes målbare bivirkninger af den intraumbilicale injektion anbefaler forfatterne et forsøg på denne metode trods den manglende statistiske signifikans.
Prostaglandin
I et mindre RCT fra 2006 fandt van Beekhuizen et al at intravenøst sulprostone (prostaglandin E2 analog) udløste fødsel af RP imod 18 % ved placebo (p=0,03).
I ovenfor nævnte Cochrane review14 findes 2 meget små studier, hvor der er signifikant effekt af IUI af prostaglandin. I det ene studie indgik 17 kvinder der fik injiceret PG F2α (prostinfenem) eller saltvand. Alle i PG-gruppen fødte selv placenta; mens alle i saltvandsgruppen fik lavet manuel placentafjernelse. Rogers et al randomiserede 34 fødende til enten 800 mkg misoprostol, 50 iu oxytocin eller 30 ml saltvand IUI. Succesraten var 57%, 19% og 46%. Ingen af forsøgene var blindede; men der findes her tydeligvis et potentiale, der bør undersøges nærmere.
Tocolytica
Der findes en del observationelle studier af glycerylnitrat (nitroglycerin (NG)) til frigørelse af placenta. Det teoretiske grundlag hviler på den udtalte relaksion af myometriet, der opstår ca. 1 minut efter injektion eller sublingual administration af NG og den ovennævnte forekomst af ’fastklemte’ placentae. Der findes dog kun til dato kun ét velgennemført RCT med 24 kvinder, hvor en IV injektion af 10 iu oxytocin ikke havde medført fødsel af placenta15. I NG-gruppen fødte 100% herefter placenta mod kun 8% i placebogruppen. Andre effekter var en 300 ml reduktion af det totale blodtab i NG-gruppen, men også et BT-fald på 5-6 mm Hg. Det skal bemærkes at der ikke forud for interventionen var forsøgt skelnet mellem fastsiddende og fastklemte placentae.
Sammenfatning
Manuel placentafjernelse er den mest effektive metode til at fjerne en retineret placenta eller dele heraf; men er samtidigt en metode der kræver analgesi og er forbundet med stort ubehag for den fødende og alvorlige komplikationer som yderligere blødning, infektion og lacerationer i cervix. En række mindre invasive metoder vil kunne øge sandsynligheden for at placenta exprimeres via de kontraktile kræfter i uterus eller ad modum Credé. Begynd med ’milde’ metoder, som ikke forstyrrer det naturlige fødselsforløb i nævneværdig grad, såsom uterin massage og akupunktur. UL vil kunne give retningslinier for rationel intervention. Findes der kliniske eller ultrasoniske tegn på en fastklemt placenta vil cervixmuskulaturen kunne forsøges afslappet med nitroglycerin for at få overstået efterbyrdsfasen. Såfremt uterus ikke umiddelbart herefter kan masseres til god tonus kan der igen gives et uterotonicum iht. PPH-guidelinen.
Findes der tegn på at placenta stadig har decidua-områder der ikke er separeret, kan det forsøges at opnå en høj oxytocin/prostaglandin koncentration tæt på det adhærente område. Dette opnås bedst v Pipingas teknik. Det kan diskuteres om det primære forsøg skal være med oxytocin, som er bedst undersøgt, men med sparsom effekt eller prostaglandin som i små studier har vist god effekt; men altså endnu i experimental fasen. Af sikkerhedsmæssige grunde har vi her valgt at anbefale oxytocin, som er kendt som et sikkert stof selv ved en hypotetisk overførsel fra placenta til den maternelle cirkulation.
Referencer
1. Cheung WM, Hawkes A, Ibish S, Weeks AD. The retained placenta: historical and geographical rate variations. J Obstet Gynaecol 2011; 31(1):37-42.
2. WHO. Pregnancy, childbirth, postpartum and newborn care: A guide for essential practice. 2006. Geneva, WHO.
3. Kenyon S, Ullman R, Mori R, Whittle M. Care of healthy women and their babies during childbirth: summary of NICE guidance. BMJ 2007; 335(7621):667-668.
4. Deneux-Tharaux C, Macfarlane A, Winter C, Zhang WH, Alexander S, Bouvier-Colle MH. Policies for manual removal of placenta at vaginal delivery: variations in timing within Europe. BJOG 2009; 116(1):119-124. 5. Magann EF, Evans S, Chauhan SP, Lanneau G, Fisk AD, Morrison JC. The length of the third stage of labor and the risk of postpartum hemorrhage. Obstet Gynecol 2005; 105(2):290-293. 6. Combs CA, Laros RK, Jr. Prolonged third stage of labor: morbidity and risk factors. Obstet Gynecol 1991; 77(6):863-867.
7. Weeks AD. The retained placenta. Best Pract Res Clin Obstet Gynaecol 2008; 22(6):1103-1117.
8. Rogers J, Wood J, McCandlish R, Ayers S, Truesdale A, Elbourne D. Active versus expectant management of third stage of labour: the Hinchingbrooke randomised controlled trial. Lancet 1998; 351(9104):693-699.
9. Herman A, Weinraub Z, Bukovsky I, Arieli S, Zabow P, Caspi E et al. Dynamic ultrasonographic imaging of the third stage of labor: new perspectives into third-stage mechanisms. Am J Obstet Gynecol 1993; 168(5):1496-1499.
10. Bullough CH, Msuku RS, Karonde L. Early suckling and postpartum haemorrhage: controlled trial in deliveries by traditional birth attendants. Lancet 1989; 2(8662):522-525.
11. Chauhan P, Gasser FJ, Chauhan AM. Clinical investigation on the use of acupuncture for treatment of placental retention. Am J Acupuncture 1998; 26:19-25.
12. Pipingas A, Hofmeyr GJ, Sesel KR. Umbilical vessel oxytocin administration for retained placenta: in vitro study of various infusion techniques. Am J Obstet Gynecol 1993; 168(3 Pt 1):793-795.
13. Mori R, Nardin JM, Yamamoto N, Carroli G, Weeks A. Umbilical vein injection for the routine management of third stage of labour. Cochrane Database Syst Rev 2012; 3:CD006176.
14. Nardin JM, Weeks A, Carroli G. Umbilical vein injection for management of retained placenta. Cochrane Database Syst Rev 2011;(5):CD001337.
15. Abdel-Aleem H, Abdel-Aleem MA, Shaaban OM. Tocolysis for management of retained placenta. Cochrane Database Syst Rev 2011;(1):CD007708.
Atoni
Medicinsk håndtering
Oxytocin
Oxytocin (Syntocinon£) er et syntetisk peptid, der har egenskaber identisk med hypofysebaglapshormonet oxytocin, der forstærker uterinkontraktioner og uterin tonus via oxytocinreceptorer i myometriet. Virkningen efter IV administration indtræder mere eller mindre øjeblikkeligt, mens den for IM injektion ses efter 3-5 min. Varighed af effekt efter IV administration er ca. 30min, mens den for IM injektion er 30-60min1.
De mest almindelige bivirkninger (1-10%) er kvalme, opkastning, bradykardi, takykardi og hovedpine. Hertil er beskrevet arytmier (0.1-1%). Hurtig indgift af ufortyndet oxytocin IV kan medføre kortvarig hypotension og myokardieiskæmi, hvorfor Lægemiddelstyrelsen tilråder forsigtighed ved kendt kardiovaskulær sygdom (promedicin.dk). Langsom infusion af større doser oxytocin øger risiko for vandintoksikation med elektrolytforstyrrelser, bevidsthedssløring og kramper pga den antidiuretiske effekt (drugs.com). Døgndosis bør derfor ikke overstige 40 IU.
Oxytocin til PPH
Oxytocin har traditionelt været førstevalg i rækken af uterotonika ved behandling af primær PPH forårsaget af atoni. Evidensen herfor er imidlertid yderst sparsom og internationale guidelines baseres således primært på ekstrapolering af resultater fra systematiske reviews omhandlende oxytocin anvendt som PPH profylakse.2,3 Der henvises til gennemgang af profylaktisk oxytocin i afsnittet ”Forebyggelse af PPH”.
Et stort multicenter dobbeltblindet RCT (N=809) fandt ligeværdig effekt af førstelinjebehandling med oxytocin sammenlignet med misoprostol hvad angik blødningsophør indenfor 20 min og postintervention blødning ≥500 ml.4 Misoprostolgruppen havde en ikke-signifikant øget risiko for postintervention blødning ≥1000 ml, ligesom der var større risiko for bivirkninger herunder kulderystelser og feber. Det bemærkes at doserne af uterotonika i RCT var markant højere end de der traditionelt anvendes i Danmark (40 IU syntocinon iv til indløb over 15 min vs 800 µg misoprostol sl).
I et mindre dobbeltblindet RCT (N=100) rapporterede Maged et al. et gennemsnitligt mindre blodtab efter administration af 100 µg carbetocin intravenøst sammenlignet med oxytocin 5 IU ved PPH (811 ml ± 389.17 ml vs. 1010 ml ± 525.66 ml; p=0.034) men ingen forskel mellem grupperne for blødning >1000 ml eller bivirkninger, herunder kvalme, kulderystelser, takykardi.5 RCT var begrænset af dets størrelse og i dansk kontekst ved inklusion af en studiepopulation der ikke havde modtaget PPH profylakse.
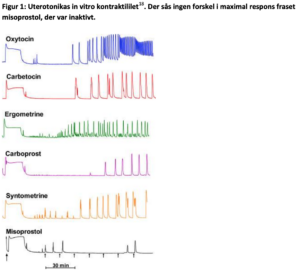
In vitro studier af isoleret myometriespån udtaget ved elektivt eller akut sectio fandt størst kontraktil effekt efter oxytocinbehandling sammenlignet med ergonovin, prostaglandin og misoprostol.6,7 Også efter oxytocin vestimulation havde oxytocin sammenlignet med øvrige uterotonika størst kontraktil effekt, og denne var større ved kombinationsbehandling med oxytocin plus ergonovine eller carboprost sammenlignet med oxytocin alene6,7
Guidelines internationalt
Mangel på robust evidens vedrørende den farmakologiske behandling af PPH afspejler sig i diskrepanser guidelines imellem. FIGO, WHO, samt guidelines fra Canada (RCOG), Frankrig (CNGOF) og Tyskland/Østrig/Schweiz (DGGG/OEGGG/SGGG) anbefaler trinvis administration af uterotonika med oxytocin først, mens guidelines fra USA (ACOG), Australien/New Zealand (RANZCOG) og Canada (SOGC) ikke definerer en rækkefølge.3 Administrationsform og dosis af oxytocin varierer ligeledes og er generelt mindre præcist beskrevet. Flere anbefaler 2-trins administration; initialt hurtig infusion IV alternativt injektion IM og herefter vedligeholdelsesinfusion.3,8 Ingen regimer er vist overlegne ifht andre.
Ergometrin (Metergin ®)
Methylergometrin (Metergin®)9-11 er et semi-syntetisk sekalalkaloid, der virker via α-adrenerge og serotonerge receptorer, og medfører derfor både øget uterus kontraktion samt vasokonstriktion. Methylergometrin har meget mindre vasokonstriktiv virkning end de oprindelige sekalalkoider. I uterus medfører de både øget tonus samt øget frekvens og amplitude af kontraktioner både i øvre og nedre segment. De elimineres via leveren. Virkningen indtræder øjeblikkeligt ved IV administration og efter 2-5min efter IM administration. Virkningen ophører 45min efter IV og 2-3t efter IM administration. Der ses hyppigt hypertension, hovedpine, kramper og underlivssmerter, imens kvalme og opkastninger er sjældnere. Meget sjældent er AMI og perifer vasokonstriktion angivet i produktresumeet. Således er svær hypertension og præeklampsi kontraindikation for behandling, hvorimod let og moderat hypertension behandles med forsigtighed.
Ergometrin til PPH
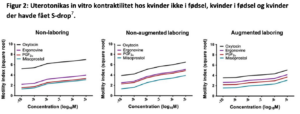
Sekalealkaloider var de første uterotonica, men havde oprindelig mange bivirkninger. Brugen af dem blev derfor afskaffet, da oxytocin blev opdaget. Siden er semi-syntetiske uterus specifikke sekalealkoloiderne methylergometrin og ergometrin blevet isoleret, og da disse har mindre vasokonstriktiv effekt har de langt færre bivirkninger9. De anbefales i de fleste nationale guidelines som sekundær uterotonica efter oxytocin12-16. Der findes få studier der undersøger ergometrins effekt som behandling af PPH. Et enkelt studie (n=1335) har retrospektivt opgjort forskel på behandling med methylergonovine og carboprost (Prostinfenem) til refraktær PPH efter sectio17. Her fandt de større risiko for blødnings relaterede morbiditet (blod transfusion, ligering af a.uterina/a. hypogastrica eller hysterectomi) hos kvinder der fik carboprost (17,4% vs 8,8%). Der foreligger flere studier, der ser på effekten af sekalealkaloider in vitro, undersøgt på myometrium biopsier taget i forbindelse med sectio. Her er ved flere forsøg fundet et større eller samme motilitets index (kontraktilitet) af ergometrin/ergonovin sammenlignet med carboprost, men mindre motitilites index end oxytocin (figur 1)6,7,18. Ligeledes er der lavet et in vitro studie, der ser på kontraktiliteten af myometrium biopsier taget ved sectio på kvinder, der ikke var i fødsel og sammenlignet disse med kvinder i fødsel og kvinder i fødsel, der havde modtaget S-drop19. Her fandt man at oxytocin havde mindre effekt på kvinder, der havde været i fødsel samt kvinder der havde fået S-drop, men at oxytocin fortsat var mere effektivt end alle andre uterotonica (figur 2)
Carboprost (Prostinfenem®)
Carboprost (Prostinfenem® )10,16,20 er et syntetisk prostaglandin F2α, der medfører langvarige uterinkontraktioner via prostaglandin receptorer i myometriet. Udover den direkte effekt på myometriet medfører prostaglandiner også øget oxytocin niveau. Carboprost virker desuden på glat muskulatur i GI-kanalen, pulmonalt samt i kar. Max virkning ses indenfor 15-30 min og varer op til 24 timer.
Bivirkninger ses meget hyppigt som opkastning, diarré, kvalme, øget temperatur og flushing. Ikke almindeligt i form af astma, dyspnø og hypertension og endelig sjældent i form af DIC, thyroideakrise og angst.
Således er behandling ved hjerte-, lunge-, nyre-, og leversygdom kontraindiceret.
Carboprost til PPH
Prostaglandiner er de uterotonica, der sidst er blevet opdaget9. Carboprost har som nævnt ovenfor vist sig at være mindre effektiv til behandling af PPH og have mindre kontraktil effekt end methylergometrin (figur 1 og 2). Desuden er der langt hyppigere bivirkninger i form af diarré samt opkastninger pga effekten på den glatte muskulatur i GI-kanalen21. Flere studier har dog vist effekt hos kvinder der har været refraktære overfor oxytocin og ergometrin19.
Carbetocin (Pabal ®)
Carbetocin (Pabal ®) er et syntetisk langtidsvirkende oxytocin, analog der er tilgængelig til parenteral behandling af PPH som følge af atoni og er stabil ved stuetemperatur (24 mdr. holdbarhed). Stoffet findes i 100mcg hætteglas, der ca. svarer til 50IU oxytocin aktivitet vurderet ved dyreforsøg. Injiceres IV langsomt over 1 min medførende 1 times uteruskontraktion, eller IM langsomt over 2 min medførende 2 timers kontraktion. Virkning opstår indenfor det første minut efter injektion. Bivirkninger er sammenlignelige imellem oxytocin og carbetocin, mens der sammenlignet med syntometrin (methergin og syntocinon kombinationspræparat) ses færre bivirkninger i form af hypertension, kvalme samt opkast ved Carbetocin.
Carbetocin til PPH
Carbetocin er i et Cochrane review22 vist at medføre mindre behov for yderligere uterotonica ved sectio ift oxytocin, samt medføre mindre blodtab ved vaginale fødsler, men der ses ingen forskel i risiko for PPH eller svær PPH. I direkte sammenligning med oxytocin er carbetocin ligeværdigt hvad angår både effekt og bivirkninger, men anvendelse ved PPH i forbindelse med vaginale fødsler er sparsomt undersøgt med kun to RCT5,23, hvor der var kvalitetsproblemer ved især det første af disse. Der sås færre bivirkninger i form af hypertension, kvalme samt opkast hos pt der fik Carbetocin ved sammenligning med syntometrin (methergin og syntocinon kombinationspræparat).
Carbetocin undersøges i øjeblikket ved direkte sammenligning med oxytocin i et stort multicenter RCT med 30.000 deltagere. Resultater forventes i 2018-2019 og kan potentielt medføre en ændret rolle ift. forebyggelse og/eller behandling af PPH.
På grund af de forskellige uterotonicas forskellige angrebspunkter, forekommer det rationelt at overveje flere former for uterotonika ved PPH. Ved massiv blødning kan carbetocin overvejes tidligt i behandlingsforløbet, men er aktuelt ikke en del af den anbfalede behandling af PPH efter vaginal forløsning, pga. den manglende dokumentation for denne situation.
Misoprostol (Cytotec®)
Misoprostol (Cytotec£) er et syntetisk prostaglandin E1 analog, der via prostaglandinreceptorer i myometriet fremkalder uteruskontraktioner/tonus. Virkningen indtræder meget varierende afhængig af administrationsrute. Ved oral administration indtræder virkningen efter 5-20 min, sublingualt efter 11 min, vaginalt efter 10-20 min og rektalt efter 30-100 min. Varighed af effekt efter oral/sublingual administration er 1-3 t, mens den for vaginal/rektal administration er 4-5 t24-26.
Misoprostol til PPH
Fire RCT har belyst effekten af adjuverende misoprostol i tillæg til standard uterotonika (oxytocin, methergin eller kombinationer heraf) ved behandling af PPH. I alle 4 studier var der givet PPH profylakse, overvejende oxytocin, i 3. stadie af fødslen27-30. Det største studie af Widmer et al inkluderede 1422 kvinder med klinisk PPH og fandt ingen gevinst efter administration af 600 µg misoprostol sublingualt vs placebo hverken for blødning ≥500 ml (14% vs 14%; RR=1.02 (0.79- 1.32)) eller for blødning ≥1000 ml (1% vs 1%; RR=1.02 (0.41-2.55))27. Tre mindre RCT manglede styrke til at demonstrere forskelle mellem misoprostol og placebogrupperne men viste favorable tendenser i blødningsmængden i misoprostol grupperne. Baseret på 238 kvinder med PPH beskrev Hofmeyr et al en ikke-signifikant reduktion af tilfælde med blødning ≥500 ml efter anvendelse af 1000 µg misoprostol vs placebo (5% vs 9%; RR=0.56 (0.21-1.46))28. Tilsvarende resultater rapporteredes for blødning ≥500 ml efter anvendelse af 600 µg misoprostol vs placebo både i Walravens studie (N=160; RR=0.58 (0.32-1.06)29 og i Zuberis studie (N=61; RR=0.59 (0.12-2.99))30. I en Cochrane metaanalyse fra 2014 af Mousa et al indgik ovennævnte 4 RCT 31. Baseret på i alt 1881 PPH cases fandt man intet additiv effekt af misoprostol ved standard PPH behandling på blødning ≥500 ml (RR=0.89 (0.71-1.12)), blødning ≥1000 ml (RR=0.88 (0.42-1.86)) eller blodtransfusion (RR=0.95 (0.77-1.17))31. På baggrund af metaanalysen kunne der i Cochrane reviewet ikke anbefales misoprostol som supplement til standardbehandling af PPH i settings hvor oxytocin er tilgængeligt31.
Nævnes bør endvidere Blums store multicenter dobbeltblindede RCT (N=809) som viste ligeværdig effekt af misoprostol 800 µg sl vs oxytocin 40 IE iv på blødningsophør inden for 20 min og blodtab ≥500 ml ved PPH efter PPH profylakse, men øget risiko for blødning ≥1000 imisoprostolgruppen (RR 3.62 (1.02-12.89))4 . Studiet medtages her, da der kan være situationer i klinikken hvor oxytocininfusion ikke umiddelbart er muligt.
Ét stort RCT (Winikoff et al, Lancet 2010)32 undersøgte misoprostol og oxytocin som førstelinjebehandling til PPH uden profylaktisk oxytocin. I scenarier uden umiddelbar tilgængelig oxytocin (fx ved hjemmefødsler), havde 90 % af 490 kvinder i studiet blødningskontrol efter 20min. Samme undersøgelse bekræftede oxytocin som en mere effektiv første linje behandling, da der i denne gruppe var 5.3 % færre (signifikant) med yderligere blødning.
Bivirkninger efter misoprostol til postpartum blødning.
Vi foretog en søgning på Pubmed ud fra MeSH terms ”misoprostol” AND ”postpartum hemorrhage” med 271 resultater. Studier publiceret indenfor de seneste 5 år blev gennemgået mhp. bivirkninger (feber og kulderystelser) efter administration af misoprostol.
Vi fandt 2 veldesignede RCTs af Widmer et al og Blum et al, der sammenlignede hhv. misoprostol vs oxytocin og misoprostol vs placebo blandt kvinder der havde modtaget PPH oxytocinprofylakse4,27.
Det fremgår af de bedst designede studier på området, at misoprostol øger forekomsten af kulderystelser og feber. Prostaglandiner passerer blod-hjerne barrieren og påvirker den fysiologiske kernetemperatur. Stigning i kernetemperaturen vil udløse kompensatoriske kulderystelser, hvorfor kulderystelser og feber kan betragtes som samme outcome.
I et Cochrane review omhandlende misoprostol behandling til PPH fra 2013 samler Hofmeyr et al. følgende for outcome feber >38C 33.
Forfatterne bemærker dog stor heterogenicitet i de evaluerede studier hvad angår outcome, under justerede forhold er resultaterne dog de samme.
Der er dosis sammenhæng i og med at effekten er tydeligere i doser på 600µg eller højere. Man konkluderer at brugen bør begrænses, og i så fald i laveste effektive dosis, doser over 800µg frarådes. I et tidligere review (Misoprostol to prevent and treat postpartum haemorrhage: a systematic review and meta-analysis of maternal deaths and dose-related effects) har samme forfatter på baggrund af en metaanalyse fundet at effekten på >1000ml blødning ikke er signifikant forskellig ift. 400µg vs. 600µg. Derimod finder de at bivirkninger (feber >38C) forekommer halvt så hyppigt. Studiet havde ikke nok power til at vise en evtuel forskel på de sjældent forekommende parametre svær morbiditet (behov for hysterektomi, intensiv behandling, blødning over 2000ml, organsvigt) og mortalitet.
Synergistisk effekt af misoprostol og anden uterotonica til postpartum blødning.
Det har været diskuteret om effekten af sekundær uterotonika (Carboprost (Prostifenem£) og Ergometrin (Methergin£)) kunne påvirkes af om der var givet Misoprostol (Cyotec£) eller ej. Det har ikke været muligt at finde studier der direkte belyser dette. Det ses dog både i Blums og Widmers studier4,27 at der ikke var forskel i brugen af yderligere uterotonica efter behandling med misoprostol vs oxytocin eller misoprostol vs placebo til behandling af PPH. Da der heller ikke var forskel på blødningsmængden mellem grupperne, kunne dette tyde på, at der heller ikke var forskel i effekten af netop den efterfølgende behandling.
Sammenfatning
Arbejdsgruppen konkluderer på baggrund af denne gennemgang, at der ikke er gevinst ved adjuverende misoprostol i situationer, hvor oxytocininfusion umiddelbart er tilgængeligt, pga både manglende dokumenteret effekt, mange bivirkninger samt lang tid til evt virkning. Efter at have gennemgået den sparsomme evidens for de øvrige uterotonika, der er tilgængelige til brug (pr. 2017 opdateringen), er det gruppens holdning at den aktuelle evidens tillader følgende rekommandation:
Ved PPH pga. atoni af uterus efter profylaktisk indgift af Syntocinon initieres:
- Koncentreret oxytocin-infusion eller hvis ingen iv adgang: injektion im iht. fødestedets lokale politik.
Ved behov desuden
- Ergometrin 0.2 mg IV/IM. Kan gentages max x 2. Kontraindiceret ved præeklampsi eller svær hypertension. og/eller
- Carboprost 0.25 mg IM. Kan gentages hver 15. min til max x8.
Der kan overvejes at supplere med følgende præparater (fx ved hjemmefødsel eller kontraindikation for Prostinfenem eller Methergin),
- Carbetocin 100mg IV
- Misoprostol 0,4mg sublingualt. Kun uden for hospital når syntocinon ikke kan administreres eller ikke er tilgængeligt
I praksis gives flere præparater simultant for opnåelse af hurtigt og vedvarende blødningsophør. Endelig bør løbende diagnostik af årsagen til blødning og overvejelser om mekanisk og/eller kirurgisk intervention altid praktiseres.
Referencer
1. https://www.drugs.com/pro/oxytocin.html. Last accessed December 2016.
2. Weeks A. The prevention and treatment of postpartum haemorrhage: what do we know, and where do we go to next? BJOG An Int J Obstet Gynaecol. 2015;122(2):202-210. doi:10.1111/1471- 0528.13098.
3. Sentilhes L, Goffinet F, Vayssière C, Deneux-Tharaux C. Comparison of postpartum haemorrhage guidelines: discrepancies underline our lack of knowledge. BJOG An Int J Obstet Gynaecol. September 2016. doi:10.1111/1471-0528.14305.
4. Blum J, Winikoff B, Raghavan S, et al. Treatment of post-partum haemorrhage with sublingual misoprostol versus oxytocin in women receiving prophylactic oxytocin: a double-blind, randomised, non-inferiority trial. Lancet (London, England). 2010;375(9710):217-223. doi:10.1016/S0140- 6736(09)61923-1.
5. Maged AM, Hassan AGMA, Shehata NAA. Carbetocin versus oxytocin in the management of atonic post partum haemorrhage (PPH) after vaginal delivery: a randomised controlled trial. Arch Gynecol Obstet. 2016;293(5):993-999. doi:10.1007/s00404-015-3911-y.
6. Balki M, Erik-Soussi M, Ramachandran N, Kingdom J, Carvalho JCA. The Contractile Effects of Oxytocin, Ergonovine, and Carboprost and Their Combinations. Anesth Analg. 2015;120(5):1074- 1084. doi:10.1213/ANE.0000000000000682.
7. Balki M, Erik-Soussi M, Kingdom J, Carvalho JCA. Comparative efficacy of uterotonic agents: in vitro contractions in isolated myometrial strips of labouring and non-labouring women. Can J Anesth Can d’anesthésie. 2014;61(9):808-818. doi:10.1007/s12630-014-0190-1.
8. Sentilhes L, Merlot B, Madar H, Sztark F, Brun S, Deneux-Tharaux C. Postpartum haemorrhage: prevention and treatment. Expert Rev Hematol. 2016;9(11):1043-1061. doi:10.1080/17474086.2016.1245135.
9. de Groot AN, van Dongen PW, Vree TB, Hekster YA, van Roosmalen J. Ergot alkaloids. Current status and review of clinical pharmacology and therapeutic use compared with other oxytocics in obstetrics and gynaecology. Drugs. 1998;56(4):523-535.
10. Gupta A. A comparative study of methylergonovine and 15-methyl prostaglandin F2α in active management of third stage of labor. Obstet Gynecol Sci. 2013;56(5):301-306. doi:10.5468/ogs.2013.56.5.301.
11. https://www.drugs.com/pro/methergine.html. Last accessed December 2016.
12. Royal College of Obstetricians and Gynaecologists. Postpartum Haemorrhage, Prevention and Management (Green-top Guideline No52). London: RCOG, 2011. [http://www.rcog.org.uk/womenshealth/clinical-guidance/prevention-and-management-postpartum-haemorrhage-green-top-52]. Last accessed 20 June 2016.
13. Dept. of Reproductive Health and Research W. WHO Recommendations for the Prevention and Treatment of Postpartum Haemorrhage. World Health Organization 2012. [http://apps.who.int/iris/bitstream/10665/75411/1/9789241548502_eng.pdf].; 2012. doi:10.1016/j.ijgo.2013.06.024.
14. American College of Obstetricians and Gynecologists. ACOG Practice Bulletin: Clinical Management Guidelines for Obstetrician-Gynecologists Number 76, October 2006: postpartum hemorrhage. Obstet Gynecol. 2006;108(4):1039-1047.
15. Royal College of Obstetricians and gynaecologists. Prevention and Management of Postpartum Haemorrhage, Peer Review Draft – September 2015. [https://www.rcog.org.uk/globalassets/documents/get-involved-in-ourwork/gtg_52_pph_pr_draft.pdf]. Last accessed October 2016.
16. Andersen H, Hopkins M. Postpartum Hemorrhage. Glob Libr women’s med. 2008. doi:10.3843/GLOWM.10138.
17. Butwick AJ, Carvalho B, Blumenfeld YJ, El-Sayed YY, Nelson LM, Bateman BT. Second-line uterotonics and the risk of hemorrhage-related morbidity. Am J Obstet Gynecol. 2015;212(5):642.e1-7. doi:10.1016/j.ajog.2015.01.008.
18. Morrison JJ, Crosby DA, Crankshaw DJ. In vitro contractile effects of agents used in the clinical management of postpartum haemorrhage. Eur J Pharmacol. 2016;789:328-333. doi:10.1016/j.ejphar.2016.07.025.
19. Oleen MA, Mariano JP. Controlling refractory atonic postpartum hemorrhage with Hemabate sterile solution. Am J Obstet Gynecol. 1990;162(1):205-208.
20. https://www.drugs.com/pro/hemabate.html. Last accessed December 2016.
21. Vaid A, Dadhwal V, Mittal S, et al. A randomized controlled trial of prophylactic sublingual misoprostol versus intramuscular methyl-ergometrine versus intramuscular 15-methyl PGF2alpha in active management of third stage of labor. Arch Gynecol Obstet. 2009;280(6):893-897. doi:10.1007/s00404-009-1019-y.
22. Ll S, Ys C, Samuel M, Su L-L, Chong Y-S, Samuel M. Carbetocin for preventing postpartum haemorrhage ( Review ). Cochrane Database Syst Rev. 2012;4(4):CD005457. doi:10.1002/14651858.CD005457.pub4.
23. Boucher M, Nimrod CA, Tawagi GF, Meeker TA, Rennicks White RE, Varin J. Comparison of carbetocin and oxytocin for the prevention of postpartum hemorrhage following vaginal delivery:a double-blind randomized trial. J Obstet Gynaecol Can. 2004;26(5):481-488. http://www.ncbi.nlm.nih.gov/pubmed/15151735. Accessed October 16, 2016.
24. Meckstroth KR, Whitaker AK, Bertisch S, Goldberg AB, Darney PD. Misoprostol administered by epithelial routes: Drug absorption and uterine response. Obstet Gynecol. 2006;108(3 Pt 1):582-590. doi:10.1097/01.AOG.0000230398.32794.9d.
25. Khan R-U, El-Refaey H, Sharma S, Sooranna D, Stafford M. Oral, rectal, and vaginal pharmacokinetics of misoprostol. Obstet Gynecol. 2004;103(5 Pt 1):866-870. doi:10.1097/01.AOG.0000124783.38974.53.
26. Tang OS, Gemzell-Danielsson K, Ho PC. Misoprostol: pharmacokinetic profiles, effects on the uterus and side-effects. Int J Gynaecol Obstet. 2007;99 Suppl 2:S160-7. doi:10.1016/j.ijgo.2007.09.004.
27. Widmer M, Blum J, Hofmeyr GJ, et al. Misoprostol as an adjunct to standard uterotonics for treatment of post-partum haemorrhage: a multicentre, double-blind randomised trial. Lancet (London, England). 2010;375(9728):1808-1813. doi:10.1016/S0140-6736(10)60348-0.
28. Hofmeyr GJ, Ferreira S, Nikodem VC, et al. Misoprostol for treating postpartum haemorrhage: a randomized controlled trial [ISRCTN72263357]. BMC Pregnancy Childbirth. 2004;4(1):16. doi:10.1186/1471-2393-4-16.
29. Walraven G, Dampha Y, Bittaye B, Sowe M, Hofmeyr J. Misoprostol in the treatment of postpartum haemorrhage in addition to routine management: a placebo randomised controlled trial. BJOG. 2004;111(9):1014-1017. doi:10.1111/j.1471-0528.2004.00217.x.
30. Zuberi NF, Durocher J, Sikander R, Baber N, Blum J, Walraven G. Misoprostol in addition to routine treatment of postpartum hemorrhage: a hospital-based randomized-controlled trial in Karachi, Pakistan. BMC Pregnancy Childbirth. 2008;8:40. doi:10.1186/1471-2393-8-40.
31. Mousa HA, Blum J, Abou El Senoun G, Shakur H, Alfirevic Z. Treatment for primary postpartum haemorrhage. Cochrane database Syst Rev. 2014;2:CD003249. doi:10.1002/14651858.CD003249.pub3.
32. Winikoff B, Dabash R, Durocher J, et al. Treatment of post-partum haemorrhage with sublingual misoprostol versus oxytocin in women not exposed to oxytocin during labour: a double-blind, randomised, non-inferiority trial. Lancet. 2010;375(9710):210-216. doi:10.1016/S0140- 6736(09)61924-3.
33. Hofmeyr GJ, Gülmezoglu AM, Novikova N, Lawrie TA. Postpartum misoprostol for preventing maternal mortality and morbidity. Cochrane database Syst Rev. 2013;7:CD008982. doi:10.1002/14651858.CD008982.pub2.
Tamponade og kirurgisk behandling
Tilfælde hvor PPH ikke kan kontrolleres konservativt medicinsk, og hvor retineret væv, vaginalrifter og koagulopati er udelukket kræver akut kirurgisk intervention. Behandlingen er udfordrende, da der ikke er nogle regelrette rekommandationer eller RCT’er for behandling. Traditionelt har behandlingstilbuddet i disse situationer været akut hysterektomi og/eller evt. ligering af arteria iliaca interna.
Gennem de sidste årtier er alternative mere skånsomme og ikke mindst fertilitetsbevarende behandlingsmetoder blevet introduceret og disse vil blive gennemgået i det følgende. Der er rapporteret utrolig mange kirurgiske metoder. Fælles for dem er at der er meget lav evidens.
Vi har i guideline gruppen valgt at beskrive de metoder vi finder mest anbefalelsesværdige. Overordnet kan man ud fra litteraturen næppe fremhæve en metode frem for en anden, men vores anbefaling er at man i hver enkelt afdeling indøver få simple metoder til hver enkelt situation, således at relevant behandling ikke forsinkes. I et review fra 2007 over 46 studier er der fundet en succes rate på 90,7 % for arteriel embolisering, 84,0 % for ballon tamponade, 91,7 % for kompressions suturer samt 84,6 % for arteriel ligering (1).
Jo før relevant behandling institueres des større er chancen for at undgå evt. koagulationsforstyrrelser og dermed medicinsk blødning og des mindre invasiv kan man være. Alle de nedenfor nævnte metoder forudsætter pt i UA, med KAD.
Anbefalinger fra nogle af de udenlandske selskaber er her kort beskrevet:
RCOG: Obstetrikere skal overveje alle options inkl. stepvise devaskularisering, bilat ligatur af arterier, embolisering og i sidste ende hysterektomi (grad C).
ACOG: Manglende effekt af medicinsk behandling med eller uden tamponade efter vaginal fødsel skal medføre ekspl. laparotomi. Kir.teknikker er: bilat. aa uterina ligatur/stepvise devaskularisering, B-lynch, hæmostatiske multiple kvadrantsuturer ved atoni og prævia/accreta. Embolisering ved stabile vitale tegn
SGOC: Ligatur af a.iliaca int., kompressionsuturer og i sidste ende hysterektomi. Embolisering ved hæmodynamisk stabil pt før evt kirurgisk intervention.
WHO: Embolisering hvis muligt som en ”second line” behandlingsmulighed ved atoni, idet evidens bag er ringe. Kir. Teknikker som ovenfor nævnt (40).
Tamponade ved atoni eller blødning fra placentaleje
Før evt laparotomi skal pt undersøges i UA. Der foretages intrauterin palpation og vaginalinspektion. I forbindelse med dette kan tamponade test foretages. Ved effekt kan laparotomi undgåes, ved forsat blødning går man videre med laparotomi. Overordnet er der 2 muligheder for at tamponere uterus;
– tamponade med kateter
– tamponade med servietter/gaze
Uterustamponade med ballonkateter.
Uterin tamponade kan udføres ved at udøve pres mod placentastedet, og er en nem, hurtig og effektiv måde at håndtere PPH der IKKE skyldes retineret væv, læsioner eller medicinsk blødning (41).
Der er ingen RCTèr vedr. tamponade i behandling af PPH, men de sidste par år har ballonkateterbehandling været foretrukket frem for uterintamponade med servietter(37).
Effekten af tamponade med ballon skyldes en kombination af ændret uterinstørrelse, sekundær uterin aktivitet, ballon/endometrieinteraktioner og påvirkning af flowet i aa.uterina(7,38)
Ballontamponade kan være en livreddende procedure, den er let og kræver minimal anæstesi,kan udføres af selv uøvede personale, er let og smertefri at fjerne og manglende effekt kan identificeres let. Det er en procedure der i u-lande kan udføres relativt let da man der ved hjælp af en slange og en handske kan danne en ballonkateter.
Der er ikke beskrevet komplikationer relateret til indgrebet og heller ikke langtids komplikationer, men den herskende anbefaling er at behandle med antibiotika iforbindelse med indgrebet(2, 39)
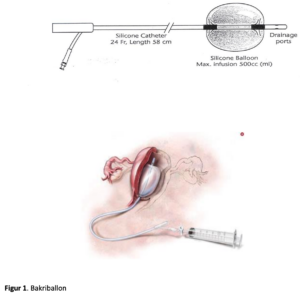
Bakriballon.
Bakri ballonkateter er specialudviklet til tamponade af uterus ved PPH, og er specielt velegnet til blødning fra lavtliggende placentasted. Katetret adskiller sig fra andre katetre ved at ballonen kan indeholde op til 800 ml NaCl/sterilt vand, der er lavet 2 drænage huller så blodet kan løbe fra uterus, og materialet er silicone der ikke adhærerer til uterinvæggen, hvilket nedsætter risiko for fornyet blødning ved seponering af katetret (fig 1). I et nyere studie med 50 cases fra Finland blev der fundet en succes rate på 86 % (8).
Procedure: Sterilt Bakriballonkateter placeres med spidsen i uterus. Vagina pakkes med servietter så katetret ikke displaceres når ballonen fyldes.
Ballonen fyldes til tamponade opnåes. Der anbefales 250- 500 ml NaCl.
Blodet fra uterus drænerer gn de 2 huller i katetret og effekt kan dermed vurderes umiddelbart. Det anbefales dog fortsat kontinuerligt at vurdere størrelsen på uterus for at udelukke intrauterin blødning, der ikke dræneres pga. fx koagler i kateret.
Katetret seponeres efter 24 timer.
Der anbefales til alle katetermetoderne:
Kontinuerligt s-drop med 20-40 ie syntocinon i 1000 ml NaCl indtil katetret er seponeret, samt 3 døgn bredspektret antibiotika (2).
Tamponade med gaze/servietter/mescher
Uterin pakning er beskrevet i gynækologiske tekstbøger fra 1930érne og 40érne.
Delee & Greenwood rapporterede i 40érne 400 tilfælde med postpartum blødning hvoraf 398 med succes blev behandlet med pakning af uterus. Der er i litteraturen beskrevet over 1000 tilfælde hvor uterin pakning er anvendt, og der er ikke rapporteret alvorlige infektioner. Der foreligger ingen sikre data om efterfølgende fertilitet.
Procedure:
Til pakning kan anvendes alle former for mecher/gaze eller servietter, bare de er bundet sammen. Det er vigtigt at caviteten udfyldes helt for at undgå et deadspace med risiko for blødning. Mescherne kan ligge 24-36 timer, og der behandles med bredspektret antibiotika.
Syntese
Der er ingen eller højst evidensgrad 3 for anvendelse af tamponade ved intraktabel postpartum blødning. Tamponade katetre kan evt anvendes som ”tamponadetest” men i Danmark hvor der er anæstesiservice på alle fødesteder må laparotomi anbefales ved manglende effekt. Bakriballon 1.valg, uterin pakning kan bruges såfremt Bakriballon ell.lign ikke er tilgængelig, eller ved overflytning til tertiært center
Blødning fra nedre segment
Blødning svarende til placentastedet, især hvis dette ligger i nedre segment, kan blive meget kraftig og er ofte resistent overfor medicinsk behandling, idet muskelfibrene i det nedre segment ikke har samme kontraktile egenskaber som i resten af uterus. Blødning skyldes ofte store dilaterede kar og her er kirurgisk behandling førstevalg, kombineret med prostinfenem og syntocinom im.
Gennemstikninger
Alle forfattere anbefaler at man som en start forsøger horizontale gennemstikninger. Tamizian et al anvender teknik med dybe (helvægs), horizontale gennemstikninger over og under blødningsstedet (5).
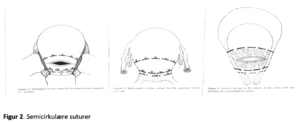
Semicirkulær suturer
Cho et al har beskrevet en serie med 8 pt med intraktabel postpartum blødning fra nedre segment, hvor hysterektomi var indiceret. Før dette indgreb forsøgte man at anlægge flere tværgående suturlinier over og under uterotomien medinddragende a.uterina lateralt (fig 2). Alle 8 ptt undgik hysterektomi, 2 fik postpartum feber, behandlet med antibiotika.
Teknik:
Initialt anlægges en suturlinie nedadtil svarende til den vesikouterine overgang i uterus for og bagvæg, samt en linie 4-5 cm over uterotomien. Suturerne er 2-3 cm lange med ca 1 cm interval, dybt ned i endometriet.Lateralt skal a.uterina inkluderes.
Ved manglende effekt kan parallelle suturlinier anlægges men pas på vævsnekrose. Materiale: resorberbar 0-1 (11).
Ballontamponade (se under 1)
Bakri ballonkateter er primært udviklet til tamponade af intraktabel blødning fra nedre segment ved placenta prævia. Hvis enkelte gennemstikninger ikke giver hæmostase anbefales at man peroperativt anlægger ballonkateter.
Dette er beskrevet anvendt på 5 ptt med god effekt (2).
Teknik: Ballonkateter anlægges med distale ende ned i vagina. Uterotomien og hud lukkes. Vagina pakkes og ballonen fyldes til tamponade opnåes med 250-500 ml NaCl. Handske træk appliceres således at der er maximum tryk på nedre segment.
Kateter seponeres efter 24 timer. 3 døgn antibiotika anbefales.
Sammenfatning
Der er evidensgrad 2-3 på de rapporterede metoder. Guideline gruppen anbefaler gennemstikninger samt ballonkateter ved nedre segment blødning.
Uterus kompressionssuturer
Lynch et al beskrev i 1997, som de første en teknik hvor man kirurgisk anlægger kompression på uterus som alternativ til hysterektomi ved intraktabel PPH (14).
Siden er teknikken modificerede og alternative kompressions metoder beskrevet.
Hvis bimanuel kompression af uterus virker kan B-Lynch suturteknik forventes at have effekt, så det anbefales altid at komprimere inden det kirurgiske indgreb.
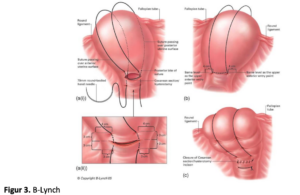
B-Lynch sutur (se figur 3)
Teknik: Indgrebet foretages ved laparotomi gennem nedre tværsnit evt i forbindelse med sectio.
Sutur: 0 eller 1 resorberbar, stor nål (70 mm) og 90 cm lang.
- Indstik 3 cm under højre hjørne af uterotomien og 3 cm fra laterale højre uterinhjørne.
- Før nålen ud 3 cm over højre hjørne af uterotomien og ca 4 cm fra højre uterinrand.
- Suturen føres udvendigt op over fundus uteri ca 3-4 cm fra uterinhjørnet og videre ned over bagsiden af uterus, ”som et par seler”.
- Indstik på bagsiden på samme niveau som på forsiden, suturen strammes op bl.a ved at lade en assistent komprimere uterus.
- Suturen føres horizontalt, nålen stikkes ud på bagsiden, symmetrisk med indstik.
- Suturen føres udvendig op over fundus uteri parallelt med suturen i højre side.
- Ind- og udstik i venstre side ved uterotomien symmetrisk med ind- og udstik i højre side.
- De to ender knyttes sammen, mens en assistent komprimerer uterus, og suturen kommer til at ligge ca 3 cm under uterotomien.
- Uterotomien lukkes på vanlig vis.
- Effekt af behandlingen sikres inden abdomen lukkes.
Antibiotikaprofylakse anbefales.
Syntocinon drop med 20-40 ie/500 ml NaCl, 60 ml/h, aftrappes over 8 timer.
C.B-Lynch rapporterede metoden anvendt til 5 ptt med intraktabel postpartum blødning i 1997. Alle havde effekt af behandlingen, dvs ingen blev hysterektomeret. To gennemførte senere normale graviditeter. Tilsvarende har Ferguson et al med succes behandlet 2 ptt med B-Lynch med succes. Disse ptt blev efterfølgende kontrolleret med HSG og MR. Begge undersøgelser viste normale uterincaviteter.
B-Lynch suturteknik er let at udføre, og der er rapporteret få alvorlige komplikationer, bl.a en enkel pt med erosion af suturen gennem uterin væggen samt en enkel med uterin nekrose (1, 14- 17).
Modificeret B-Lynch suturteknik er foreslået både ved sectio med atoni, blødning fra nedre segment og ved atoni efter vaginalfødsel.
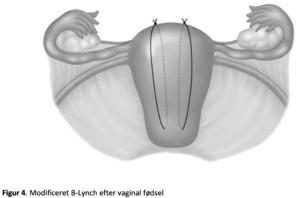
Modificeret B-Lynch efter vaginal fødsel
I 2002 har Hayman et al i tilfælde af laparotomi efter vaginalfødsel hvor der ikke er uterotomi foreslået modificerede B-Lynch ”seler” (18). Man fandt peroperativt atonisk uterus samt velkontraheret nedre segment. Oprindeligt placeres 4 suturer, men seneste opgørelser viser god succesrate ved 2 suturer (19, 20)
Teknik (fig 4):
1. 2 stk resorberbare suturer 0 eller 1 på lige nål.
2. Indstik fra uterus forside, over blærens omslagsfold, svt hvor uterotomien ville have været. Indstikket skal være gennem for og bagvæg.
3. De 2 suturer placeres i linie horizontalt og knyttes sv.t fundus, mens assistenten komprimerer uterus.
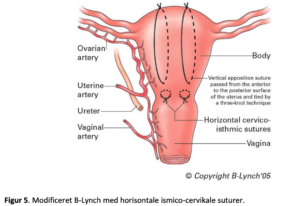
Modificeret B-Lynch ved atoni og nedre segment blødning
Ved nedre segment blødning efter sectio fx efter prævia anbefaler flere forfattere B-Lynch kombineret med ”isthmic-cervicale” horizontale suturer(4,16) (fig 5).
Teknik: resorberbar 2-0 på lige nål.
1. Indstik fra uterus anterior side lige over blærens omslagsfold, 3 cm under uterotomien, 2 cm medialt for uterus lateralkant.
2. Tilbage fra posterior til anteriorside 1 – 2 cm medialt for indstikket.
3. Proceduren gentages på modsatte side.
4. Tampontang i cervix sikrer passage.
5. Suturer knyttes.
6. Slutteligt B-Lynch (fig 3) eller modificeret B-lynch (fig 4).
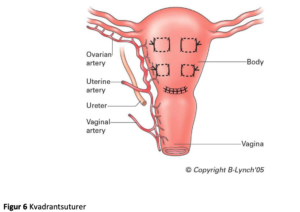
Kvadrant suturer.
Cho et al har foreslået en alternativ teknik kaldet ”multiple square suturing” (kvadrant suturer), hvor uterus for- og bagvæg approximeres med suturer til uterincaviteten er aflukket (21).
Teknik (fig. 6):
Indgrebet foretages ved laparotomi gennem nedre tværsnit
Sutur: resorberbar 0 eller 1 på lige nål
1. Et punkt på uterus vælges, helst sv.t blødningsmax.
2. Instik gennem for og bagvæg med sutur på lige nål.
3. Næste punkt vælges 2-3 cm lateralt og der stikkes gennem bagvæg til forvæggen, og igen fra forvæg til bagvæg 2-3 cm over eller under første suturlinie således at en firkant dannes hvorefter knuden bindes
4. Flere firkanter anlægges svarende til blødningsområder.
Ved atoni anbefales 4-5 firkanter fra fundus til nedre segment
Ved blødning sfa prævia eller placenta accreta kan firkanterne anlægges sv.t nedre segment, efter at blæren er refouleret
Primært blev en serie på 23 kvinder med intraktabel PPH efter sectio rapporteret. Alle fik anlagt ovennævnte suturer med god effekt. Af de 23 havde 10 efterfølgende graviditetsønske. HSG hos 6 ptt var ia, 4 gennemførte normal graviditet og fødsel. Alle 23 havde normal menstruation efter operationen (21, 22).
Ingen komplikationer blev fundet i det primære studie men efterfølgende er der rapporteret et enkelt tilfælde med pyometra 4 uger postpartum samt tilfælde med Aschermans synecchier (23). Fordelen ved kvadrant suturerne er at teknikken er sikker og let at udføre.
Komplikationer ved B.Lynch og andre kompressionsuturer er beskrevet, men kun kasuistiske. Nyere referencer beskriver få kort – og langsigtede komplikationer, overvejende pyometra på baggrund af uterin iskæmi.
Der er ikke beskrevet fertilitetsproblemer efter kompressionssuturerne. 15 kvinder med B-lynch. 12 undgår hysterectomi, 3 hysterectomeres , den ene pga pyometra efter iskæmisk uterus efter suturerne, de 2 andre pga vedvarende blødning. Konklusion: BL ser ud til at være sikker (24) effektiv og uden kort eller langsigtede komplikationer (25).
Når udført korrekt er der ingen øget risiko for komplikationer. Udført i forbindelse med devaskularisation er der måske risiko for uterin iskæmi i nogle tilfælde (26). Der er ingen kirurgiske komplikationer (27)
Sammenfatning
Anvendelse af kompressionssuturer har evidens 2-3. Alle er simple og ukomplicerede at udføre. Komplikationer ved B-Lynch og andre kompressionssuturer er beskrevet, men kun kasuistisk. Guideline gruppen anbefaler B-Lynch som metoden ved atoni, og evt modificeret B-Lynch ved samtidig nedre segment blødning, men den ene metode kan næppe fremhæves fremfor den anden hvad angår effekt.
Ligering af kar
Abdominal ligering af a.uterina
Abdominal ligering af arteria uterina er første gang beskrevet i 1952 af Waters (28).
90 % af uterus blodforsyning stammer fra a.uterina og bilateral ligering af a.uterinae har vist effekt på blødningen i op til 80 % af tilfældene således at hysterectomi er undgået (29-32).
I et retrospektivt studie publiseret i 1995 rapporterede O`Leary et al 265 ptt hvor man grundet postpartum blødning efter sectio foretog ligering af arteriae og venae.uterinae. Der var effekt i helt op til 95 % af tilfældene, hvormed hysterektomi blev undgået (29).
Teknikken er nem, hurtig og der er rapporteret meget få komplikationer.
Teknik:
1. Laparotomi ved nedre tværsnit
2. Blæreperitoneum incideres og blæren refouleres
3. Uterus løftes op og et avasculært område i ligamentum latum identificeres
4. Sutur 0-1 resorberbar atraumatisk på stor nål anvendes. Gennemstikning medialt for a.uterina, medinddragende myometrium, og ud gennem det avasculære vindue på niveau med den vesicouterine overgang
5. Gøres bilateralt
Vaginal ligering af a.uterina.
Behersker man vaginale operationer kan ligering af a.uterina ligeledes foretages vaginalt, med samme effekt som nævnt ovenfor (33, 34).
Trinvis devascularisering
Abdrabdo publiserede i 1994 et studie med 103 ptt med postpartum blødning behandlet med trinvis devascularisering, forud for evt hysterektomi.
Princippet er at man følger trin for trin indtil blødningen ophører (30), (fig 1)
Trin:
1a. Unilateral ligering af a.uterina
1b. Kontralateral lig.af a.uterina
2. Bilateral lav ligering af a.uterina:
Blæren incideres og blæren refouleres.Bilaterale dybe genemstikninger 3-5 cm under de første gennemstikninger medinddragende myometrium medialt. Med disse gennemstikninger kuperes den cervicovaginale gren af a.uterina
3a. Unilateral ligering af a.ovarica
3b. Kontralateral lig. af a.ovarica
Effekt trin for trin:
1a: 8,7 % blødningsophør
1b: 74,8 % blødningsophør, især atonierne
2: 3,9 % blødningsophør, typisk prævia hvor trin 1+2 ikke er nok
3a: 6,8 %
3b: 5,8 %
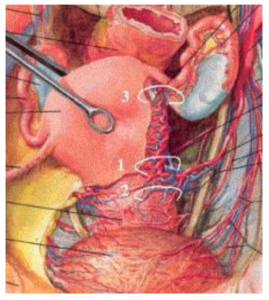
Figur 7. Trinvis devaskularisering. Hvert trin (1,2,3) efterfølges af ligering af den kontralaterale side før der progredieres til næste trin (se tekst ovenfor).
Ligering af a.iliaca interna.
Bilateral ligering af a.iliaca interna er i flere undersøgelser vist at have en effekt på blødningen hos 40-42 % (5, 36).
Operationen er vanskelig og kræver øvede operatører. Der er rapporteret alvorlige komplikationer med ureter, vene og nerve læsioner samt nedsat flow til glutealmuskulatur, perineum og pelvis med risiko for ischæmi og i sjældne tilfælde nekroser (32,36). Postpartum hysterectomi efter ligering af a.iliaca interna er beskrevet forbundet med øgede komplikationer, i forhold til hvis a.iliaca int. ikke var ligeret inden hysterektomien (36, 37). Ved forsat blødning trods medicin, B-Lynch, og evt trinvis devascularisering kan ligering af a.iliaca ikke forventes at give yderligere effekt. Hvis metoden alligevel anvendes må det anbefales at operatøren er rutineret i at operere på bækkenvæggen og i retroperitoneum.
Sammenfatning
Ligering af arteria uterina, og a.iliaca interna har evidensgrad 1-2. Det anbefales altid at overveje kompressionssuturer inden ligering af kar. Evt kan B-Lynch kombineres med trinvis devascularisering. Ligering af a.iliaca interna er kun meget sjældent indiceret, og bør forbeholdes meget rutinerede kirurger, evt karkirurger.
Alle de nævnte metoder forsøges for at undgå akut hysterektomi. Foretages dette alligevel er der ingen signifikant forskel på om man vælger subtotal eller total hysterektomi hvad angår operationstid, blødningsmængde eller komplikationer. Anbefalingen må dog være at ved nedre segment blødning skal man foretage total hysterektomi.
Postpartum hysterectomi
Traditionelt har behandlingen af intraktabel postpartum blødning været ligering af a.iliaca interna og ved manglende effekt hysterektomi.
I et stort retospektivt studie i perioden 1978-82 har Clark et al registreret ialt 70 postpartum hysterektomier, heraf 60 efter sectio svarende til 0,7 % af alle sectioer, og 10 efter vaginal fødsel sv.t 0,02 % af det samlede antal vaginale fødsler.
46 % fik udført total abdominal hysterektomi og 54 % subtotal hysterektomi.
Forfatterne fandt ingen forskel på de 2 operationsmetoder hvad angår blodtab, operationstid, indlæggelsestid og komplikationer. Forfatterne anfører at valg af operationsmetode må afhænge af udløsende årsag. Ved atoni er subtotal hysterektomi effektiv, mens blødning som følge af placenta accreta vil kræve total hysterektomi for at stoppe blødningen, idet den cervicovaginale gren af a.uterina skal kuperes (33, 5). I et nyere review fra 2010 fandtes en lignende incidens på 0,02-0,5 % blandt fødende, og af de der fik hysterektomi var 73,2 % foretaget efter sectio (34).
Teknik
1. Laparotomi gn nedre tværsnit.
2. Rotunde ligamenter kuperes med gennemstikninger.
3. Lig.proprium ovarii kuperes med gennemstikninger.
4. Blæreperitoneum incideres og blæren refouleres.
5. Posteriore blad af det brede ligament incideres til de sacrouterine ligamenter.
6. Aa.uterinae kuperes med gennemstikninger.
7. Ved subtotal hysterectomi fjernes corpus uteri og cervixstumpen lukkes med enkeltknuder.
8. Ved total hysterectomi dissikeres blæren fri af cervix til toppen af vagina visualiseres.
9. De cardinale ligamenter gennemstikkes.
10. Hvis cervix har været dilateret åbnes uterus via lav uterotomi og en finger føres ind i caviteten ned gennem cervix således at fornix anterior markeres.
11. Vaginaltoppen åbnes i midten, så tæt på cervix som muligt og uterus fjernes.
12. Vaginaltoppen lukkes med hjørnesuturer og enkeltknuder.
13. Postoperativ tæt monitorering.
14. Peroperativt anbefales antibiotika og postoperativt tromboseprofylakse.
Abdominal pakning:
Trods postpartum hysterektomi ser man af og til forsat blødning diffust i det lille bækken, oftest som følge af forbrugs koagulopati.
Ved manglende effekt af el koagulation og gennemstikninger kan abdominal pakning være nyttig.
Metode:
Man pakker bækkenet tæt med duge og/eller servietter. Disse fjernes efter 24 timer når koagulopatien er korrigeret.
Metoden anvendes indenfor de fleste kirurgiske specialer ved ukontrollabel blødning.
Referencer
1. Doumouchtsis S.K, Papageorghiou A.T, Arulkumaran S. Systematic review of conservative management of postpartum hemorrhage: What to do when medical treatment fails. Obstet Gynecol Surv 2007; 62(8); 540-7.
2. Bakri Y.N, Amri A, Jabbar F.Tamponadeballon for obstetrical bleeding. Int J Gynecol Obstet 2001.
3. Katesmark M, Brown R, Raju K.S.Succesful use of sengstaken-Blakemore tube to control massive postpartum hemorrhage. Br J Obstet Gynecol.1994;101;259-60
4. Deloor J.A,Dam P.,Foleycatheters for uncontrollable obstetric or gynecologic hemorrhage. 1996.vol 8(4),737.
5. Tamizian O.,Aralkumaran S.The surgical management of postpartum hemorrhage. Clinical obstetrics and gyencology 2002.vol 16,1,81-98
6. Johanson R,Kumar M, Obhrai M,Young P. Management of massive postpartum hemorrhage;use of a hydrostatic ballooncatheter to avoid laparotomy.Br J Obstet Gynecol 2001,vol 108,420-22.
7. Georgiou C. Balloon tamponade in the management of postpartum haemorrhage: a review. BJOG 2009; 116(6); 748-57.
8. Grönvall M, Tikkanen M, Tallberg E. Use of Bakri balloon tamponade in the treatment of postpartum hemorrhage: A series of 50 cases from a tertiary teaching hospital. Acta Obstet Gynecol Scand 2012 Aug. 22.
9. Maier R.Control of postpartum hemorrhage with uterine packing. Am J Obstet Gynecol.1993;169;317-23.
10. Hsu S, Rodgers B, Lele A. Use of packing in obstetric hemorrhage of uterine origin. J Reprod Med 2003; 48(2); 69-71.
11. Cho J, Kim sS, Cha K et al. Interrupted circular suture:Bleeding control during cesarean delivery in placenta previa accreta.Obstet Gynecol 1991.78;876-79.
12. Bonnar J.Massive obstetric hemorrhage.Clinical obstetrics and gynecology.2000,vol 14,1-18.
13. Tamizian O,Aralkumaran S. The surgical management of postpartum hemorrhage.Current opinion in obstetrics and gynecology.2001;13;127-31.
14. Lynch C.B,Coker A,Laural A,Abu J,Cowen M.B-Lynch surgical technique for the control of massive postpartum hemorrhage; an alternative to hysterectomy ?Five cases reported. Br J Obstet Gynecol.1997,104,372-75.
15. Wergeland H,Alagic E,Lokvik B.Use of B-Lynch suturing technique in postpartum hemorrhage.Tidsskr Nor.Laegefore.2002.122,370-2.
16. Ferguson J.E,Bourgeois J. Underwood P.B-Lynch suture for postpartum hemorrhage.Obstet Gynecol 2002,95(6),1020-22.
17. Dildy G.Postpartum hemorrhage:New management options.Clinical obstetrics and gynecology.2002.vol 45(2).330-344.
18. Hayman R.G, Aralkumaran S,Steer P. Uterine compression sutures; surgical management of postpartum hemorrhage.Obstet Gynecol 2002;99(3),502-5.
19. Nanda S, Singhal S.R, Hayman uterine compression stich for arresting atonic postpartum hemorrhage: 5 year experience. Taiwan J Obstet Gynecol. 2011; 50(2); 179-81.
20. Ghezzi F, Cromi A, Uccella S. The Hayman technique: a simple method to treat postpartum haemorrhage. BJOG. 2007; 114(3); 362-5.
21. Cho J,Jun H, Lee C. Hemostatic suturing technique for uterine bleeding during cesarean delivery. Obstet Gynecol 2000;96;129-31.
22. Chen C,Chang T,Yen L et al. Appearance of the uterus after simple square suturing for rapid control of postpartum hemorrhage and preservation of fertility.J Clin Ultrasound,2002.30.189-91.
23. Ochoa M,Allaire A,Stitely M.Pyometra after hemostatic square suture technique.Obstet Gynecol 2002.99.506-9.
24. Sentilhes L et alActa Obstet Gynecol Scand. 2008;87(10):1020-6
25. Tsitlakidis C et al.Ten year follow-up of the effect of the B-Lynch uterine compression suture for massive postpartum hemorrhage. Int J Fertil Womens Med. 2006 Nov-Dec;51(6):262-5.)
26. C. Fotopoulou .Uterine compression sutures for preserving fertility in severe postpartum haemorrhage: An overview 13 years after the first description. J Obstet gynaecol;May 2010, Vol. 30, No. 4 , Pages 339-349)
27. Hackethal A et al. Uterine Compression U-sutures in Primary Postpartum Hemorrhage After Cesarean Section: Fertility Preservation With a Simple and Effective Technique Hum Reprod. 2008;23(1):74-79. © 2008 Oxford University Press )
28. Waters E.G.Surgical management og postpartum hemorrhage with particular reference to ligation of uterine arteries.Am J Obstet Gynecol.1952.64,1143-8.
29. O´Leary J.A. Uterine artery ligation in control of postcesarean hemorrhage.J reprod med.1995;40;189-93.
30. Abdrabbo .Stepwise uterine devascularisation.A novel technique for management of uncontrollable postpartum hemorrhage with preservation of the uterus.Am J Obstet Gynecol.1994,171(3),694-99.
31. Fahmy K.Uterine artery ligation to control postpartum hemorrhage.Int J Obstet Gynecol.1987;72;617-9.
32. Rath W, Hackethal A, Bohlmann M.K. Second-line treatment of postpartum haemorrhage (PPH). Arch Gynecol Obstet. 2012; 286(3); 549-61.
33. Hebish G,Huch A.Vaginal uterine artery ligation avoids high bloodloss and puerperal hysterectomy in postpartum hemorrhage. Obstet Gynecol.2002;100:574-8.
34. Philippe H,Oreye D,Lewin D.Vaginal ligature of uterine arteries during postpartum hemorrhage.Int J gynecol Obstet 1997(56)267-70.
35. Bruinse H.W, Metz G.C.H, Kwee A. Surgical treatment of postpartum haemorrhage. Int Congr Series 2005; 1279; 369-75.
36. Clark S,Phelan J,Yeh S et al. Hypogastric artery ligation for obstetric hemorrhage.Obstet Gynecol.1985;66;353-56.
37. Clark S,Yen S,Phelan J et al. Emergency hysterectomy for obstetric hemorrhage.Obstet gynecol.1984;64;376- 81.
38. Rossi A.C, Lee R.L, Chmait R.H. Emergency postpartum hysterectomy for uncontrolled postpartum bleeding. A systematic review. Obstet Gynecol 2010; 115(3); 637-44.
39. RCOGs Green-top guideline no 52: prevention and management of PPH. May 2009, London UK
40. Georgiou C (2010) Intraluminal pressure readings during establisment of a positive tamponade test in the mangament of PPH. BJOG 117;295-299
41. Bakri YN et alUse of intrauterine balloonkatheters for control of uterne heamorrhage. www.uptodate.com 2011
42. Rath W et al secondline treatment of postpartum haemorrhage. Arch Gynecol Obstet (2012) 286;549-561
43. Laas E, Bui C et al. Trends in the rate of invasive procedures after the addition of the intrauterine tamponade test to a protocol for management of severe postpartum hemorrhage. AJOG. Oct. 2012; 281.e1-e7.
Arteriel embolisering og ballonokklusion
Perkutan arteriel embolisering er en veldokumenteret teknik til at stoppe blødning i forbindelse med f.eks. traumer, kirurgi og stråleskader på kar. Embolisering ved intraktabel postpartum blødning er første gang beskrevet i 1979 (1;2) og teknikken er nu vidt udbredt internationalt. Mulighederne for tilgang til interventionsradiologi varierer dog betydeligt. På centre hvor interventionsradiologi er til stede bør embolisering/ballonokklusion overvejes som et alternativ eller supplement i behandlingen af postpartum blødning.
NB: Interventionsradiologiske teknikker anvendt i forbindelse med behandling af kendt abnormally invasive placenta (AIP) behandles i afsnit 6 ” Fastsiddende placenta”, samt under ”Placenta prævia”.
Perkutan arteriel embolisering
Embolisering kan anvendes for at opnå hæmostase ved intraktabel postpartum blødning efter sectio eller vaginal fødsel. I nogle tilfælde kan det medføre at hysterektomi udgås. Patienten skal dog være cirkulatorisk stabil nok til at tåle en overflytning/transport til interventionsradiologisk stue eller hybridstue med røntgengennemlysning. Alternativt kan patienten stabiliseres temporært med en ballonokklusion af aorta (3-5).
Et studie fra 2011 af Ganguli et al inkluderede 66 kvinder der blev emboliseret pga. postpartum blødning (6). De rapporterede en klinisk succesrate på 98 % for primær postpartum blødning, 88 % for sekundær og 94 % for blødning associeret med sectio. Et andet studie fra 2012 af Poujade et al inkluderede 98 kvinder der blev emboliseret pga. postpartum blødning og her var den samlede kliniske succesrate 91,8 % (7). Det konkluderes desuden at abnormally invasive placenta er associeret med manglende effekt af embolisering. I et tredje studie fra 2009 af Kirby et al indgik 43 kvinder der blev emboliseret pga. postpartum blødning og desuden et review af litteraturen der i alt omfattede ca. 430 kvinder (8). Samlet for disse studier ligger den kliniske succesrate på 71,5 % til 100 % (median 96,3 %) afhængigt af kriterierne for klinisk succes og populationen.
Der beskrives en komplikationsrate på 1,5-7 % for embolisering (6;8;9). De fleste komplikationer er dog ikke direkte procedurerelaterede og kunne også skyldes den massive blødning eller være opstået i forbindelse med kirurgiske indgreb (6;8;9). Iskæmiske komplikationer er meget sjældne og risikoen minimeres ved brug af optimal størrelse af okklusionsmateriale (6;8;9).
Der er kun begrænsede data i litteraturen m.h.t. fremtidig fertilitet efter embolisering i forbindelse med postpartum blødning. Et review fra 2009 af Delotte et al omfatter followup vedr. fertilitet for 168 kvinder (10). Der beskrives 45 efterfølgende graviditeter, hvoraf 8 (18 %) resulterede i spontan abort.
Perkutan arteriel ballonokklusion
I tilfælde af ukontrollabel livstruende blødning trods kompression, tamponade, uterotonica, kompressionssuturer og evt. ligering kan en temporær arteriel okklusionsballon anlægges i aorta uden brug af røntengennemlysning for at opnå stabilisering. Den midlertidige stabilisering kan give mulighed for at opnå permanent hæmostase kirurgisk eller at planlægge f.eks. embolisering (3;4). Der er desuden beskrevet spontan hæmostase efter midlertidig okklusion af aorta (3;4).
Teknik
I lokalanæstesi indføres et kateter i a. femoralis com., hvorfra det/de blødende kar kateteriseres selektivt og emboliseres under røntgengennemlysning. Ved samme teknik kan en okklusionsballon placeres temporært i aorta – også uden brug af røntgengennemlysning på f.eks. sectiostuen.
Sammenfatning
Anvendelse af interventionsradiologiske teknikker i behandlingen af postpatum blødning har evidensgrad II-3 og rekommandationsgrad B. På centre hvor muligheden for interventionsradiologi er til stede kan ballonokklusion af aorta overvejes i behandlingen af fortsat ukontrollabel livstruende postpartum blødning trods kompression, tamponade, uterotonica, kompressionssuturer og evt. ligering. Embolisering kan overvejes hvis patienten er cirkulatorisk stabil nok til at tåle overflytning/transport til interventionsradiologisk stue eller 49 hybrid stue med røntgengennemlysning eller kan stabiliseres med en ballonokklusion af aorta. Begge teknikker kan anvendes ved både primær som sekundær postpartum blødning og efter såvel sectio som vaginal fødsel.
Referencer
1. Brown BJ, Heaston DK, Poulson AM, Gabert HA, Mineau DE, Miller FJ, Jr. Uncontrollable postpartum bleeding: a new approach to hemostasis through angiographic arterial embolization. Obstet Gynecol 1979 Sep;54(3):361-5.
2. Heaston DK, Mineau DE, Brown BJ, Miller FJ, Jr. Transcatheter arterial embolization for control of persistent massive puerperal hemorrhage after bilateral surgical hypogastric artery ligation. AJR Am J Roentgenol 1979 Jul;133(1):152-4.
3. Martinelli T, Thony F, Declety P, Sengel C, Broux C, Tonetti J, et al. Intra-aortic balloon occlusion to salvage patients with life-threatening hemorrhagic shocks from pelvic fractures. J Trauma 2010 Apr;68(4):942-8.
4. Sovik E, Stokkeland P, Storm BS, Asheim P, Bolas O. The use of aortic occlusion balloon catheter without fluoroscopy for life-threatening post-partum haemorrhage. Acta Anaesthesiol Scand 2012 Mar;56(3):388-93.
5. Leonhardt H, Liedman B, Wingren U, Lonn L. [Endovascular treatment in massive uncontrolled intestinal hemorrhage. Stabilization with aortic balloon allows time for angiographic survey]. Lakartidningen 2005 Apr 25;102(17):1326-30.
6. Ganguli S, Stecker MS, Pyne D, Baum RA, Fan CM. Uterine artery embolization in the treatment of postpartum uterine hemorrhage. J Vasc Interv Radiol 2011 Feb;22(2):169-76.
7. Poujade O, Zappa M, Letendre I, Ceccaldi PF, Vilgrain V, Luton D. Predictive factors for failure of pelvic arterial embolization for postpartum hemorrhage. Int J Gynaecol Obstet 2012 May;117(2):119-23.
8. Kirby JM, Kachura JR, Rajan DK, Sniderman KW, Simons ME, Windrim RC, et al. Arterial embolization for primary postpartum hemorrhage. J Vasc Interv Radiol 2009 Aug;20(8):1036-45.
9. Ratnam LA, Gibson M, Sandhu C, Torrie P, Chandraharan E, Belli AM. Transcatheter pelvic arterial embolisation for control of obstetric and gynaecological haemorrhage. J Obstet Gynaecol 2008 Aug;28(6):573-9.
10. Delotte J, Novellas S, Koh C, Bongain A, Chevallier P. Obstetrical prognosis and pregnancy outcome following pelvic arterial embolisation for post-partum hemorrhage. Eur J Obstet Gynecol Reprod Biol 2009 Aug;145(2):129-32.
Inversio uteri
Den rapporterede hyppighed er 1:2000 fødsler.
Ses oftest ved uhensigtsmæssigt kraftigt træk på navlesnoren, atonisk uterus, mangegangsfødende og evt. ved pludseligt højt intraabdominalt tryk.
Symptomer og fund
Kraftig blødning, hæmodynamisk påvirket patient. Uterus ses uden for vagina eller der føles tomt over symfysen med samtidig udfyldning i vagina
Behandling
Der er enighed om vigtigheden af at uterus reponeres umiddelbart. Er placenta fastsiddende skal den fjernes før reponering, men først når der er etableret iv-adgang. Der kan med fordel gives ueterusrelakserende middel. Effektiv anvendelse af ritodrine, salbutamol, terbutalin, magnesium sulfat, halothan og glycerylnitrat er beskrevet (1-7)
Lykkes det ikke at reponere uterus manuelt kan det i ganske enkelte tilfælde være nødvendigt at foretage laparotomi med samtidig reponering af uterus nede- og oppefra. En evt. kontraktionsfure, som forhindrer reponering kan gennemskæres posteriort.
Når uterus er reponeret afbrydes indgiften af uterusrelakserende middel umiddelbart og der gives uterotonika
. Umiddelbar reponering af uterus evt. efter indgift af glycerylnitrat er beskrevet i flere studier (4-7). Altabef (4) beskriver i 1992 et tilfælde af fastsiddende placenta med inversio og total prolaps af uterus. Denne reponeres let efter 2 x 0.05mg nitroglycerin uden bivirkninger for moderen. Senere har Bayhi (6) og Dayan (7) beskrevet lignende succes i forbindelse med inversio.
Anvendelse af nitroglycerin i obstetrikken er ligeledes beskrevet i forbindelse med fastsiddende placenta, fastsiddende sidstkommende hoved samt vending og fremtrækning på fod.
Alle meddelelser er dog kasuistiske eller mindre retro- eller prospektive serier. Der foreligger ingen case-controlstudier eller studier som randomiserer mellem forskellige uterolytica.
Glycerylnitrat (Nitroglycerin) virker relaxerende på glatmuskulatur. Kan indgives intravenøst, sublingualt eller som mundspray. Virkningen indsætter ved inden for 0,5-1,5 minutter. Plasmahalveringstiden er 2 min og virkningsvarigheden ca 10 min. Da glycerylnitrat samtidig virker kardilaterende kan det medføre blodtryksfald og bør derfor anvendes med forsigtighed til potentielt hypovolæme patienter (Obs: ptt med stor blødning og præeclamptikere). Virkningen er understøttet af et svensk in vitro-studie som påviste en dosisafhængig hæmning af såvel spontan som oxytocininduceret myometrieaktivitet. I et tilknyttet in vivo studie fandtes maximal relaxation af uterus efter 0,1 – 0,2 mg (8) Peng anvendte 0,5 mg som iv bolus i en serie på 15 patienter med fastsiddende placenta. Placenta kunne i alle tilfælde fjernes, men der registreredes samtidig signifikante, ej klinisk betydende, blodtrykfald (9). DeSimone anvendte kun 0,05 mg i en serie på 6 ptt. Med fastsiddende placenta. Denne dosis måtte i et tilfælde gentages for at opnå effekt, hvorfor de i en større serie anvendte 0,1mg med succes i alle tilfælde. Ingen bivirkninger blev registreret (10)
Fordelen ved glycerylnitrat i forhold til de øvrige uterolytica er således den umiddelbart indsættende virkning, meget korte virkningsvarighed samt fravær af klinisk betydende bivirkninger ved de undersøgte doseringer.
Virkningen på uterinmuskulaturen ved sublingual indgift eller mundspray er ikke beskrevet.
Selvom nitroglycerin i vid udstrækning har erstattet det afregistrerede amylnitrit, ved behov for hurtigt indsættende uterusrelaxation er stoffet endnu ikke registreret til dette brug i DK
Sammenfatning
De publicerede serier tyder på at nitroglycerin indgivet iv i doser på 0,1- 0,2 mg er effektivt og stort set bivirkningsfrit til akut afslapning af uterusmuskulaturen og dermed mulighed for reponering af inverteret uterus. Studierne er dog få og små og ukontrollerede.
Ved inversio uteri skal uterus reponeres umiddelbart efter indgift af uterolyticum, f.eks glycerylnitrat iv 0.1 mg. Dette kan gentages hvis ingen effekt efter 1.5 minutter. Ved manglende iv adgang, evt sublingualt 0.25 –0.5 mg indtil dette er etableret. Obs hypotension ved stor blødning, ellers ingen øvre dosisgrænse. Kan uterus ikke umiddelbart reponeres skal pt i UA. Samtidig stabilisering og observation af patienten som angivet tidligere i guideline. I tilfælde hvor manuel reponering er umulig gøres laparotomi. Efter reponering indgives uterotonica.
Referencer
1. Catanzarite VA, Moffitt KD, Baker ML et al. New approaches to the management of acute puerperal uterine inversion.Obstet Gynecol. 1986; 68(3 Suppl):7S-10S.
2. Kovacs BW, DeVore GR. Management of acute and subacute puerperal uterine inversion with terbutaline sulfate. Am J Obstet Gynecol. 1984 15;150(6):784-6.
3. Thiery M, Delbeke L. Acute puerperal uterine inversion: two-step management with a beta-mimetic and a prostaglandin. Am J Obstet Gynecol 1985;153(8):891-2
4. Altabef KM, Spencer JT, Zingberg S. Intravenous nitroglycerin for uterine relaxation of an inverted uterus. Am J Obstet Gynecol 1992; 166: 1237-8
5. Dufour P, Vinatier D, Puech F. The use of intravenous nitroglycerin for cerviko-uterine relaxation: a review of the literature. Arch Gynecol Obstet 1997; 261: 1-7
6. Bayhi DA, Sherwood CD, Campbell CE. Intravenous nitroglycerin for uterine inversion. J Clin Anaesth. 1992; 4: 487-8
7. Dayan SS, Schwalbe SS. The use of snall dose nitroglycerin in a case of uterine inversion. Anest Analg 1992; 82: 1091-3
8. Axemo P, Fu Xin, Lindberg B et al. Intravenous nitroglycerin for rapid uterine relaxation. Acta Obstet Gynecol Scand 1998; 77: 50-53
9. Peng ATC, Gorman RS, Shulman SM et al. Intravenous nitroglycerine for uterine relaxation in the postpartum patient with retained placenta. Anesthesiology 1989; 71: 172 – 3
10. DeSimone CA, Norris MC, Leighton BL. Intravenous nitroglycerine aids manual extraction of the retained placenta. Anesthesiology 1990; 73: 787
Læsioner i fødselsvejene
Hæmatomer
Litteraturen er sparsom og af ældre dato. Patientmaterialerne er gennemgående små og studierne deskriptive. Der findes ingen studier som randomiserer til forskellige typer af håndtering
Klassifikation
1. Vulvahæmatomer.
Lokaliseret under m.levator ani. Begrænses oftest i deres udbredning af diaphragma urogenitale og den anorectale fascie. Posteriore hæmatomer kan dog i sjældne tilfælde dissekere sig ned i fossa ischiorectale og opnå en anselig størrelse.
2. Paravaginale hæmatomer
Lokaliserede over m levator ani, men under de kardinale ligamenter. Symptomer er smerter, trykken mod endetarmen og evt blæreretention og dislokation af uterus. Erkendes oftest først ved vaginal inspektion/eksploration.
3. Supravaginale hæmatomer
Over de kardinale ligamenter. Udbreder sig retroperitonealt. Opstår oftest efter uterine eller høje cervixlæsioner. Udbreder sig retroperitonealt og kan give anledning til abdominal katastrofe og cirkulatorisk svært påvirket patient. Kan evt erkendes ultrasonisk, men oftest vil klinikken være afgørende.
Forekomst og risikofaktorer
Den angivne hyppighed af paravaginale hæmatomer varierer betydeligt, men ligger samlet mellem 1:500 og 1:900 fødsler med sjældnere forekomst af større hæmatomer (1-4). For de supravaginale hæmatomers vedkommende er der beskrevet forekomster på 1: 3500(1) til 1:20.000(2). Vigtigste risikofaktor er instrumentelle vaginale forløsninger, desuden er der fundet en korrelation til forekomst af bristninger i perineum og vagina samt til episiotomi, med samtidig episiotomi i 87- 93% af hæmatomerne (1,2,5). Sheik fandt ved gennemgang af 40 tilfælde af interventionskrævende paravaginale hæmatomer at 75% af disse opstod hos førstegangsfødende og at 85% havde episiotomi eller bristning af perineum. I 90% af tilfældene sad hæmatomet i samme side som episiotomien/bristningen. Fliegner gennemgik 39 tilfælde af supravaginale hæmatomer. De fordelte sig på ca 1/3 efter vaginal fødsel, 1/3 efter forceps og 1/3 efter sectio. I 28 af tilfældene konstateredes en høj collumrift, denne var i 11 tilfælde ikke erkendt ved vaginal inspektion.
Gennemgående for de refererede studier er at de er af ældre dato, at der er anvendt forceps og ikkecup ved instrumentel forløsning og at de udgår fra populationer med høj episiotomirate.
Håndtering
Vulvahæmatomer
Ved hæmatom <5cm: Enighed i litteraturen om at disse kan observeres mht yderligere udbredning. Evt anvendes ispose eller kompression (4,5).
Ved hæmatom >5cm eller hastigt tiltagende størrelse: Litteraturen anbefaler gennemgående kirurgisk intervention: Åbning af hæmatomet, gennemstikning af eventuelle synligt blødende kar, drænage og kompression samt antibiotikaprofylakse(2,3,6). Den sparsomme litteratur er dog ikke entydig. Zahn konkluderer på baggrund af eget materiale på 11 vulvahæmatomer og den fundne litteratur at der formentlig er færre komplikationer efter kirurgisk intervention kombineret med antibiotika end ved konservativ håndtering (5).
Paravaginale hæmatomer
Ved små hæmatomer under 5 cm anbefales oftest observation (4,5).
Ved større hæmatomer anbefales i litteraturen åbning og evakuering af hæmatomet (2,3,6) Synlige kar gennemstikkes, mens ”blind” oversyning næppe har nogen mening. Det er omdiskuteret om hæmatomcaviteten skal lukkes og om der i alle tilfælde skal anlægges dræn. I de fleste tilfælde anbefales tamponade af vagina. Benrubi sammenlignede 19 patienter som behandledes konservativt med 10 kirurgisk og finder bedre resultater i den sidste gruppe (ingen komplikationer og kortere indlæggelsestid). Komplikationer til konservativ behandling sås ved hæmatomer >15cm i diameter. Drænage og kompression er beskrevet i et dansk studie fra 2000 (7): I to tilfælde af intraktable paravaginale hæmatomer anlagdes efter rømning af hæmatomerne dræn i hæmatomet, hvorefter vagina udtamponeredes med en blodtrykmanchet suffleret til lige over patientens systoliske BT og placeret i en steril handske. Luften kunne i det efterfølgnde døgn exuffleres gradvist under observation og i begge tilfælde havde patienten ikke yderligere blødning efter fjernelse af manchetten.
Et nyligt studie har vist at Bakri ballon tidligt i forløbet en plads i behandlingen af paravaginale hæmatomer, hvis der ikke med anden standard beh. kan opnås hæmostase, dette også gerne tidligt i forløbet, for at forebygge svær post partum blødning (11).
Et mindre studie har også vist, at man ved angiografisk embolisering kan opnå kontrol over blødningen, hvorefter suturering blev mulig. Dette kun ved cirkulatorisk stabil patient. Det er ikke udbredt til akut brug på mange sygehuse, men spændende resultater (12).
Supravaginale hæmatomer:
Ca halvdelen af supravaginale hæmatomer konstatereres umiddelbart, den anden halvdel først efter 24 timer (3). Symptomer er nedre abdominalsmerter, dislokation af uterus, urinretention, cirkulatorisk påvirkning og evt blødningsshock.
Det er omdiskuteret om supravaginale hæmatomer skal håndteres konservativt eller kirurgisk. Der er dog enighed om at akut laparotomi med opsøgning af blødningskilde efterfulgt af relevant kirurgisk intervention er påkrævet, såfremt hæmatomets omfang påvirker patienten cirkulatorisk (1). Timingen kan naturligvis være vanskelig. Intervention vil oftest bestå i kompression og evt ligering af relevante kar (se relev afsnit). Fliegner behandlede 26 ud af 39 konservativt med og opsummerer 48 patienter beskrevet i litteraturen (i nyere tid), heraf kunne 40 (83%) behandles konservativt (1,2,8) Som alternativ til kirurgisk intervention er kombineret pakning af uterus og vagina beskrevet (se afsn).
Angiografisk embolisering er beskrevet i flere studier og kan have en plads ved større hæmatomer, primært retroperitoneale hæmatomer med vedvarende intraktabel blødning hos en i øvrigt cirkulatorisk stabil patient. Resultaterne er lovende, men metoden er endnu ikke udbredt og slet ikke organiseret til akut brug (se relevant afsnit).
Collumrifter
Et nyligt studie har vist, at cerclage udgør en risikofaktor for collumrifter hos både primi- og multipara (9)
Derudover er der ikke meget tilgængelig litteratur om emnet.
Anbefaling: Kun blødende collumrifter sutureres. Ikke blødende rifter lades urørte. Går riften meget højt op er der risiko for involvering af den descenderende gren af a. uterina, og pt skal observeres tæt for evt udvikling af retroperitonealt hæmatom (3,10)
Syntese
Bløder en kvinde efter placentas fødsel udtamponeres vagina, mens indledende manøvrer udføres.
Når patienten er stabiliseret, når der er tilkaldt hjælp og relevante remedier er på stuen eller patienten er overflyttet til operationsstue/bedøvet, foretages inspektion af vulva og vagina. God oversigt, assistance og nødvendige remedier er essentielt. Er der ikke optimal oversigt, eller er der mistanke om større læsioner, bør patienten bedøves.
1. Ved hæmatom < 5 cm i diameter: som hovedregel observation
2. Ved hæmatom >5 cm:
- Vulvahæmatom: Rømning af hæmatomet, evt dræn, gennemstikning af synligt blødende kar, evt oversyning, kompression, antibiotika.
- Paravaginalt hæmatom: Rømning, gennemstikning af synligt blødende kar, evt drænage, kompression i ca. 24 timer med gaze, blodtryksmanchet eller ballon. Antibiotika.
- Supravaginalt hæmatom: Observation kan overvejes hos cirkulatorisk stabil patient. Ved begyndende cirkulatorisk instabilitet: akut laparotomi med relevant kirurgisk intervention: trinvis ligering af kar, hysterectomi, abdominal tamponade eller evt angiografisk embolisering. I alle tilfælde kombineret med stabilisering af patienten cirkulatorisk og koagulationsmæssigt (se afsn).
3. Kun blødende collumrifter sutureres. Obs udvikling af retroperitonealt hæmatom.
Referencer
1. Fliegner JRH. Postpartum Broad Ligament hematomas. J Obstet Gynecol. Br Commenwealth 1971; 78:184.
2. Sheik GN. Perinatal Genital Hematomas. Obstet Gynecol 1971; 38: 571-5.
3. Hankins GDV, Zahn CM. Pueperal hematomas and lower genital tract lacerations. In: Hankins GDV et al. Operative Obstetrics. Conneticut: Appleton & Lange, 1995: 257-72.
4. Ridgway LE. Pueperal Emergency Vginal and Vulvar hematomas. Obstet Gynecol Clin North Am 1995; 22(2): 275-82.
5. Zahn C, Hankins GDV, Yeomas ER. Vulvovaginal Hematomas Complicating Delivery. J Reprod Med 1996; 41: 569-574.
6. Benrubi G, Neuman C, Nuss RC, Thompson RJ. Vulvar and vaginal hematomas: A retrospective study of conservtive versus operative management.
7. Pinborg A, Bødker B, Høgsall C: Postpartum hematoma and vaginal packing with a blood pressure cuff. Acta Obstet Gynecol Scand 2000; 79: 887-889.
8. McElin TW, Bowers VM. Pueperal hematomas. Am J Obstet Gynecol 1954; 67:356
9. Landy HJ et al. Consortium of safe labour. Characteristics associated with severe perineal and cervical lacerations during vaginal delivery. Obstet Gynecol 2011;117(3):627-35.
10. Williams Obstetrics 20th edition. Cunningham, Macdonald, Gant.
11. Maiju Grønvall et all: Use of bakri balloon tampomade in the treatment of postpartum hemorrhage: a series of 50 cases from tertiary teaching hospital. Acta Obstet Gynecol Scand. 2012;91
12. Yann fargeadou et al: Severe primary postpartum hemorrhage due to genital tract laceration after operative vaginal dilevery: successful treatment with transcatheter arterial embolization. Eur Radiol (2009) 19:2197- 2203
Håndtering af blodtab og koagulation
Baggrund
Under graviditeten øges blodvolumen med 45-55 % sv.t. ca. 1-1,5 L, primært ved en øgning i plasmavolumen. Erytrocytter øges kun 20 %, hvilket bevirker en fysiologisk anæmi (hæmatokrit falder).
Pga. den gravides fysiologisk betinget hypervolæmi, kan den fødende tåle et blodtab på 1 l uden nogen nævneværdig påvirkning af blodtryk, hæmatokrit eller hjertefrekvens. Normalt blodtab ved vaginal fødsel er 500 ml, og ved sectio op til 1000 ml. Blodtab over 1000 ml kan hurtigt udvikle sig medfører en tilstand der truer patienter og det har højeste prioritet at stoppe blødningen, blodtab over 2000 ml er yderst truende for patient og livstruende blødning kan udvikle sig løbende. De fysiologiske ændringer der sker under graviditeten med bloodflow til uterus og placenta på ca. 600 ml/min ved terminen, bevirker at der er risiko for nedblødning af den fødende i løbet af ganske kort tid når de normale mekanismer til hæmning af blødningen postpartum ikke fungerer. (1)
Definition
Blødning efter fødsel (PPH = postpartum hemorrhage), er normalt defineret som estimeret blodtab > 500 ml i de første 24 timer efter fødslen. Men da de fleste har et blodtab på ca. 500 ml i forbindelse med fødsel, og blodtab på op til 1000 ml generelt tolereres uden ændringer i blodtryk eller CO, er det mere relevant at bruge svær PPB (sPPH) som defineres ved blødning over 1000 ml, uafhængig af fødselsmåden. Ved at anvende denne definition vil 1-2 % af alle fødsler blive kompliceret af PPH.
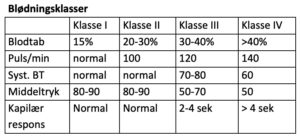
Blodtab kan beskrives i klasserne I-IV ud fra ovenstående, selvom det oftest ikke er så klassisk som opstillet her. Blødning > 40 % er livstruende hvis volumen ikke erstattes og medfører altid blodtransfusion. Blodtransfusion er ofte nødvendig ved 30-40% blodtab, og sjældent nødvendigt ved blødning < 30% i forbindelse med PPH. Patientens vitale parametre kan følges ved skift fra klasse til klasse, således bør en tiltagende takykardi med øgning af puls fra 120/min til 140/min rejse mistanke om livstruende blødning > 40% og behandling iværksættes eller intensiveres for at stoppe blødningen samtidigt med symptomatisk behandling med volumen i form af fx blodtransfusion overvejes.
Behandling
Væsketerapi
Væsketerapi har det formål at normalisere blodvolumen i fasen hvor blødningen søges stoppet. Krystalloider (ringer laktat/NaCl) vælges primært til at erstatte den hypovolæme tilstand indtil hæmoglobinen falder til et niveau hvor erythrocyttransfusion overvejes. Krystalloider er nemt tilgængelige og bør vælges primært som erstatning givet faktor 2 i erstatning (blødning 500 ml erstattes med 1000 ml NaCl). Syntetiske kolloider (fx Voluven, Macrodex etc) er ofte anvendt og fortynder blodbanen ligesom krystalloider, men i tillæg til dette påvirkes hæmostasen i negativ retning (koagulopati) via påvirkning af trombocytterne og fibrin dannelsen, og dette medfører øget blødning og transfusionsbehov. Flere studier i generel kirurgi, traume og svært sepsis m.v. har vist denne koagulopati, og i svær sepsis/septisk shock er det endda forbundet med øget dødelighed at bruge Voluven (2, 3). Ydermere findes der ikke evidens for en bedre volumeneffekt af syntetiske kolloider sammenlignet med krystalloider (2), og samlet set anbefales disse ikke til blødende patienter med behov for normal hæmostase – og især PPH patienten er meget afhængig af normal hæmostase.
Blodkomponenterapi
Følger altid Sundhedstyrelsen (4) og blodbankernes gældende vejledninger, men princippet er restriktiv anvendelse af blodkomponenter for at minimere patientens udsættelse for allogene blodkomponenter (fra andre mennesker) pga. de mange specifikke og uspecifikke bivirkninger. Post partum patienten tåler pga. den fysiologiske hypervolæmi anæmi bedre end andre patienter. I de tilfælde hvor livstruende blødning (præget af kredsløbssvigt) udvikles gælder dog et pro-aktivt princip med erstatning af det tabte med balanceret blodkomponentterapi (SAG-M, FFP og trombocytter) for at opretholde normal oxygenering og hæmostase da dette har vist at forbedre overlevelsen for massive blødninger (5).
Livstruende blødning:
1. SAG M gives sammen med FFP og trombocytter i ratio 3 SAG-M : 3 FFP : 1 Trombocytkoncentrat (3:3:1 princippet) fra den tidligste fase og indtil blødningskontrol. Således opsættes 1 FFP når første SAG-M sættes op, og efter 3 sæt SAG-M/FFP opsættes 1 trombocytkoncentrat. I ventetiden på blodprodukter kan gives krystalloider.
Kontrollabel blødning (pågående):
Behandling med Erytrocytsuspension (SAG-M):
1. Hb < 6.0 mmol/l og samtidig:
1.1. Svær hjertesygdom
1.2. Septisk shock (i den initiale fase, < 6 timer)
1.3. Akut, alvorlig blødning (fx tab > 30% af blodvolumen indenfor 24 timer)
2. Alle øvrige patienter overvejes behandling med SAG-M ved Hb < 4.5 mmol/l
Behandling med FFP overvejes (kontrollabel pågående blødning)
1. I henhold til svar på
1.1. TEG/ROTEM, se afsnit nedenfor
1.2. INR > cirka 2: dosis 20 ml/kg kropsvægt
1.3. Aktiveret Partiel Tromboplastintid (APTT) > 45 sekunder: dosis 20 ml/kg kropsvægt
1.4. Fibrinogen < 3 µmol/l (1 g/l): dosis 20 ml/kg kropsvægt
2. Efter 6. SAGM gives SAGM og FFP i forholdet 1:1
Behandling med trombocytkoncentrat overvejes (kontrollabel pågående blødning)
1. I henhold til svar på
1.1. TEG/ROTEM, se afsnit nedenfor
1.2. Trombocyttal 60 mia/l: dosis 5 ml/kg kropsvægt
2. Efter 12 komponenter (SAGM + FFP) gives 1 TK og derefter gives SAGM og TK i forholdet 5:1
Hæmostasemonitorering
Hæmostasemonitorering foretages klassisk med trombocyttal, INR, APTT, P-Fibrinogen, Pantithrombin og evt. P-Fibrin D-dimer, og denne monitorering bør gøres hyppigt (3-4 / dag) i tilfælde hvis DIC mistænkes (1). Flere nationale/regionale og internationale vejledninger anbefaler at blodtransfusioner styres i henhold til resulteter af Thrombelastografi (TEG) eller Thrombelastometri (ROTEM) og ikke i henhold til den klassiske laboratorie værdier, hvilket også er valideret i PPH (6). TEG/ROTEM er to fabrikater af nær samme fuldblodsanalyse, der kan identificere forstyrrelser i de forskellige dele af den hæmostatiske proces og derved identificere forskellige årsager til koagulopatier (blødningsforstyrrelser). TEG er endda valideret i raske gravide helt indtil 8 uger postpartum. TEG/ROTEM bruges til blødende patienter, og udfra resultatet gives forslag til behandling med blodkomponenter og/eller hæmostatiske lægemidler med det mål at normalisere hæmostasen, begrænse blødningen og dermed reducere behovet for blodtransfusion. Anvendelse af TEG/ROTEM bør gøres i henhold til regionale vejledninger.
Koagulopatier (blødningsforstyrrelser)
Ved behandlingskrævende postpartum blødning kan det være svært at skelne om årsagen er kirurgisk eller medicinsk (koagulopati), og kirurgisk blødning kan hurtigt blive medicinsk pga. forbrug. Derfor er man nødt til, sideløbende med stabilisering af patienten og afklaring af blødningskilde, at vurdere koagulationsstatus ved hæmostasemonitorering og behandle derefter. En aktivering af koagulationssystemet bør overvejes senest når blødningen bliver transfusionskrævende. Hyperfibrinolyse med faldende fibrinogen ses hyppigt ved PPH og forbruget kan hurtigt udvikle sig en DIC-tilstand med mange abnorme blodprøvesvar og livstruende blødning (1, 6).
DIC kan udvikles i forlængelse af hyperfibrinolyse hos ptt med stort blodtab og trykfald, eller pt kan debutere med DIC, hvilket oftest ses hos risikopatienter med foetus mors, præeklampsi, amnionemboli eller abruptio. Mistanke om DIC eller svære koagulopatier bør medføre konference med regional blødnings- eller koagulations-ekspertise
Tranexamsyre
Tranexamsyre (TXA) er et antifibrinolytisk lægemiddel som hæmmer plasmin-medieret fibrinolyse og på denne baggrund fremmer blodet evne til at danne stabile koagler. De mest almindelige bivirkninger er diarré, kvalme og opkastning (1-10%). Herudover er kramper, hypotension, tromboemboli, anafylaksi og sysforstyrrelser anført af lægemiddelstyrelsen men med ukendt frekvens. I forhold til tromboembolisme bemærkes det at ingen af de større RCT’s eller systematiske reviews indenfor området finder øget risiko for tromboembolier ved TXA behandling (7-9). Prisen for 1 g TXA IV, som er den anbefalede standardbehandling ved generel fibrinolyse, er omkring 80 kr.
Aktuelt er der publiceret ét RCT studie, som undersøger TXA’s effekt som PPH-behandling ved vaginal fødsel (10). Her finder man at behandling af PPH (>800 ml) med TXA signifikant reducerer blodvolumen, tid til blødningsophør, hæmoglobinfald samt risiko for udvikling af svær PPH. Herudover er der publiceret en række RCT studier, som undersøger effekten af profylaktisk TXA ved forløsning. Tre af de omtalte studier vedrører vaginal forløsning, og overordnet finder studierne at TXA behandling signifikant reducerer det gennemsnitlige blodtab (11-13). To af studierne viser endvidere at TXA ligeledes reducerer forekomsten af større blodtab. I et Cochrane review fra 2015, omhandlende TXA som profylaktisk intervention mod PPH, fandt man lignende resultater med signifikant reduktion af henholdsvis det gennemsnitlige blodtab, blodtab >500 ml/ >1000 ml samt reduceret behov for blodtransfusioner (9).
Doseringen i de omtalte studierne ligger mellem 0,5-1 g IV op til 4 g IV efterfulgt af 1 g IV/time, men optimal dosering er uafklaret.
Ud over de nævnte studier pågår der aktuelt et stort internationalt studie, The WOMAN Trial, som inkluderer >20.000 kvinder med konstateret PPH radomiseret til 1 g TXA IV eller placebo (14). Resultaterne herfra forventes endeligt at afklare effekten af TXA som behandling ved PPH.
På nuværende tidspunkt må det ud fra den eksisterende litteratur konkluderes at TXA 1 g IV skal gives ved PPH – og dette tidligst muligt. Herudover understreges det at denne behandling bør gentages efter 30 min ved fortsat blødning, samt efter hver 10 blodprodukter ved fortsat livstruende blødning. Desuden bør TXA 1 g x 6 IV/PO overvejes indtil blødningskontrol (max 1 døgn).
Fibrinogen niveau og substituering
Et plasma fibrinogenniveau under 2 g/l (6 µmol/l) i den tidlige fase af PPH er associeret til svær PPH, og et kritisk lavt fibrinogen niveau kan skyldes resuscitations strategien med fortynding, brugen af kolloider (Voluven) eller en udviklet hyperfibrinolyse (11). Den kritiske grænse for fibrinogen er ikke kendt men ligger forventeligt et sted mellem 1-2 g/l (3-6 µmol/l).
Kritisk lavt fibrinogen niveau og samtidig pågående, alvorlig blødning kan erstattes med
1) FFP 20 ml/kg, eller
2) Kryopræcipitat poolet 5 ml/kg
3) Fibrinogen koncentrat 25 mg/kg
men evidensen for valg af behandling eller betydning for outcome er endnu ikke afklaret (15).
Rekombinant koagulationsfaktor VIIa (rFVIIa; NovoSeven)
rFVIIa er udviklet specielt til hæmofilipatienter og er beskrevet på et meget spinkelt grundlag at have gunstig effekt på PPH (talrige kasuistikker), men der foreligger ikke randomiserede studier der støtter brugen af rVIIa ved PPH (16). rVFIIa er ikke en erstatning for optimal balanceret blodkomponentterapi (efter 3:3:1 princippet, se ovenfor), optimal uterin kontrol eller optimale forsøg på at opnå kirurgisk/medicinsk hæmostase.
I særlige tilfælde hvor livstruende blødning består trods optimal medicinsk, uterin, transfusionsmedicinsk og kirurgiske forsøg på hæmostase kan rFVIIa overvejes: rFVIIa kan doseres 100 µg/kg IV bolus, men hvis kritiske niveauer af trombocytter og fibringen ikke kan udelukkes bør rFVIIa behandling forudgåes af 2 trombocytkoncentrater (10 ml/kg) og fibrinogen koncentrat 25 mg/kg for understøtte effekten.
Anvendelse af rFVIIa til livstruende PPH bør foretages i henhold til regionale vejledninger.
Referencer
1. Ahonen J, Stefanovic V, Lassila R. Management of post-partum haemorrhage. Acta Anaesthesiol Scand. 2010 Nov;54(10):1164-78.
2. Reinhart K, Perner A, Sprung CL et al. Consensus statement of the ESICM task force on colloid volume therapy in critically ill patients. Intensive Care Med (2012) 38:368–383.
3. Perner A, Haase N, Guttormsen AB et al. Hydroxyethyl starch 130/0.42 versus Ringer’s acetate in severe sepsis. N Engl J Med. 2012 Jul 12;367(2):124-34.
4. http://www.sst.dk/publ/publ2007/EFT/blodtransfusion/vejl_blodtransfusion.pdf.
5. Johansson PI, Stensballe J. Effect of Haemostatic Control Resuscitation on mortality in massively bleeding patients: a before and after study. Vox Sang. 2009 Feb;96(2):111-8.
6. Solomon C, Collis RE, Collins PW. Haemostatic monitoring during postpartum haemorrhage and implications for management. Br J Anaesth. 2012 Dec;109(6):851-63.
7. Shakur H, Roberts I, Bautista R, Caballero J, Coats T, Dewan Y, et al. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): a randomised, placebo-controlled trial. Lancet. 2010;376:23-32.
8. Henry DA, Carless PA, Moxey AJ, et al. Anti-fibrinolytic use for minimizing perioperative allogeneic blood transfusion. Cochrane Database Syst Rev. 2011 (3):Cd001886.
9. Novikova N, Hofmeyr GJ, Cluver C. Tranexamic acid for preventing postpartum haemorrhage. Cochrane Database Syst Rev. 2015 (6):CD007872.
10. Ducloy-Bouthors AS, Jude B, Duhamel A, et al. High-dose tranexamic acid reduces blood loss in postpartum haemorrhage. Critical Care 2011; 15: R117
11. Yang H, Zheng S, Shi C. Clinical study on the efficacy of tranexamic acid in reducing postpartum blood lose: a randomized, comparative, multicenter trial. Zhonghua Fu Chan Ke Za Zhi 2001;36:590-2.
12. Gungorduk K, Asıcıoğlu O, Yıldırım G, Ark C, Tekirdağ Aİ, Besımoglu B. Can intravenous injection of tranexamic acid be used in routine practice with active management of the third stage of labor in vaginal delivery? A randomized controlled study. Am J Perinatol 2013;30:407-13
13. Mirghafourvand M, Mohammad-Alizadeh S, Abbasalizadeh F, Shirdel M. The effect of prophylactic intravenous tranexamic acid on blood loss after vaginal delivery in women at low risk of postpartum haemorrhage: a double-blind randomised controlled trial.Aust N Z J Obstet Gynaecol. 2015 Feb;55(1):53-8
14. Shakur H, Elbourne D, Gulmezoglu M et al. The WOMAN Trial (World Maternal Antifibrinolytic Trial): tranexamic acid for the treatment of postpartum haemorrhage: an international randomised, double blind placebo controlled trial. Trials. 2010 Apr 16;11:40.
15. Wikkelsoe AJ, Afshari A, Stensballe J et al. The FIB-PPH trial: fibrinogen concentrate as initial treatment for postpartum haemorrhage: study protocol for a randomized controlled trial. Trials. 2012 Jul 17;13:110.
16. Ahonen J. The role of recombinant activated factor VII in obstetric hemorrhage. Curr Opin Anaesthesiol. 2012 Jun;25(3):309-14.
BILAG 1
SØGETERMER
Nedenstående MESH-termer er anvendt i litteratursøgning på PubMed der gav 238 hits. Ved gennemgang fandtes 6 relevante artikler for det specifikke PICO-spørgsmål (2 reviews 2,30 og 4 RCT 31-34). Endvidere fandtes 2 case series 35,36 og 3 case reports 37,39 som qua studiedesign og størrelse ikke er tillagt betydende evidens i udarbejdelsen af guideline. (“Oxytocin” OR “Oxytocics”) AND “Misoprostol” AND (“Postpartum Hemorrhage” OR “Uterine Inertia”)
BILAG 2
Forslag til patientinformation om profylakse
Om forebyggelse:
Alle kvinder bløder efter fødslen. Nogle bløder så meget, at de får blodmangel efter fødslen og i værste fald må have blodtransfusion. Jordemoderen kan vælge at hjælpe aktivt ved moderkagens fødsel (aktiv metode) eller at lade moderkagen fødes af sig selv (fysiologisk metode).
Aktiv metode:
Man kan nedsætte risikoen for blødning ved at give en sprøjte med medicin, der hjælper livmoderen med at trække sig sammen, og derefter sørge for, at moderkagen fødes hurtigt efter barnet. Denne metode er kun forbundet med få gener, men kan føre til efterveer. Du kan få smertelindrende medicin, hvis du ønsker det. Behandlingen indebærer ingen risiko for barnet og har ingen betydning for amningen.
Fysiologisk metode:
Når moderkagen fødes, skal livmoderen trække sig sammen, ellers vil kvinden miste blod. Livmoderen trækker sig sammen af sig selv ved de fleste normale fødsler. Hvis du er rask og normalvægtig og føder normalt, vil det være forsvarligt at lade moderkagen fødes af sig selv.
Om risikogrupper:
Nogle kvinder har større risiko for at miste blod efter fødslen end andre. Hos disse vil det være særligt relevant, at vi anvender den aktive metode ved moderkagens fødsel, fordi (specificer risikogruppe).
Hvis kvinden trods information ikke ønsker profylakse:
Notat i journal: Frabeder sig blødningsprofylakse trods relevant information om fordele og ulemper ved aktiv håndtering af efterbyrdsperioden.
