Hypernatriæmi hos kritisk syge
Natriumfolderen er en kort vejledning vedhæftet som pdf
Udarbejdet af arbejdsgruppe under DASAIM
Godkendt af DASAIM: 19. februar 2024
Gyldig fra: 19. februar 2024
Revision senest: 2028
Tovholder/Korrespondance:
Christian Overgaard Steensen (Region Hovedstaden) E-mail: christian.overgaard.steensen@regionh.dk
Arbejdsgruppe/Referenter:
Jens Michelsen (Region Syd), Frank Hansen (Region Syd), Zahida Ali (Region Nord), Henrik Gammelager (Region Midt), Masja Bluhme Hoe (Region Midt), Helle Scharling Pedersen (Region Sjælland), Christoffer Grant Sølling (Region Midt), Ulrikka Nygaard (Region Hovedstaden, Dansk Pædiatrisk Selskab), Christian Trolle (Region Midt, Dansk Endokrinologisk Selskab).
Interessekonflikter: Ingen i gruppen har meldt om interessekonflikter.
Indledning
Hypernatriæmi er hyppig ved ankomst til intensiv men induceres også hyppigt under indlæggelse.1-7 Hypernatriæmi hos kritisk syge er associeret med øget mortalitet i observationelle studier.1-7 Plasma natrium koncentrationen (PNa) er afgørende for toniciteten og dermed cellestørrelsen og det intracellulære miljø. Derfor kan hypernatriæmi – øgning af PNa – i sig selv forårsage cerebral dysfunktion og osmostisk demyelinisering med hjerneskade og død.8 Samtidig er der ved PNa> 147 mmol/l maksimalt tørststimulus, som kan være svært ubehageligt og forårsage til uro/delir.9
Hos raske børn og voksne reguleres PNa nøje mellem 137-144 mmol/l, bl.a. ved tørst, ikke-tørst, kvalme, indtagelse af vand og renal regulation. De normale regulationsmekanismer er ofte kompromitterede hos den kritisk syge (f.eks. cerebral påvirkning, nyresvigt, diuretikabehandling) kombineret med at væsken gives iv/sonde og dermed by-passer normal tørst/kvalme regulation. Derfor er det behandlernes ansvar at patienten som udgangspunkt ikke påføres hypernatriæmi medmindre det er en del af behandlingsplanen (f.eks. ved forhøjet intrakranielt tryk [ICP]).7 Det kræver viden om hvad der bestemmer PNa og rationel behandling med væske og diuretika. Til gengæld kan opmærksomhed på PNa sammen med vægtændringer kvalificerer væskeplanen. Hypernatriæmi inddeles praktisk i tilstande med dehydrering (vandmangel) og tilstande med salt og vandoverskud. Der kan være overlap mellem de to tilstande.
Ændringer siden 2020-udgave:
- Anvendelse af 5-10/ml/kg/time vand/5 % glukose til ønsket PNa ved dehydrering
- Mere liberal reduktion af PNa, hvis patienten ikke falder i bevidsthedsniveau
- Vægtændringer understreget til adskillelse af dehydrering/saltoverskud og forebyggelse af iatrogen dehydrering
- Algoritme ved svær saltforgiftning
- Oversigt over hyppigt anvendte iv-væskers indikation, indhold og effekt på PNa
Forkortelser
CDI Central Diabetes Insipidus
CRRT Continuous Renal Replacement Therapy
ECV Ekstracellulær Volumen
EFWC Elektrolytfri Vandclearance
ICP Intracranial Pressure
ICV Intracellulær Volumen
NDI Nefrogen Diabetes Insipidus
PNa Plasma natriumkoncentrationen
PNakorrigeret Plasma natriumkoncentrationen korrigeret for hyperglykæmi
RVI Regulatory Volume Increase
UK Urin kaliumkoncentrationen
UNa Urin natriumkoncentrationen
PNa, tonicitet, hyperglykæmi og elektrolytfri vandclearance
Natrium er den kvantitativt vigtigste osmolyt i extracellulær volumenet (ECV) og kalium i intracellulærvolumenet (ICV). Natrium og kalium bevæger sig ikke frit over cellemembranen i modsætning til vand. Derfor bestemmes PNa af forholdet mellem kroppens mængde af frit natrium, kalium og vand:10 11

Dvs. PNa ændres af ændringer i natrium-, kalium- og vandbalancerne. Natrium- og kaliumbalancerne estimeres som forskellen mellem input og output. Vandbalancen estimeres bedst ved vejning og se ændring fra udgangsvægt (indlæggelse/oplyst) og dag til dag ændringer.
PNa ændres fra PNa1 til PNa2 ved ændring i vandbalancen (∆TBW), ændringer i natrium- og kaliumbalancen (∆(Na+ + K+)) og ved estimeret total kropsvand (TBW), hvor TBWkvinder~kropsvægt x 0.5 og TBWmænd~kropsvægt x 0.6:8
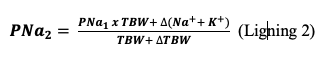
PNakorrigeret= PNamålt + 0,4 x (Blodsukker – 5 mmol/l)
PNa udtrykker toniciteten i plasma og dermed fordelingen af vand mellem ECV og ICV: Ved fald i PNa svulmer cellerne op; omvendt skrumper cellerne ved stigning i PNa.8 En vigtig undtagelse er ved hyperglykæmi (eller andre tilstande med osmotisk aktive partikler i ECV, f.eks. mannitol). De osmotisk aktive glukosemolekyler flytter vand fra cellerne til ECV. Derfor skal den målte PNa korrigeres for det øgede blodsukker (> 12 mmol/l) for at udtrykke toniciteten:12
PNamålt + 0,4 x (Blodsukker – 5 mmol/l) = PNakorrigeret
PNa reguleres tæt hos den raske. Vandinput reguleres af tørst og kvalme. Udskillelsen af natrium, kalium og vand reguleres renalt. Urinens bidrag til ændringer i PNa bestemmes ud fra elektrolytfri vandclearance (EFWC), hvor UK og UNa er kalium- og natriumkoncentrationen i urinen:11

Urinens bidrag til PNa ændringer kan praktisk bestemmes som størrelsen på diureserne og spot urin Na (UNa) og K (UK):
Ved UNa + UK > PNa bidrager urinen til et fald i PNa
Ved UNa + UK < PNa bidrager urinen til en stigning i PNa
EFWC kan også appliceres på andre væsker, men for praktiske formål er væsketab udover urin, altid med UNa + UK < PNa, hvilket vil sige at vandtab overstiger salttab og derfor alt andet lige vil bidrage til øgning i PNa.
Fritvandsclearance FWC = urinvolumen x ![]() , kan ikke anvendes, da
, kan ikke anvendes, da
osmolalitetsbestemmelsen inkluderer karbamid.8 Karbamid passerer cellemembranen – er en ineffektiv osmolyt – og bidrager derfor ikke kvantitativt til PNa.11 Bidraget ved osmotisk karbamid diurese (hyperalimination) er inkluderet i EFWC.
Ved måling af PNa skal som udgangspunkt anvendes samme metode, da der kan være forskel på PNa (2-4 mmol/l) ved bestemmelse på blodgasanalyseapparat og på klinisk biokemisk afdeling.13
Hypernatriæmi forårsaget af dehydrering – vandmangel
Generelt
Hypernatriæmi ved ankomst til hospitalet skyldes oftest dehydrering pga. manglende erstatning af vandtab. Dette ses hyppigst hos små børn, ældre, mennesker med manglende evne til at udtrykke tørst og/eller skaffe sig vand, og ekstremsportsudøvere. Dehydrering kan også opstå under indlæggelse pga. utilstrækkelig vandindgift. Dette kan være uintenderet pga. manglende opmærksomhed eller som led i afvanding ved f.eks. svært hypoxisk svigt. Ved intederet dehydrering ved f.eks. hypoxisk respirationssvigt afbalanceres fordele ved dehydrering overfor risikoen for hypovolæmi, nyreskade, svær tørst/delir. Dehydrering adskilles fra hypernatriæmi med salt og vandoverskud ved vægttab og negativ væskebalance.8
Ved dehydrering med betydende hypovolæmi (kliniske tegn: hypotension, takykardi, øget kapillærresponstid og kølige ekstremiteter) øges ECV med natriumholdige væsker (eks. bolus Ringer-laktat/0,9 % NaCl) til stabilisering af hæmodynamik (Se Tabel 3 hyppigt anvendte iv væsker).14
Ved dehydrering uden betydende hypovolæmi (evt. efter patienten er stabiliseret med natriumholdige væsker) korrigeres vandmanglen med hypotone væsker. Førstevalg er vand p.o./sonde 5-10 ml/kg/time til ønsket PNa. Ved intraktable aspirater og ”tørlægning” anvendes i.v. væsker som bliver hypotone efter indgift f.eks. 5 % glukose 5-10 ml/kg/time til ønsket PNa, NB undgå hyperglykæmi.
Der skal et forbavsende stort positivt vandoverskud (forskel mellem input og output) til at reducere PNa. Vanddeficit kan estimeres som:
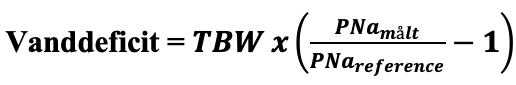
hvor TBW er total kropsvand (~kropsvægt x 0.5(kvinder)/0.6(mænd).8
F.eks. 70 kgs mand svarer PNamålt = 170 mmol/l, PNareference = 140 mmol/l og TBW 42 L til et rent vanddeficit på 9 L. Reduktion fra 170 mmol/l til mål på PNareference = 160 mmol/l kræver en positiv væskebalance på 2.6 L i væskeplanen.
Men det er vigtigt at beregningen ikke tager højde for ændringer i natrium- eller kaliumbalancen eller vedvarende vandtab og kan ikke erstatte justering af behandling ud fra monitorering af PNa og vægt. En praktisk tilgang er derfor stor vandindgift (5-10 ml/kg/time – svarende indtag af ½- 1 L Cola på en time ved svær tørst) til PNa-målet er opnået.
Når PNa reduceres svulmer cellerne op, det kan føre til hjerneødem, hvor kardinalsymptomet er nedsat bevidsthedsniveau. Omvendt er stigning i PNa associeret til mortalitet og osmotisk demyelinisering.7 Den optimale korrektionshastighed hos den enkelte patient kendes ikke. PNa kan reduceres hurtigt (> 12 mmol/l/døgn), hvis patienten ikke falder i bevidsthedsniveau af dette.15 16 Hos patient som ikke kan vurderes cerebralt stiles mod reduktion på PNa 8-10 mmol/l/døgn.
Ved tilstande med potentielt forhøjet ICP (eks. meningitis, traumatisk hjerneskade [TBI] og akut iskæmisk/anoxisk hjerneskade) skal der udvises ekstra forsigtighed ved reduktion i PNa med tæt monitorering af bevidsthedsniveau/GCS/ICP.
Udredning og behandling
- Afdækning af vand-, natrium- og kaliumbalancerne i henhold til ligning 1 og 2 s.3. Manglende vandindtag? Tørst, kvalme? Stort output (opkast, diarré, brandsår, blødning, sved, urin)?
- Vejning diagnosen og monitorering af behandlingen (vandbalancen). Ændring fra udgangsvægt (indlæggelse/oplyst) og dag til dag ændringer.
- Komorbiditet (efter akut nyresvigt,17 efter urinvejsobstruktion, diabetes insipidus/mellitus, intracerebral patologi)?
- Medicinstatus (særligt diuretika).
- Udover tørst/kvalme og dermed vandindtaget reguleres PNa renalt. Urinens påvirkning af PNa kan vurderes ud fra EFWC på spoturin:18
- Ved UNa + UK > PNa modvirker urinen hypernatriæmien. Årsagen til dehydreringen er primært at vandtab (f.eks. basale, gastrointestinale, renale, sår, sved) ikke er erstattet. Tabet søges reduceret (f.eks. temperaturkontrol, pauser laksantia) og vanddeficit erstattes.
- Ved UNa + UK < PNa bidrager urinen til hypernatriæmien evt. med andre vandtab. Årsagerne kan være:
Osmotisk diurese. Glukosuri. Stor karbamidudskillelse. Andre osmotisk aktive stoffer i urinen.
Hyperglykæmi behandles. Evt. proteinoverdosering reduceres.
Furosemid. Reducerer nyrernes evne til at producere koncentreret urin.19 Pauseres/seponeres.
Diabetes insipidus (DI): Timediureser > 4 ml/kg (NB diureserne aftager ved udtalt hypovolæmi ved svær dehydrering/høj PNa), stigende PNa og UNa < 20 mmol/l. DI deles i:
-
- Central diabetes insipidus (CDI) kan bl.a. opstå ved inkarceration (organdonor), traumatisk hjerneskade (kan være tegn på cerebral forværring), hypofysenær tumor/kirurgi, pituitær apoplexi og anden CNS-skade. Samtidig binyrebarkinsufficiens maskerer CDI.8 Se Tabel 1 s.11 for andre årsager til CDI.20 Behandles som udgangspunkt med desmopressin, f.eks. 1-2 µg i.v. 1-2 gange dagligt 20 µg nasalt eller 120 µg smelt tablet hos voksne og 0,025 µg/kg i.v. 1-2 gange dagligt hos børn.
- Nefrogen diabetes insipidus (NDI) kan være medfødt eller erhvervet. En relativt hyppig årsag på intensiv er efter akut nyresvigt med polyuri.17 Andre årsager kan være efter urinvejsobstruktion, kronisk lithium behandling, V2-receptorantagonist behandling og hyperkalkæmi (Se Tabel 2 s.12 for andre årsager). Behandlingen består af vandkorrektion, evt. medicinsanering og korrektion af hyperkalkæmi. Ved kronisk NDI diæt med lavt solute load, prostaglandinsyntesehæmmere og thiazider.
Hypernatriæmi forårsaget af salt- og vandoverskud – deresuscitation
Generelt
Hypernatriæmi pga. natrium-, kalium- og vandoverskud opstår oftest under indlæggelse. Adskilles fra hypernatriæmi pga. dehydrering ved vægtøgning og positiv væskebalance.
Årsagen er oftest indgift af natrium- og kaliumholdige væsker, hvor vandtabet efterfølgende overstiger natrium- og kaliumtabet (Se Ligning 1 s.3) særligt i forbindelse med deresuscitation. Væskerne er ofte isotoniske efter indgift som 0,9 % NaCl, KNaCl eller moderat hypotone som Ringers laktat/acetat, men kan også være i kombination med indgift af hypertone væsker som hyperton NaCl og hyperton NaHCO3 (Se Tabel 3 hyppigt anvendte iv væsker).8
Behandlingen rettes mod årsager til saltoverskuddet og ved at skabe en negativ saltbalance. Den negative saltbalance opnås ved at reducere saltindtaget ved at gennemgå medicin og væsker. Da ernæringsprodukter med lavt natriumindhold ofte er med 1 kcal/ml og indeholder ca. 11 mmol/l natrium i modsætning til ca. 43 mmol/l i almindelige produkter, vindes der relativt lidt ved dette i forhold til f.eks. at blande medicin i ikke saltholdige væsker og reducere mængden.
Samtidig øges natriumudskillelsen med:
- Sikring af blodsukker 6-10 mmol/l (undgå glukosuri)
- Thiazid (f.eks. Hydromed® 25-50 mg p.o. dagligt [voksne] og 1-1,5 mg/kg p.o. dagligt [børn] ) eller metolazon (f.eks. Zaroxolyn® 2,5-5 mg p.o. dagligt [voksne] og 0,1-0,2 mg/kg p.o. dagligt [børn])
- Om muligt spironolacton (Spiron® p.o.; Aldactone® i.v..) f.eks. 50-100 mg dagligt (voksne) og 1-2 mg/kg dagligt (børn); obs nyreinsufficiens og hyperkaliæmi8
- Ved manglende effekt af ovenstående kan forsøgsvis tillægges pn furosemid
- Furosemid alene øger PNa og anvendes derfor ikke som monoterapi19
Vandoverskuddet behandles som udgangspunkt ikke med mere vand. Ved fortsat stigning i PNa trods ovenstående tillægges hypotone væsker, hvis patienten ikke er for overhydreret. Førstevalg er vand i sonden/po 5-10 ml/kg/time til PNa-mål. Alternativt tilsvarende 5 % Glukose (OBS undgå hyperglykæmi). Ved PNa > 160 mmol/l overvejes dialyse (se næste afsnit).
Når PNa reduceres svulmer cellerne op, det kan føre til hjerneødem, hvor kardinalsymptomet er nedsat bevidsthedsniveau. Omvendt er stigning i PNa associeret til mortalitet og osmotisk demyelinisering.7 Den optimale korrektionshastighed hos den enkelte patient kendes ikke. PNa kan reduceres hurtigt (> 12 mmol/l/døgn), hvis patienten ikke falder i bevidsthedsniveau af dette.15 16 Hos patient som ikke kan vurderes cerebralt stiles mod reduktion på PNa 8-10 mmol/l/døgn. Hos patient med potentielt forhøjet ICP reduceres PNa forsigtigt – f.eks. 4 mmol/l per døgn – samtidig med monitorering af bevidsthedsniveau/GCS/ICP.
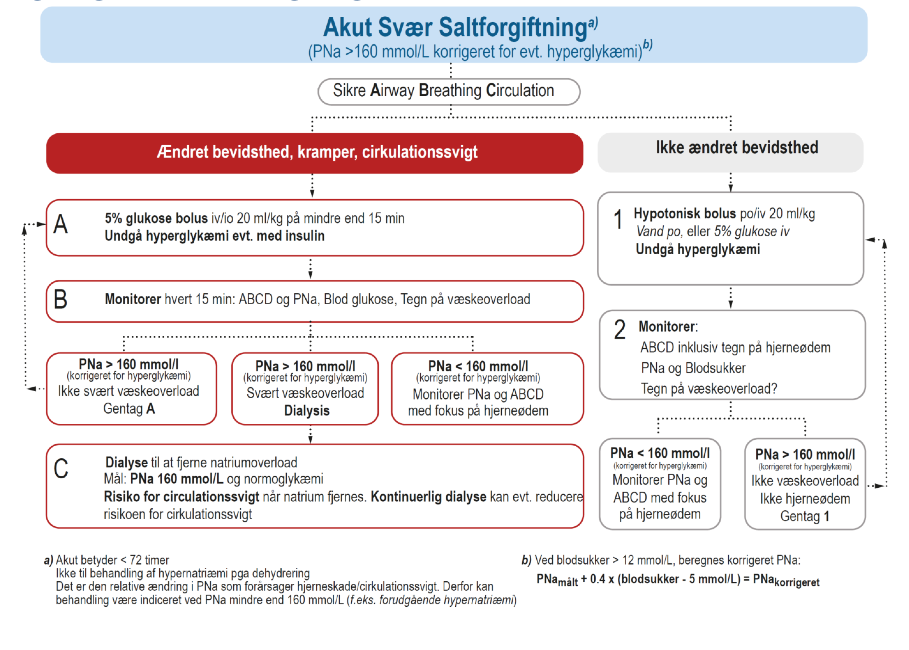
Svær saltforgiftning
Der kan opstå akut svær saltforgiftning med PNa > 160 mmol/l – Se algoritme i figur 1 – f.eks. ved stort indtag af vejsalt eller soya sauce eller iatrogent med hyperton NaCl eller DI korrigeret med 0,9 % NaCl. Her kan hurtigere korrektion være nødvendigt.21 Primært behandles med vand po/sonde 20ml/kg/time til PNa 160 mmol/l. Alternativt med 5 % glukose (hyperglykæmi behandles aggressivt). Ved tegn på væskeoverload behandles med dialyse, med opmærksomhed på risikoen for hypovolæmi pga væskeskift særligt ved hæmodialyse.21
Udredning
- Afdækning af vand-, natrium- og kaliumbalancerne inklusiv NaHCO3 og KCl i henhold til Ligning 1 og 2 s.3. Tørst? Kvalme? Stort output?
- Vejning med henblik på diagnosen og monitorering af behandlingen (vandbalancen). Ændring fra udgangsvægt (indlæggelse/oplyst) og dag til dag ændringer.
- Hyperglykæmi?
- Komorbiditet (sekundær hyperaldosteronisme, nyreinsufficiens)?
- Medicinstatus (særligt diuretika).
- Urinens påvirkning af PNa kan vurderes ud fra mængden af urin og EFWC på spoturin:
- Ved UNa + UK > PNa modvirker urinen hypernatriæmien.
- Ved UNa + UK < PNa bidrager urinen til hypernatriæmien evt. med andre vandtab:
Osmotisk diurese. Glukosuri. Stor karbamidudskillelse. Andre osmotisk aktive stoffer i urinen.
Hyperglykæmi behandles. Evt. proteinoverdosering reduceres.
Furosemid reducerer som monoterapi nyrernes evne til at producere koncentreret urin, hvilket ofte øger PNa.19 Furosemid pauseres/seponeres og der opstartes om muligt po thiazid og spironolacton som beskrevet ovenfor.
Sekundær hyperaldosteronisme. F.eks. svær levercirrhose, svært hjertesvigt. Behandles med optimering af hæmodynamik. Evt. spironolacton og ACE-hæmmer eller Angiotension-II antagonist behandling.
Hypernatriæmi og CRRT
Ved CRRT (og konventionel hæmodialyse) og hypernatriæmi er der risiko for hurtigt fald i PNa og hjerneødem. Årsagen er at CRRT-væskerne har en natriumkoncentration omkring 140 mmol/l. Stor risiko for kraftig ICP stigning ved forhøjet ICP, pga. PNa-fald og Dialyse Disequilibrium Syndrom som i sig selv kan forårsage hjerneødem.18
Fald i PNa ved CRRT kan kontrolleres ved følgende tiltag:Faldet i PNa kan reduceres ved at nedsætte effektiviteten/clearance ved at reducere udløbsdosis, f.eks. ved at anvende protokol for en lavere vægtklasse, hvis patienten tåler dette.8 18 Dette vil samtidig nedsætte risikoen for Dialyse Disequilibrium Syndrome.18
Ved høj udgangs PNa vil det ofte være nødvendigt med samtidig i.v. infusion af 1 mmol/ml hyperton NaCl.22 Forslag til opstarts infusion hastigheder:
-
- Voksen: 40 mmol/time hyperton NaCl iv og tilsvarende væsketræk plus evt. væsketræk til afvanding.
- Barn: 0,5-1 mmol/kg/time hyperton NaCl og tilsvarende væsketræk plus evt. væsketræk til afvanding.
Infusionshastigheden af hyperton NaCl justeres ud fra hyppige PNa målinger og pauseres ved CRRT nedetid. Optitrering af PNa med bolus 1 mmol/kg hyperton NaCl i.v. kan være nødvendigt (øger PNa~2 mmol/l).
Forebyggelse af hypernatriæmi
Dehydrering:
Risikoen for dehydrering under indlæggelse nedsættes ved at monitorere vandbalancen (væskeskema og regelmæssig vejning) og monitorering af PNa så vandtab erstattes. Vandbalancen er meget individuel og uafhængig af antropometriske målinger som vægt og højde.23 Derfor skal vandindgift individualiseres hos den kritisk syge. Opmærksomhed på at patient med tidligere hypernatriæmi pga saltoverskud/vandoverskud kan afvandes til hypernatriæmi pga dehydrering afspejlende sig i vægttab. Ved intenderet dehydrering ved f.eks. hypoxisk respirationssvigt afbalanceres fordele ved dehydrering overfor risikoen for hypovolæmi, nyreskade, svær tørst/delir.
Natrium-/kalium-/vandoverskud:
Hos raske er anbefalet natrium indtag 100 mmol per døgn svarende til 0,7 liter 0,9 % NaCl eller 0,8 liter Ringer-Laktat. Denne mængde er hos intensivpatienten ofte dækket ved medicinindgift og fra tryksæt. Hos den kritisk syge anvendes natriumholdige væsker til at øge ECV, f.eks. ved septisk shock og brandsårs shock. Et natriumload som langt overstiger et evt. tab er ofte nødvendigt. Det kan give bivirkninger: Respiratorisk, cirkulatorisk, renalt, sårheling, transplantatheling, anastomoseheling og tørst. Omvendt kan underdosering medføre hypoperfusion og organsvigt. Derfor doseres og revurderes væske som anden medicin og opvejes ift. vasopressor/inotropi.24 Samtidig monitoreres væskebalancen med vejning, da klinisk vurdering af vandbalancen er upræcis. Vurderes det, at et evt. vand- og saltoverload skal udskilles, er diuretikastrategien vigtig. Behandling med loop-diuretika (Furix®, Burinex®) øger vandudskillelsen relativt mere end saltudskillelsen, og kan derfor forårsage hypernatriæmi.19 Thiazider (Hydromed® 25-50 mg p.o. dagligt [voksne] og 1-1,5 mg/kg p.o. dagligt [børn]) eller metolazon (Zaroxolyn® 2,5-5 mg p.o. dagligt [voksne] og 0,1-0,2 mg/kg p.o. dagligt [børn]) øger saltudskillesen relativt mere end vandudskillelsen, og forårsager ikke i samme grad hypernatriæmi. Thiazider eller metolazon kan anvendes alene eller i kombination spironolacton (Spiron® p.o.; Aldactone® i.v..) f.eks. 50-100 mg dagligt (voksne) og 1-2 mg/kg dagligt (børn); obs nyreinsufficiens og hyperkaliæmi . Ved manglende effekt kan tillægges loop-diuretika.
Titreret hypernatriæm ved forhøjet ICP
Induktion af hypernatriæmi med hyperton NaCl er én blandt flere behandlingsmuligheder ved forhøjet ICP (analgosedation, CO2-kontrol, ekstern liquor drænage, kraniektomi med flere). Se evt. TBI-flowchart Dansk Neurotraumeudvalg: Voksne https://dnks.dk/wp-content/uploads/2021/11/TBI_flow_chart_2017.pdf og Børn https://dnks.dk/wp-content/uploads/2021/11/TBI_flow_chart_BOERN_2019.pdf
Hypernatriæmien titreres til lavest mulige PNa-værdi med tilstrækkelig effekt på ICP.
- Praktisk titreres med hyperton NaCl bolus 1 mmol/kg givet hurtigt i.v./i.o. (< 5 min).
- PNa skal ikke øges unødigt/til en arbitrær høj værdi:
- Det er den relative ændring i PNa som reducerer cellestørrelsen/reducerer hjernens vandindhold og dermed ICP.8
- Reduktion af cellevolumen modvirkes af regulatory volume increase (RVI) for at genskabe et optimalt intracellulært miljø.8 Derfor kan det være nødvendigt at øge PNa yderligere efter 12-24 timer.
- Stort natriuminput øger risikoen for renal salt wasting.24
2) PNa fastholdes på titrerede niveau.25
-
- med i.v. infusion hyperton NaCl (f.eks. 0,1-1 mmol/kg/time) evt. kombineret med p.o. fludrocortison (Florinef®) 0,05-0,3 mg/døgn (voksne) og 150 µg/m2/døgn (børn) til ICP ikke længere er labilt.
- Det kan være nødvendigt at øge PNa yderligere ved stigende ICP (pga. forværring af den tilgrundliggende årsag til ICP stigningen eller pga. RVI).
- PNa monitoreres tæt (risiko for fald i PNa pga renal/cerebral salt wasting, risiko for hurtig stigning ved udvikling af CDI)
- Ved behov for CRRT se afsnit om dette s.9 pga. risiko for voldsom ICP-stigning pga. fald i PNa samtidig med Dialyse Disequilibrium Syndrome.18
3) PNa reduceres forsigtigt (f.eks. 4 mmol/l per døgn) når ICP ikke længere er labilt.
-
- For at nedsætte risikoen for ICP-stigning.
- PNa reduceres som udgangspunkt ved at inducere en negativ natriumbalance, da hypernatriæmien er forårsaget af saltoverskud.
Figur. Algoritme Svær Saltforgiftning
Tabel 1. Årsager til central diabetes insipidus

Tabel 2. Årsager til nefrogen diabetes insipidus

Tabel 3. Hyppigt anvendte intravenøse væsker – Farve reflekterer væskernes tonicitet efter indgift
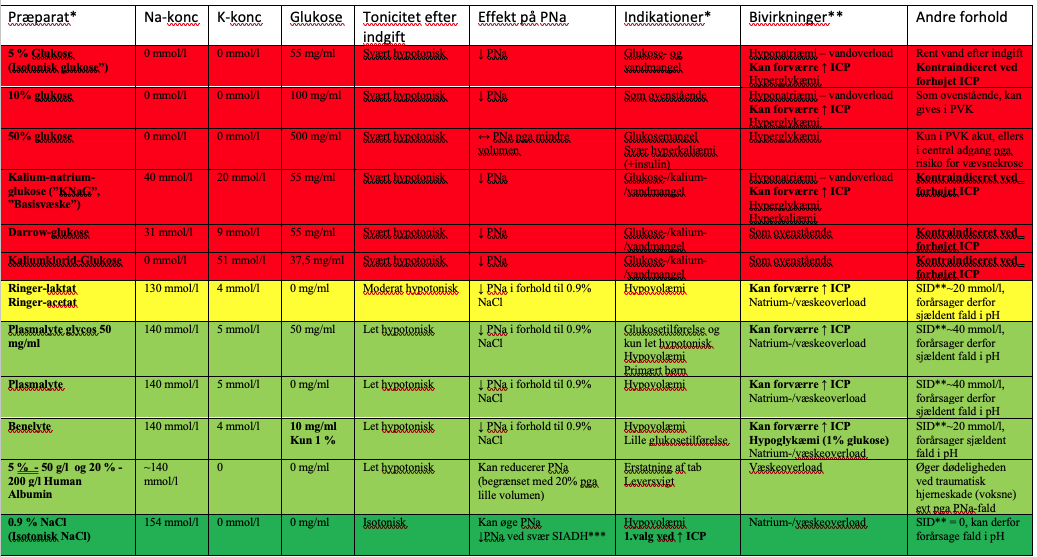
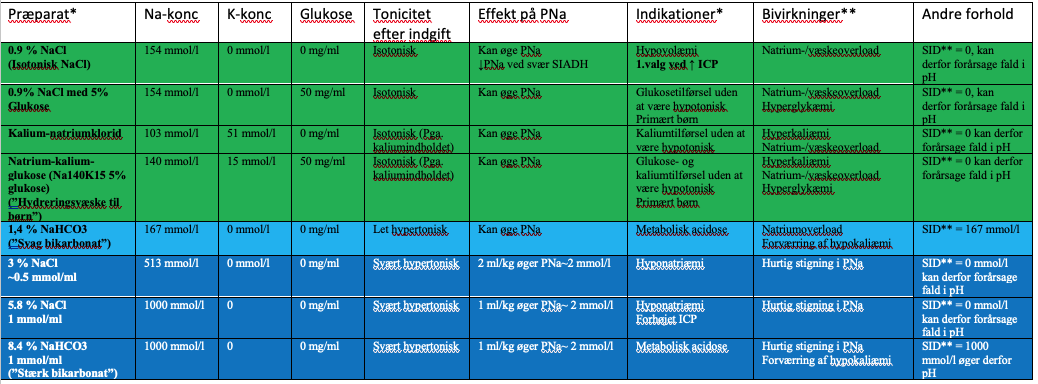
* Ikke alle i.v. væsker/indikationer/bivirkninger/indholdsstoffer er nævnt. Se evt. produktresuméet for den enkelte væske
** SID = Strong ion difference her approximeret som [Na+]-[Cl-]. I plasma er SID~40 mmol/l. Fald i SID reducerer pH. Stigning i SID øger pH.
*** Ved svær SIADH med UNa + UK > 154 mmol/l reducerer 0.9 % NaCl (Na 154 mmol/l) PNa.
Reference List
1. Stelfox HT, Ahmed SB, Khandwala F, et al. The epidemiology of intensive care unit-acquired hyponatraemia and hypernatraemia in medical-surgical intensive care units. Crit Care 2008;12(6):R162.
2. Sakr Y, Rother S, Ferreira AM, et al. Fluctuations in serum sodium level are associated with an increased risk of death in surgical ICU patients. Crit Care Med 2013;41(1):133-42.
3. Darmon M, Timsit JF, Francais A, et al. Association between hypernatraemia acquired in the ICU and mortality: a cohort study. NephrolDialTransplant 2010;25(8):2510-15.
4. Darmon M, Diconne E, Souweine B, et al. Prognostic consequences of borderline dysnatremia: pay attention to minimal serum sodium change. Crit Care 2013;17(1):R12. doi: 10.1186/cc11937 [published Online First: 20130121]
5. Funk GC, Lindner G, Druml W, et al. Incidence and prognosis of dysnatremias present on ICU admission. Intensive Care Med 2010;36(2):304-11.
6. Lindner G, Funk GC, Schwarz C, et al. Hypernatremia in the critically ill is an independent risk factor for mortality. AmJKidney Dis 2007;50(6):952-57.
7. Arzhan S, Roumelioti ME, Litvinovich I, et al. Outcomes of Hospital-Acquired Hypernatremia. Clin J Am Soc Nephrol 2023;18(11):1396-407. doi: 10.2215/CJN.0000000000000250 [published Online First: 20230918]
8. Overgaard-Steensen C, Ring T. Clinical review: practical approach to hyponatraemia and hypernatraemia in critically ill patients 1. Crit Care 2013;17(1):206.
9. Baylis PH, Thompson CJ. Osmoregulation of vasopressin secretion and thirst in health and disease. Clin Endocrinol (Oxf) 1988;29(5):549-76. doi: 10.1111/j.1365-2265.1988.tb03704.x
10. Edelman IS, Leibman J, O’Meara MP, et al. Interrelations between serum sodium concentration, serum osmolarity and total exchangeable sodium, total exchangeable potassium and total body water. JClinInvest 1958;37(9):1236-56.
11. Rose BD. New approach to disturbances in the plasma sodium concentration. AmJMed 1986;81(6):1033-40.
12. Hillier TA, Abbott RD, Barrett EJ. Hyponatremia: evaluating the correction factor for hyperglycemia. AmJMed 1999;106(4):399-403.
13. Nanda SK, Ray L, Dinakaran A. Agreement of arterial sodium and arterial potassium levels with venous sodium and venous potassium in patients admitted to intensive care unit. J Clin Diagn Res 2015;9(2):BC28-30. doi: 10.7860/JCDR/2015/12418.5602 [published Online First: 20150201]
14. Bhave G, Neilson EG. Volume depletion versus dehydration: how understanding the difference can guide therapy. AmJKidney Dis 2011;58(2):302-09.
15. Feigin E, Feigin L, Ingbir M, et al. Rate of Correction and All-Cause Mortality in Patients With Severe Hypernatremia. JAMA Netw Open 2023;6(9):e2335415. doi: 10.1001/jamanetworkopen.2023.35415 [published Online First: 20230905]
16. Chauhan K, Pattharanitima P, Patel N, et al. Rate of Correction of Hypernatremia and Health Outcomes in Critically Ill Patients. Clin J Am Soc Nephrol 2019;14(5):656-63. doi: 10.2215/CJN.10640918 [published Online First: 20190404]
17. Hamdi A, Hajage D, Van Glabeke E, et al. Severe post-renal acute kidney injury, post-obstructive diuresis and renal recovery. BJU Int 2012;110(11 Pt C):E1027-34. doi: 10.1111/j.1464-410X.2012.11193.x [published Online First: 20120515]
18. Overgaard-Steensen C, Ring T. Disorders of Sodium and Water Balance. Critical Care Nephrology Third Edition2019.
19. Bihari S, Holt AW, Prakash S, et al. Addition of indapamide to frusemide increases natriuresis and creatinine clearance, but not diuresis, in fluid overloaded ICU patients. J Crit Care 2016;33:200-6. doi: 10.1016/j.jcrc.2016.01.017 [published Online First: 20160127]
20. Oiso Y, Robertson GL, Norgaard JP, et al. Clinical review: Treatment of neurohypophyseal diabetes insipidus 20. JClinEndocrinolMetab 2013;98(10):3958-67.
21. Overgaard-Steensen C, Poorisrisak P, Heiring C, et al. Fatal case of hospital-acquired hypernatraemia in a neonate: lessons learned from a tragic error. Clin Kidney J 2021;14(4):1277-83. doi: 10.1093/ckj/sfaa108 [published Online First: 20200706]
22. Yessayan L, Yee J, Frinak S, et al. Continuous Renal Replacement Therapy for the Management of Acid-Base and Electrolyte Imbalances in Acute Kidney Injury 1. AdvChronicKidney Dis 2016;23(3):203-10.
23. Raman A, Schoeller DA, Subar AF, et al. Water turnover in 458 American adults 40-79 yr of age. AmJPhysiol Renal Physiol 2004;286(2):F394-F401.
24. Lunoe M, Overgaard-Steensen C. Prevention of hospital-acquired hyponatraemia: individualised fluid therapy. Acta Anaesthesiol Scand 2015;59(8):975-85. doi: 10.1111/aas.12522 [published Online First: 2015/05/12]
25. Roquilly A, Mahe PJ, Latte DD, et al. Continuous controlled-infusion of hypertonic saline solution in traumatic brain-injured patients: a 9-year retrospective study. Crit Care 2011;15(5):R260. doi: 10.1186/cc10522 [published Online First: 20111028]