NBV Kritisk syge børn: National behandlingsvejledning for børneintensiv terapi
2. udgave 2025. Udarbejdet af arbejdsgruppe under DASAIM
og Guidelinegruppen ved Intensiv Symposium Hindsgavl.
Godkendt den 23-01-2025 på guidelinemøde og af DASAIMs bestyrelse den ??-03-2025.
Indledning
Denne nationale behandlingsvejledning for kritisk syge børn er lavet af en stor og bred arbejdsgruppe med repræsentanter fra hele landet. På Guidelinemødet i januar 2023, blev det besluttet at 1. udgave af vejledningen aktuelt var dækket af ”Akut-barn appen” og at denne 2. udgave derfor skulle have et andet fokus. Derfor beskriver denne vejledning behandlingen af det kritisk syge barn, der indlægges på en børneintensiv afdeling. Dette efter at den hyperakutte stabilisering er foretaget, og hvor ”Akut barn appen” dækker behovet.
Evidensen for behandling af børn på intensiv, er på mange områder sparsom eller ekstrapoleret fra studier fra voksne patienter. Derfor er vejledningen ikke opbygget efter GRADE-principperne. Vejledningen beskriver overvejende ”Best Practice” udledt af tilgængelig litteratur og internationale vejledninger på området. Det lægefaglige skøn af det enkelte kritisk syge barn, støttet af forslag i denne vejledning, anbefales derfor stadig af styregruppen at være afgørende.
Vejledningen er bygget op efter organsystemer, som er lig den måde en patient ville blive systematisk vurderet og behandlet på en børneintensiv afdeling. Vejledningen afsluttes med et kapitel om interhospital transport.
Arbejdsgruppe
Tovholder / Korrespondance: Thomas Pasgaard (thomas.pasgaard@auh.rm.dk)
Redaktører af den samlede vejledning:
Johan Emdal Navne (johan.emdal.navne@regionh.dk)
Jørgen Wiis – Repræsentant for Guidelinegruppen (Joergen.Wiis@regionh.dk)
Lasse Wegener Lund (lasse.wegener.lund@regionh.dk)
Marcela Carlsson (Marcela.Carlsson@rsyd.dk)
Thomas Pasgaard (Thomas.pasgaard@auh.rm.dk)
Ulla Lei Larsen (Ulla.Lei.Larsen@rsyd.dk)
Forfattere til de enkelte afsnit:
Centralnervesystemet (CNS):
Lasse Wegener Lund, Hoveduddannelse Anæstesi, Region Øst.
Johan Emdal Navne, Afdeling for Intensiv behandling, Rigshospitalet.
Helene Gudmann Steuble Brandt, Afdeling for bedøvelse og intensiv behandling, Neurocentret, RH
Marianne Berntsen, Afdeling for bedøvelse og intensiv behandling, Neurocentret, Rigshospitalet.
Tobias Magid, Afdeling for bedøvelse og operation, Center for Kræft og Organsygdomme, RH.
Kristin Brønnum Nystrup, Klinik For Lindrende Behandling, Rigshospitalet
Christina Høi-Hansen, Afdeling for Børn og Unge, Rigshospitalet
Respiratorisk:
Marcela Carlsson, Anæstesiologisk Intensiv Afdeling V, Odense Universitetshospital.
Thomas Pasgaard, Intensiv Afd., Aarhus Universitetshospital.
Jeppe Sylvest Angaard Nielsen, Afdeling for intensiv behandling af nyfødte og mindre børn, RH.
Søren Kjærgaard, Anæstesi og Intensiv Afd., Aalborg Universitetshospital.
Cirkulatorisk:
Thomas Pasgaard, Intensiv Afd., Aarhus Universitetshospital.
Jeppe Sylvest Angaard Nielsen, Afdeling for intensiv behandling af nyfødte og mindre børn, RH
Jesper Brøndum Poulsen, Thoraxanæstesiologisk klinik, Rigshospitalet.
Therese Risom Vestergaard, Thoraxanæstesiologisk klinik, Rigshospitalet.
Abdominalt/Ernæring:
Ulla Lei Larsen, Anæstesiologisk Intensiv Afdeling V, Odense Universitetshospital.
Jørgen Wiis, Afdeling for Intensiv behandling, Rigshospitalet
Maria Grevit, Anæstesiologisk Intensiv Afdeling V, Odense Universitetshospital.
Peter Søndergaard Tyrrestrup, Anæstesi Nord, Aalborg Universitetshospital.
Renalt:
Ulla Lei Larsen, Anæstesiologisk Intensiv Afdeling V, Odense Universitetshospital.
Anders Bastiansen, Afdeling for Intensiv behandling, Rigshospitalet.
Henrik Gammelager, Intensiv Afd., Aarhus Universitetshospital.
Jeppe Bove, Anæstesiologisk Intensiv Afdeling V, Odense Universitetshospital.
Marcela Carlsson, Anæstesiologisk Intensiv Afdeling V, Odense Universitetshospital.
Systemisk/endokrinologisk:
Johan Emdal Navne, Afdeling for Intensiv behandling, Rigshospitalet.
Asta Aliuskeviciene, Børneanæstesi, Unge- og Gravide, Aarhus Universitetshospital.
Jeppe Sylvest Nielsen, Afdeling for intensiv behandling af nyfødte og mindre børn, RH.
Lasse Wegener Lund, Hoveduddannelse Anæstesi, Region Øst.
Koagulation:
Thomas Pasgaard, Intensiv Afd., Aarhus Universitetshospital.
Asta Aliuskeviciene, Børneanæstesi, Unge- og Gravide, Aarhus Universitetshospital.
Christine Lodberg Hvas, Intensiv Afd., Aarhus Universitetshospital.
Lotte Marie Vestergaard, Sjællands Universitetshospital, Køge.
Interhospital transport:
Mads Astvad, Afdeling for Intensiv behandling, Rigshospitalet.
Tobias Magid, Afdeling for bedøvelse og operation, Center for Kræft og Organsygdomme, RH
Kapitel 1 – Sedation-, smerte- og abstinensbehandling
| · Analgosedation skal målrettes den kliniske situation
· Børn udvikler hurtig tolerance og abstinenser · Delirium forekommer hyppigt, oftest som stille delir (risiko for underdiagnosticering) · Benzodiazepiner bør minimeres (kraftig uafhængig risikofaktor for delirium) medmindre det er klinisk indiceret (kramper, ICP-kontrol mv.) · Non farmakologiske tiltag er essentielle ved evaluering af det ukomfortable barn · Ved kortvarig respiratorbehandling < 48 timer / delayed ekstubation foreslås alfa-2 agonist (dexmedetomidin/clonidin) eller propofol (< 4 mg/kg/t) som sedativa samt et opioidpræparat med kort halveringstid · Ved længerevarende > 48 timers respiratorbehandling foreslås alfa-2 agonist (dexmedetomidin /clonidin) som sedativa samt et opioidpræparat og ved behov, tillæg af intermitterende adjuverende medicin (propofol, esketamin, barbiturater eller benzodiazepin mm) · Nasal intubation foretrækkes så snart barnet er stabiliseret · Anvend sedations-, smerte-/ abstinens-og delir-scoringsredskaber som personalet er velkendt med |
Formål med analgesi og sedation
• Lindring af angst
• Lindring af smerter
• Patientsikkerhed: Forhindre selv-ekstubation, tab af CVK mm. eller selvskadende adfærd
• Immobilisering: Muliggørelse af invasive, risikable eller smertefulde procedurer (CVK-anlæggelse, CRRT, CT-scanninger, sårskift mm.)
• Respiratorbehandling: Tubeaccept, respiratorsynkroni, bedret oxygenering/ventilation
• Andre specifikke behandlinger: Reduktion af øget ICP, krampebehandling mv.
Analgosedation – fordele og ulemper

Tabel 1
Non-farmakologiske tiltag skal altid benyttes hvor muligt
• Lejring, aflastende madras, sikre ernæring, behandling af kvalme, udelukke urinretention og sikre GI funktion.
• Distraktion – tablet, musik, mv.
• Familieinddragelse, forklaring, beroligelse, tilstedeværelse
• Døgnrytme – mørke og ro om natten, mobilisering og aktiviteter om dagen og samle procedurer/blodprøvetagninger.
Farmakologiske tiltag
| Smertestillende lægemidler | |
| Type | Kommentar |
| Topikale lægemidler | Overfladeanalgesi før stik (Eks. EMLA) |
| Lokalanæstesi v kateteranlæggelse mv. | |
| Regional blokade | Epidural (større abd cikatrice/rygoperation, ribbensfrakturer) |
| Smertekatetre | |
| Non-opioider | Paracetamol, oftest relevant, CAVE svær leversvigt
NSAID, ofte Post-OP, forsigtighed ved nyresvigt, koagulopati, GI blødning Clonidin – sederende med let analgesi uden respiratorisk påvirkning Tricykliske antidepressiva (TCA) f.eks amitriptylin (neuropatiske smerter) Antiepileptika (feks gabapentin) ved neuropatiske smerter S-ketamin |
| Opioider | PCA pumpe
Helst administreret po/sonde jævnt fordelt over døgnet Lejring, aflastende madras, sikre ernæring |
Tabel 2.
Sedativa og adjuverende medicin
Til behandling af angst, agitation og seponerende adfærd.
Har stor grad af tilvænning, hvorfor skift mellem lægemidler ofte er nødvendigt.
Bør styres iht. scoring af sedationsdybde med COMFORT-B (se monitorering)
| Sedativa og adjuverende medicin | |
| Medikament | Kommentar |
| Propofol | Max 4 mg/kg/t (infusion + boli) max 48 (72) timer, Obs risiko for PRIS |
| Alfa2-agonister | Dexmedetomidine infusion eller clonidin-infusion/refrakte doser |
| Opioider | Synergistisk sløvende effekt med andre sedativa |
| Benzodiazepiner | God amnesi og beroligende. Begrænses hvis muligt, stærk risikofaktor for delir |
| S-Ketamin | Dissociativ og smertestillende effekt, enten bolus eller infusion, gives i kombination med benzodiazepin for at mindske bivirkninger |
| Barbiturater | F.eks. ved svær status epilepticus, ICP-kontrol, svær pARDS |
| Neuromuskulær blokade | Bolus eller infusion. Ved f.eks. invasive procedurer, svær pARDS, respiratordyssynkroni, pulmonal hypertension mfl. Der skal sikres sufficient analgosedation (obs awareness). |
| Inhalationsanæstesitka | Hvis tilgængeligt, gives som escape eller ved f.eks. svær status astmaticus |
Tabel 3
Sedationsstrategi
Sedation af intuberede børn tager udgangspunkt i indikationen, formålet med behandlingen (herunder valg af sedationsdybde) og vil afhænge af grundsygdom, komorbiditet og forventet varighed. Denne bør løbende revurderes i henhold til den kliniske status af barnet.
I henhold til de overordnede principper stiles efter:
- Minimal benzodiazepin eksponering (stærk risikofaktor for delir)
- Præparatvalg justeret ud fra indikation og optimering af synergistisk effekt, typisk med en kombination af sedativa som Dexmedetomidin og/eller Propofol sammen med korttidsvirkende opioid som morfin, Fentanyl eller Remifentanil.
- Ved behov for yderligere sedationsdybde kan suppleres med pn benzodiazepin (f.eks. Lorazepam) eller pn Clonidin (NB ej Clonidin samtidig med inf. Dexmedetomidine).
- Giv bolus opioid før smertefulde procedurer for at undgå unødige stigninger i infusionshastighed
- Undgå oversedation og minimer eksponeringsvarighed grundet øget risiko for abstinensudvikling ved udtrapning samt udvikling af delirium (se særskilt instruks).
- Der henvises til andre guidelines ved særlige kliniske problemstillinger, herunder forhøjet intrakranielt tryk, refraktær status-epilepticus, pARDS, pulmonal hypertension mv.
Nedenfor angivet forslag til analgosedation med startdoser og vedligehold, baseret på forventet respiratorvarighed.
Forventet respirator varighed < 48 timer
Remifentanil
· Dosis:
– Infusion 3 – 12 g/kg/time (dvs. 0.06 – 0.24 ml/kg/time af konc. 50 g/ml)
– Risiko for bradykardi, hypotension (overvej skift til Fentanyl ved cirkulatorisk dekompensation)
– NB: Før abrupt ophør opstartes adækvat analgesi og evt. pn Clonidin
Dexmedetomidin
· Startdosis:
– Bolus bør undgås (hypotension/bradykardi risiko, CAVE: 2. og 3 grads AV blok)
– Infusion 0,2 – 2,0 g/kg/time. Start med 1.5 g/kg/time svt 0.375 ml/kg/time (konc. 4 g/ml) og titreres herefter til effekt.
Ved behov for yderligere sedation foreslås pn Lorazepam (dosis 0.05 – 0.1 mg/kg iv, hver 2.-4 time, max dosis 4 mg/dosis) inden yderligere supplerende tiltag overvejes.
Alternativt Clonidin-infusion
· Startdosis:
– Bolus undgås (hypotension/bradykardi risiko). Infusion 0,2 – 2,0 g/kg/time.
Propofol (evt. som supplement ved behov for dybere sedation)
· Startdosis
– Infusion 2 mg/kg/time svt. 0,2 ml/kg/time af konc. 10 mg/ml
NB: Propofoldoser bør ikke overstige totalt 4 mg/kg/time, (infusion samt bolus) eller fortsætte længere end 48 timer pga. risiko for PRIS. Tillæg i stedet Clonidin (enteralt eller iv) eller inf. Dexmedetomidine med henblik på reduktion af akkumuleret Propofoldosis. Yderligere kan suppleres med pn doser Lorazepam (enteralt/iv). Hvis fortsat utilstrækkeligt opstartes Midazolam-infusion.
NB: Propofol er kontraindiceret ved Brugada syndrom, abnorm lipidmetabolisme samt kendt mitokondriesygdomme.
Forventet varighed > 48 timer
Fentanyl
· Startdosis:
– Bolus 1-2 gr/kg
– Infusion 0,5 – 2 gr/kg/time svt. 0,01 – 0,04 ml/kg/time af konc. 50 g/ml
Ved behov for doser over 2 g/kg/t skal der overvejes supplerende tiltag
Alternativt Morfin
· Startdosis:
– Bolus 0,05 – 0,1 mg/kg
– Infusion 0,02 – 0,3 mg/kg/time svt. 0,02 – 0,3 ml/kg/time af konc. 1 mg/ml
Dexmedetomidin
· Startdosis:
– Bolus undgås (hypotension/bradykardi risiko, CAVE: 2. og 3 grads AV blok)
– Infusion 0,2 – 2,0 g/kg/time. Start med 1,5 g/kg/time svt 0,375 ml/kg/time (konc. 4 g/ml) og titreres herefter til effekt.
Ved behov for yderligere sedation foreslås pn Lorazepam (dosis 0,05 – 0,1 mg/kg iv, hver 2.- 4. time, max dosis 4 mg/dosis) inden yderligere supplerende tiltag overvejes.
Alternativt Clonidin-infusion
· Startdosis:
– Bolus undgås (hypotension/bradykardi risiko)
– Infusion 0,2 – 2,0 g/kg/time
Midazolam (2. Valg, eller supplement)
· Startdosis:
– Bolus 0,1 mg/kg (max 5 mg)
– Infusion 0,1 – 0,5 mg/kg/time svt. 0,02 ml/kg/time af 5 mg/ml
Revurder løbende sedationsdybde med henblik på dosisreduktion grundet risiko for akkumulation, særligt ved AKI (aktive metabolitter) samt abstinens og delirium.
Clonidin i refrakte doser (dog ej ved pågående dexmedetomidin- eller clonidin infusion)
· Tillægges f.eks. når midazolam kører > 0,3 mg/kg/time
– Dosis 2 – 4 g/kg x 4 – 6 iv evt. po max 100 g/dosis
Tiltag ved stigende sedationsbehov
• Overvej andre årsager til uro hos barnet (se ovenstående)
• Vurder om den non-farmakologiske behandling kan optimeres
• Skift oral til nasal intubation
• Tillæg adjuverende præparater (se nedenfor)
• Optimer intervaller af pn-administrationer
• Overvej rotation af sedativa (pga. tilvænning)
• Propofol kan fortsat anvendes pn som supplement ved kortvarige ikke smertefulde procedurer
Dosis forslag til adjuverende præparater ved behov for øget sedationsdybde
S-Ketamin
· Gives som supplement til eksisterende sedativa/analgetika, som herefter ofte vil kunne af- eller nedtrappes.
– Startdosis 0,5 – 1 (max 2) mg/kg/t, svt 0,25 – 0,50 (max 1,0) ml/kg/t
(konc. 2 mg/ml.)
– Infusion 0,3 – 2 (max 5) mg/kg/t
– Bør suppleres med et benzodiazepin, f.eks. Lorazepam, mhp dosisreduktion og mindskning af bivirkninger
– Desuden synergistisk effekt ved anvendelse med Propofol, og mulighed for ketamin-dosisreduktion. Kan med fordel opstartes 4-6 timer før ekstubation for roligere opvågning
– Ved udtalt spytsekretion overvej Robinul eller atropin 0.02 mg/kg/dosis – max 0.5 mg/dosis).
Kloralhydrat
· Gives som supplement til eksisterende sedativa/analgetika. Kan kun gives p.o,/sonde.
– 20 mg/kg x2-4/døgn. Max 1000 mg/døgn
Barbiturater
Indikation: Behov for dybere sedation f.eks. ved pARDS respiratorbehandling, status epilepticus mhp burst suppression eller behandling af forhøjet ICP
· Gives som supplement til eksisterende sedativa, som herefter ofte vil kunne aftrappes.
– Thiopental inj 50 mg/ml, (neo/pæd) inj 2,5 mg/ml.
– Bolus: 2-3 mg/kg i.v (langsom indgift obs hypotension)
– Infusion: 1-5 mg/kg/t (ved status epilepticus og ICP kontrol se særskilt vejledning)
Se-niveau: 150 – 200 mol/L (x 0,24 = g/ml)
– Eller
– Phenobarbital (fenemal) inj 100 mg/ml, oral opl 5 mg/ml, oral opl 10 mg/ml eller tabl 15 mg
– Loading dosis: 10 mg/kg iv (langsom indgift) ved kramper. Kan gentages op til 3 x dgl.
– Evt. vedligehold: 2,5 – 4 mg/kg iv/p.o x 1-2 dgl.
Sevofluran (hvis tilgængeligt)
· Gives vha. SedaConDa
– Doseres primært iht. til effekt. Den terapeutiske værdi Fet% (0,6 % – 1%) er kun vejledende. Ved mindre børn (Tidalvolumen < 200 ml), hvor SedaConda’en er placeret på inspirationsslangen, skal der relativt højere infusionshastigheder for at opnå samme Fet%
– Skift til Propofol 4-6 timer før ekstubation for roligere opvågning
Relaksantia
· Bør kun gives ved sufficient analgosedation (OBS awareness), og ifm. procedurer eller når indikeret ved f.eks. svært respiratorisk svigt.
– Rocuronium – Bolus 0,5 – 1 (1,2) mg/kg/dosis (NB Forlænget effekt ved nyre-og leversvigt samt neuromuskulær sygdom)
Antidot sugammadex = Bridion, 4-16 mg/kg iv
– Cisatracurium – Bolus 0,1 – 0,2 mg/kg, infusion 0,2 – 0,3 mg/kg/time titreres til effekt (max 0,7 mg/kg/t)
Monitorering
Comfort-B Score: Redskab til vurdering af smerter og sedationsdybde hos intuberede og intensivt behandlede børn.
Optimalt vurderes parametrene over én uforstyrret time.
 Comfort-B Score
Comfort-B Score
Mål
· 6-12 point overvejes om patienten er for dybt sederet
· 13-20 point vil sedationsdybden ofte være passende.
· 21-30 point overvejes om patienten er for overfladisk sederet.
Eksempel på abstinens/delir scoringsredsskab
SOS-PD Skala (Sophia Observation Withdrawel Symptoms Scale)
Børn i risiko for udvikling af abstinenser ved udtrapning af opioider og benzodiazepiner, og delirium efter indlæggelse i mindst 48 timer. (se i øvrigt instruks vedr. delirium)
Abstinens og udtrapningsplan af sedativa og opioid
Inden udtrapning af sedativa og ekstubation skal risiko for udvikling af abstinens vurderes. Ved eksponering for høje doser og/eller varighed ≥ 2-3 dage, vil risikoen for abstinensudvikling være høj, og det vil være relevant at opstarte iv/enteral aftrapning.
Abstinenssymptomer
Tabel 4
Forebyggelse af abstinenser efter langvarig sedation (> 3 dage) og børn i risiko (lav alder, høj kumuleret medicin eksponering)
- Abstinensscores f.eks. med SOS-PD. (Inkluderer både abstinens- og delir scoring)
- Omlægning af et præparat ad gangen fra infusion til intermitterende.
- IV administration indtil sikker enteral funktion.
- Herefter lægges aftrapningsplan af analgetika og sedativa på alternerende dage. Først sidst i rolig fase aftrappes clonidin. Barnet bør have lagt plan for aftrapning før overflytning fra intensiv til sengeafdeling.
Nedenfor følger eksempler på omstilling af Fentanyl infusion til Metadon, Midazolam infusion til Lorazepam og Dexmedetomidin infusion til Clonidin. Samme principper kan anvendes ved andre præparater, fx morfininfusion til peroral morfin. Man bør i høj grad være opmærksom på forhold omkring ækvipotens, især ved overgang fra intravenøs til peroral administration.
Fentanyl
Tilstræber langsom aftrapning ved hjælp af opioid med lang halveringstid (metadon).
Start med intravenøs metadon indtil pt har sikker enteral absorption.
Overgang fra Fentanyl til Metadon
| Trin | Handling |
| 1 | Beregn seneste døgndosis Fentanyl i mg |
| 2 | Startdosis Metadon svarer til døgndosis Fentanyl fordelt på 3 (-4) doser |
| 3 | Efter 2. Metadon dosis reduceres Fentanyl infusion med 50%. |
| 4 | Efter 3. Metadon dosis reduceres Fentanyl med yderligere 50%. |
| 5 | Efter 4. Metadon dosis seponeres Fentanyl |
| 6 | Dosis er vejledende. Det tilrådes at give Metadonen iv indtil korrekt dosis er opnået, og tilstanden er stabil. Derefter skiftes til peroral administration i samme dosis. |
| 7 | Den totale mængde pn. Morfin indgivet i løbet af 24 timer pga. opioid abstinenser omregnes og lægges til næste dags metadondosis |
| 8 | Ved fortsatte abstinenssymptomer de næste 72 timer gives Morfin i ovennævnte dosering, men metadon dosis ændres ikke indenfor denne periode |
| 9 | Hvis patienten bliver for sederet, holdes en Metadondosis tilbage, og dosis reduceres med 10-20% |
| 10 | Når en passende dosis er opnået påbegyndes aftrapningen med 25 % af dosis 1 gang om ugen, således at Metadon aftrappes over i alt 4 – 6 uger |
Eksempel:
Børn: Der er givet inf. Fentanyl 2 ml/time (0,1 mg/time) i sidste døgn svarende til døgndosis på 2,4 mg. Beregnet iv/peroral Metadon dosis: 2,4 mg fordelt på 3 doser, svt. 0,8 mg x 3.
Midazolam
Langsom aftrapning vha. peroral benzodiazepin med lang halveringstid. Lorazepam foretrækkes frem for diazepam og midazolam, idet sidstnævnte har aktive metabolitter med variabel halveringstid og virkningsvarighed. Nogle centre bruger dog midazolam, hvor formulering til iv. kan gives p.o/per sonde.
Overgang fra Midazolam til Lorazepam
| Trin | Handling |
| 0 | Beregn seneste døgndosis Midazolam |
| 1 | Beregn ækvivalent Lorazepam dosis = Døgndosis Midazolam divideret med 12. |
| 2 | Startdosis Lorazepam fordeles på 4 doser peroralt/i sonde eller intravenøst (iv). |
| 3 | Reducer Midazolam infusion med 50 % efter 2. dosis Lorazepam. |
| 4 | Reducer Midazolam infusion med yderligere 50 % efter 3. dosis Lorazepam. |
| 5 | Seponér (stop) Midazolam infusion efter 4. dosis Lorazepam. |
| 6 | Ved abstinenser som kvalme/opkastning under omstillingen kan pn Lorazepam iv. gives i samme dosis. |
| 7 | Total Lorazepam pn mængde givet pga. abstinenser (over 24 timer) lægges til næste dags Lorazepam dosis. |
Eksempel:
Børn: Der er givet inf. Midazolam 10 mg/time i sidste døgn svarende til døgndosis på 240 mg.
Beregnet peroral Lorazepam dosis: 20 mg (240 mg: 12) fordelt på 4 doser, svt. 5 mg x 4.
Overgang fra Dexmedetomidin til Clonidin
| Trin | Handling |
| 1 | Start abstinensscoring |
| 2 | Startdosis enteral Clonidin 2-4 mg/kg (max 100 mg/dosis) hver 4. time |
| 3 | En time efter 2. dosis Clonidin reduceres Dexmedetomidin infusion med 0,2 mg/kg/t svt 0.05 ml/kg/t (konc. 4 mg/ml) |
| 4 | Herefter reduceres som ovenstående hver 4. time indtil seponering |
| 5 | Øvrige analgo-sedativa bør ikke aftrappes samtidig |
Generelt ved mistanke om abstinenser (høj SOS-PD score) og/eller rebound hypertension, takykardi, angst, feber, som ikke kan forklares på anden vis eller behandles non-farmakologisk, kan man:
– Pausere et aftrapningstrin
– Øge til seneste infusions-dosis
– Nedsætte aftrapningsdosis af infusionen
– Øge aftrapningsinterval (hver 6.- /8.- eller 12. time)
Propofol-Relateret Infusions Syndrom (PRIS)
Livstruende tilstand hos patienter der har kørt Propofol-infusion i høj dosis (>4 mg/kg/time inkl. bolus administrationer) og/eller gennem længere tid (>48 timer).
Risikofaktorer for PRIS
| Dosis > 4 mg/kg/t |
| Infusion > 48 timer |
| Vasopressorer |
| Steroider |
| Mitokondriesygdomme |
| Små glykogen depoter |
| CNS (TBI og status epilepticus) |
Symptomer og paraklinik der kan sandsynliggøre PRIS
| Primære | Sekundære |
| Ekg forandringer | Lipidæmi |
| Breddeøget QRS | Hyperkaliæmi |
| Bradykardi | AKI |
| VT / ventrikelflimmer | Feber |
| Asystoli | Kardiel dysfunktion |
| Nyopstået svær metabolisk acidose | Påvirkede leverenzymer |
| Rhabdomyolyse | Høj serum laktat |
PRIS er beskrevet ved lavere doser og kortere brug, så det skal altid haves in mente ved uforklaret metabolisk acidose, rhabdomyolyse og ekg-forandringer herunder arytmier. Flere tilfælde er beskrevet med fatalt udfald hos børn behandlet i intensiv regi.
Patogenesen er ikke klarlagt, og der findes ingen definitiv behandling, hvorfor tidlig diagnose og dermed ophør af infusion er vigtig.
Smertebehandling
Vurdering af smerter hos børn
• Hos ekstuberede børn (>2mdr), kan FLACC anvendes og fra ca. 4 års-alderen eller når barnet selv kan kommunikere om deres smerter kan anvendes Wong Baker Face Pain Scale og fra omkring 8-årsalderen VAS eller NRS-skalaen. (se nedenfor)
• Hos intuberede børn < 17 år eller ved nedsat kommunikationsevne pga. nedsat bevidsthed, mentalt handicap, vurderes ved Comfort-B score (se ovenfor).
• Det er ikke sufficient at skønne smerter alene ud fra fysiologiske tegn (takykardi, takypnø, sveden, tårer, uro, dilaterede pupiller)
Smertevurdering foretages minimum x 1/sygeplejerskevagt dvs. x 3/døgn, hyppigere ved problematisk smertebehandling, smertevoldende indgreb eller større analgetiske dosisændringer. Smertescoringer registreres i journalen.
Smertescoring (hos vågne / extuberede patienter)
FLACC – Face, Legs, Activity, Cry and Consolability. Denne metode kan bruges til børn fra ca. 2 mdrs. alderen og til de har sprog og evne til at VAS-score.
(se i øvrigt NBV fra Videnscenter for Børnesmerter, vedr. Akutte smerter hos børn og unge)

Wong Baker og VAS

Behandling
- Non-farmakologiske principper (se ovenfor)
- Topikale lægemidler (se ovenfor)
- Lette smerter: Paracetamol pn eller fast
- Moderate smerter: Paracetamol fast, NSAID fast (hvis ikke kontraindiceret.), opioid pn
- Svære smerter: Paracetamol fast, evt. NSAID fast, opioid fast (enteralt eller infusion) + pn (iv), Clonidin pn/fast
- Komplicerede smertetilstande:
- Konsultation med smerte-team
- Overvej tillæg af Gabapentin, S-Ketamin, Clonidin, PCA-morfin eller epiduralanalgesi
- Opioid-rotation kan forsøges ved behandling af mere end 7 døgns varighed med brat stigende opioid behov (kirurgisk årsag udelukket).
- Aftrapning af opioider og Clonidin skal ske gradvist af hensyn til risikoen for abstinenser (se ovenfor)
Anbefalet dosering – Sedativa og Smertebehandling
| Sedativa | Dosering (start) | Farmakodynamik | Kommentar |
| Dexmede-tomidin | Bolus undgås
Startdosis = 1,5 mg/kg/t Infusion 0,2 – 2,0 mg/kg/t Pn. Fentanyl bolus initialt til ønsket Dexmedetomidin effekt er opnået |
Effekt efter 5-10 min
Varighed dosis afhængig 60-120 min |
Mindre egnet til dyb sedation
Bradykardi risiko Bevaret egen-respiration |
| Midazolam | Bolus 0,05 – 0,2 mg/kg
Infusion 0,1-0,5 mg/kg/time |
Effekt efter 2-5 min (iv)
Varighed < 2 timer (bolus) |
Lever- og nyresvigt forlænger effekten
Flumazenil er antidot |
| Propofol | Bolus 1-2 mg/kg
Infusion 1-4 mg/kg/time (max 4 mg/kg/time, < 48 timer) |
Effekt efter 30-60 sek.
Varighed 3-10 min |
Propofol-related infusion syndrome, ses ved højere doser og længere brug – se tekst
Risiko for apnø, hypotension, hypertriglyceridæmi, smerter ved infusion |
| Clonidin | PO: 2-4 mg/kg x 4-6 dgl. IV: 2-4 mg/kg x 4-6 dgl. (max 100 mg/dosis)Infusion 0,2 – 2 mg/kg/t |
Effekt efter 30-60 min (po)
Varighed 6-10 timer |
Peroral administration foretrækkes såfremt muligt.
Obs iv skal gives langsomt pga. risiko for bradykardi Skal ikke gives ved samtidig Dexmedetomidin infusion Let analgesi effekt |
| Kloralhydrat | PO: 20 mg/kg x 2-4/døgn
Max 1000 mg/døgn |
Let sedation eller som tilføjelse ved det urolige barn. Meget beskeden respirationsdæmpende effekt. |
| Analgetika (opioider) | Dosering (start) | Farmakodynamik | Kommentar |
| Morfin | PO: 0,2-0,5 mg/kg, hver 4. time
IV: 0,05-0,2 mg/kg Infusion: 0,02 – 0,3 mg/kg/t |
Effekt efter 30-60 min (po), 5-10 min (iv)
Varighed 3-5 timer |
Bør ikke anvendes ved svær nyresvigt
Giv altid samtidig laksantia |
| Oxynorm | PO: 0,2-0,5 mg/kg, hver 4. time
IV: 0,05 – 0,2 mg/kg Infusion: 0,01 – 0,05 mg/kg/t |
Effekt efter 30-60 min (po), 5-10 min (iv)
Varighed 3-5 timer |
Alternativ til morfin (1. Valg) ved nyreinsufficiens. |
| Alfentanil | IV: 10 – 20 mg/kg/dosis
Vedl.hold pn. hver 5-20 min |
Effekt efter 2-3 min
Varighed 30-60 min |
Ved korte procedurer, OBS: resp. dæmpning, hypo-/hypertension, rigid chestwall, bradykardi, ICP stigning |
| Fentanyl | Bolus 1 – 2 mg/kg
Infusion 2 mg/kg/time |
Effekt efter 2-3 min
Varighed 30-60 min |
Påvirker kredsløbet mindre end morfin og remifentanil |
| Remifentanil | Infusion 3 mg/kg/time (3 – 12) mg/kg/time |
Effekt efter 1-3 min
Varighed 3-10 min |
Clearance uafhængig af nyre- og leverfunktion
Kan give bradykardi og hypotension |
| Analgetika (non-opioid) |
Dosering (start) | Farmakodynamik | Kommentar |
| Paracetamol | Po: 10-15 mg/kg/dosis
hver 4.-6 time
Iv (Børn < 2 år): (max dosis 60 mg/kg/dag)
Iv (Børn > 2 år) 15 mg/kg/dosis, hver 6.time max 750 mg/dosis (< 50 kg) max 1000mg/dosis (> 50 kg) |
Effekt < 1 time (po) Effekt < 5-10 min (iv)Varighed 4 – 6 timerAbsorption fra tyndtarm (oral adm) Hepatisk elimination |
1. valg mod lette smerter, postoperative smerter, feber
Cave svær leversvigt-/ intoksikation. NAC-infusion ved forgiftning.
|
| Ketorolac | Iv Børn > 6 mdr. < 2 år:
0,25 – 0,50 mg/kg/dosis Iv Børn > 2 år:
|
Effekt < 30 minutter
Varighed 4 – 6 timer
Hepatisk elimination |
Post operative smerter
Max 2-3 døgns varighed Cave nyreinsufficiens, Hydrering vigtig |
| Gabapentin | Po: (børn > 3 år < 12 år) Dag 1: 5 mg/kg/dosis, (max 300 mg nocte) Dag 2: Øges til x 2 dgl (max 300 mg x 2 dgl) Dag 3: Øges til x 3 dgl (max 300 mg x 3 dgl)Po: Børn > 12 år, samme dosis som voksne |
Effekt < 2 – 3 timer
Varighed 5-9 timer
Metaboliseres ikke |
Neuropatiske smerter
Dosisjustering v nyreinsufficiens Mange interaktioner |
| S-Ketamin | Iv: 0,5 – 1 mg/kg (procedurer)Infusion 0,5 – 2 mg/kg/t svt 0,25 – 1,25 ml/kg/t (koncentration 2 mg/ml) |
Effekt efter 1-2 minutter
Varighed 1-3 timer |
Til korte smertefulde procedurer Bevaret egenrespiration Status astmaticus, refraktær status epilepticusSuppleres med benzodiazepin ved længerevarende infusion.OBS: Hallucinationer, øget spytsekretion, risiko for larynxspasmer, takykardi. Forsigtighed ved:Svær hjerteinkompensation Muligvis ved: højt ICP-/-okulært tryk |
Referencer:
- Playfor S. Analgesia and sedation in critically ill children. Contin Educ Anaesthesia, Crit Care Pain. 2008;8(3):90-94. doi:10.1093/bjaceaccp/mkn011
- Johnson PN, Miller JL, Hagemann TM. Sedation and analgesia in critically Ill children. AACN Adv Crit Care. 2012;23(4):415-434. doi:10.1097/NCI.0b013e31826b4dea
- Smith et al. 2022 Society of Critical Care Medicine Clinical Practice Guidelines on Prevention and Management of Pain, Agitation, Neuromuscular Blockade, and Delirium in Critically Ill Pediatric Patients With Consideration of the ICU Environment and Early Mobility, Ped Crit Care Med 2022 Feb;23(2):e74-e110
- Vet NJ, Ista E, de Wildt SN, van Dijk M, Tibboel D, de Hoog M. Optimal sedation in pediatric intensive care patients: a systematic review. Intensive Care Med. 2013;39(9):1524-1534. http://eutils.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&id=23778830&retmode=ref&cmd=prlinks
- Hemphill S, McMenamin L, Bellamy MC, Hopkins PM. Propofol infusion syndrome: a structured literature review and analysis of published case reports. Br J Anaesth. 2019;122(4):448-459. doi:10.1016/j.bja.2018.12.025
- UpToDate ”Initiating Mechanical Ventilation – Sedation and Analgesia”
- ”Drugdoses” Frank Shann´s 17th edition, Database update April 2022
- NBV fra Videnscenter for Børnesmerter, DASAIM, DPS og Dansk Selskab for Akutmedicin vedr Akutte smerter hos børn og unge https://paediatri.dk/images/dokumenter/retningslinjer_2024/National_vejledning_Akutte_smerter_hos_b%C3%B8rn_revision_04.10._2024.pdf
Kapitel 2 – Pædiatrisk delirium (PD)
| · Pædiatrisk delir er associeret med længere indlæggelse på ITA, større morbiditet og større omkostninger
· Pædiatrisk delir er oftest hypoaktivt og derfor svært at erkende · Det anbefales stærkt at screene systematisk for tilstanden · Sanér årsager til delir fx ved brug af huskehjælpen BRAIN MAPS, se senere · Brug altid non-farmakologiske tiltag, se senere · Ved brug af farmakologiske tiltag skal effekten vurderes løbende |
Definition og inddeling
Pædiatrisk delirium er defineret ved akut cerebral dysfunktion. Børns symptomer ligner voksnes med døgnrytmeforstyrrelser, konfusion, uopmærksomhed, hallucinationer, angst og adfærdsændringer. Manifestationen af delir vil også være afhængigt af barnets alder der er ganske forskellige i spændet fra 0 til 18 år
| DSM-5 (Diagnostic and Statistical Manual of the American Psychiatric Association) kriterierne for delir er: | |
| 1 | Evnen til at fastholde eller ændre opmærksomheden er påvirket |
| 2 | Tilstanden fluktuerer i både tid og intensitet. Den udvikler sig over kortere tid (timer til dage) og er en akut ændringen af barnets grundlæggende opmærksomhedsniveau. |
| 3 | Kognitionspåvirkning i form af desorientering, påvirket hukommelse, sprog eller visuospatial opfattelse |
| 4 | Symptomer under 1 og 3 skyldes ikke en underliggende neuropsykologisk tilstand og skyldes ikke tung sedation |
| 5 | Der er klinisk evidens for, at tilstanden er en direkte fysiologisk konsekvens af sygdomstilstand |
Pædiatrisk delir kategoriseres i tre subgrupper
• Hyperaktivt delirium
En særlig type af det hyperaktive delir er det såkaldte emergence delir; også kaldet opvågningsdelir
• Hypoaktivt delirium
• Blandet delirium
Hos børn ses hyppigst det hypoaktive og det blandede delir, om end det hyperaktive delir opdages lettere. Delir er hyppigst hos yngre børn.
Forekomst og betydning
Forekomsten af pædiatrisk delir er angivet med svingende prævalens fra 4 til 56%. Pædiatrisk delir er associeret med forlænget indlæggelsestid, flere dage i respirator og muligvis langtidseffekter i form af udvikling af posttraumatisk stress. Årsagen til delir er delvist ukendt og pædiatrisk delir kan ligne og have overlappende udløsende årsager med abstinenstilstande og smerter (se figur 1).

Figur 1
Årsager/ risikofaktorer
- Non-modificerbare: Prædisponerende faktorer hos barnet i form af genetisk disposition, kognitive begrænsninger og depression
- Modificerbare: Sygdomsrelaterede faktorer: Shock, sepsis, elektrolytforstyrrelse anæmi m.fl.
- Iatrogene faktorer: Sedation, immobilisering, insufficient analgesi, vaskulære katetre, manglende forebyggende tiltag
Diagnostik og screening
Der findes forskellige værktøjer til diagnostik af og screening for PD. Det vigtigste er, at afdelingen bruger et værktøj og gerne det samme, samt at personalet kan bruge det korrekt og systematisk. Delirium er en fluktuerede tilstand, hvorfor det anbefales at screene rutinemæssigt mindst hver 8. time.
Screening af barnet kræver desuden, at barnet er vågent nok, hvorfor sedationsniveauet først bør afklares ved hjælp af f.eks Comfort-B, RASS (Richmond Agitation Sedation Score) eller SBS (State Behavioral Scale)
Det anbefales stærkt fast at anvende et redskab, som afdelingen er bekendt med.
Følgende validerede redskaber findes:
- pCAM-ICU (over 5 år)
- psCAM-ICU (6 mdr. til 5 år)
- CAPD (Cornell Assessment Score) (0-21 år)
- SOS-PD (Sophia Observational Withdrawal Symptoms -Pediatric Delirium), (3 mdr. til 21 år, skelner mellem abstinenser og delir)
Stilles diagnosen delirium skal mulige årsager til delir overvejes. Akronymet BRAINMAPS er et redskab brugt i internationale sammenhænge til gennemgå mulige behandlelige årsager til delir.
| Brain Maps | |
| B | Bring Oxygen |
| R | Remove or Reduce drugs that are delirogenic (i.e. anticholinergics, benzodiazepines) |
| A | Patient Atmosphere (i.e. lights, noise, family presence, non-mobility) |
| I | Immobilization, Inflammation, Infection |
| N | New organ dysfunktion or failure |
| M | Metabolic disturbances (i.e. ↑↓Na, ↑↓K, ↓Ca, alkalose, acidose) |
| A | Awake (i.e. sleep-wake cycle disturbance prior to procedure). Anxiety |
| P | Pain (i.e. not enough analgesia OR pain treated and now excessive drug dosing |
| S | Sedation (i.e. residual anaesthesia, ongoing sedation for perceived agitation or anxiety) |
Tabel 5
Tester et barn positiv for delir i et af screeningsredskaberne, mens det samtidig vurderes, at barnet ikke er delirøst, bør forskellige differentialdiagnoser overvejes som f.eks. NMDA encefalitis.
Mistænkes kramper bør der foretages EEG. Hvis indiceret, overvej MR- eller CT cerebrum.
Flow chart over behandlings og screeningsstrategi ved Pædiatrisk delir

Figur 2 Flowchart over behandlings- og screeningsstrategi ved Pædiatrisk delir.
Behandlingsstrategi
Overordnet set anbefales det så vidt muligt kun at anvende nonfarmakologiske tiltag og ikke anvende farmakologisk behandling systematisk, men kun efter vurderet behov.
Pædiatrisk delir kan i nogen grad forebygges ved hjælp af forskellige strategier.
Non-farmakologisk behandling
- Faste skemalagte rutiner
- Søvnhygiejne. Mindst 5-6 timers uafbrudt nattesøvn og aldersvarende lur om dagen
- Skærmning for lys og lyd (alarmer!)
- Hjemlig atmosfære (billeder, legetøj etc.)
- Daglig orientering (aldersafhængigt) i tid og sted
- Anvend briller og høreapparater hvis barnet normalt bruger det
- Brug af fast plejepersonale
- Minimering af fastholdelse
- Inddragelse af forældre i den daglige pleje
- Daglig vurdering af behov for respirator og adgange
- Tidlig mobilisering
Farmakologisk behandling
Farmakologisk behandling er en undtagelse og overvejes først, når non-farmakologiske tiltag er utilstrækkelige f.eks. hvor:
- Patienter der er i fare for sig selv eller andre
- Patienter hvor delirium forhindrer sufficient diagnostik og behandling
- Patienter der er forpint af f.eks. hallucinationer og vrangforestillinger
- Terminale patienter i de sidste dage/timer
Non-farmakologiske tiltag skal fastholdes ved tillæg af farmakologisk behandling. Der bør dagligt tages stilling til, om medicinsk behandling forsat er indiceret, bør udelukkende hvile på ovenstående 4 grunde og ikke på diagnosen delir i sig selv.
I Danmark er det eneste godkendte lægemiddel til behandling af voksne med delirium Haloperidol. Der er ingen anbefalinger for børn. Haloperidol bruges i Danmark på anden indikation til børn fra 6 år, men brug under denne alder frarådes af Lægemiddelstyrelsen. Der er ingen Food and Drug Agency godkendte lægemidler til behandling af delir; hverken hos børn eller voksne.
Det anbefales at involvere en børnepsykiater ved behov for farmakologisk behandling.
Præparatvalg
| Antipsykotika receptor farmakologi | |||
| Receptor | Receptoraffinitet | Klinisk effekt via receptor | Bivirkninger |
| Dopamine (D2) | Haloperidol ++++
Risperidon +++ Olanzapin ++ Quetiapin + |
Antipsykotisk effekt
Antihallucinatorisk effekt |
Extrapyramidale symptomer
Endokrine effekter: forhøjet prolactin og insulin secretion Arytmier Svækket kognition |
| Serotonin (5-HT2a) | Risperidon ++++
Olanzapin +++ Quetiapin ++ Haloperidol + |
Antipsykotisk effekt
Antihallucinatorisk effekt Bedret kognition Lindring af extrapyramidale symptomer |
Ukendt |
| Histamine (H1) | Olanzapin ++++
Quetiapin +++ Risperidon +++ Haloperidol 0 |
Sedation | Vægtøgning
Øget appetit |
| Muscarine (M1 and M3) | Olanzapin ++
Quetiapin + Risperidon 0 Haloperidol 0 |
Lindring af extrapyramidale symptomer | Anticholinerge effekter:
Urin retention Forstoppelse Mundtørhed Hukommelsesbesvær |
| Adrenergic (α1) | Risperidon +++
Quetiapin ++ Haloperidol ++ Olanzapin + |
Ukendt | Hypotension
Refleks takykardi |
Tabel 6
1. generations antipsykotika
Haloperidol
Haloperidol blokerer uselektivt dopamin D2 receptorer og udøver herved sin antipsykotiske effekt. Ved tiltagende blokering af D2 receptorer stiger risikoen for ekstrapyamidale bivirkninger samt en række andre alvorlige bivirkninger som forlænget QT og hyperinsulinæmi.
Det anbefales at starte i lavest mulige dosering i forhold til vægt og titrere op. Haloperidol anbefales generelt til hyperaktivt delir, hvor hallucinationer synes at være fremtrædende.
| Dosering af Haloperidol | |
| Loading | |
| Vægt 3,5 – 10 kg | 0,05 mg (ikke pr kg) givet langsomt over 30-45 min.
Kan gentages 2 gange til max 3 gange dagligt |
| Vægt > 10 kg | 0,15-0,25 mg (ikke pr kg) givet langsomt over 30-45 min.
Kan gentages 2 gange til max 3 gange dagligt |
| Vedligehold (det anbefales at starte i lavest mulige dosering i forhold til vægt og titrere op) | |
| Vægt 3,5 – 10 kg | Initielt 0,01-0,05 mg/kg/dag. Kan deles op i 1 – 4 doser dagligt |
| Vægt > 10 kg | Initielt 0,05-0,5 mg/kg/dag. Kan deles op i 1 – 4 doser dagligt |
Tabel 7
2. generations antipsykotika
Gruppen af 2. generations antipsykotika binder af varierende grad til D2 receptorer, serotonin 5 HT2a receptorer, H1 receptorer samt muscarine receptorer M1 og M2 samt adrenerge receptorer (α1). Varierende virkning og bivirkninger er et resultat af dette. En svagere binding til D2 receptoren gør, at ekstrapyramidale bivirkninger er mindre fremtrædende hos 2. generations antipsykotika.
Risperidon
Enteralt administreret anbefales til det hypoaktive og blandede Pædiatriske delir med en loading-dosis på 0,1-0,2 mg/kg/døgn og en vedligeholdelsesdosis på 0,2-2,0 mg/kg/døgn.
Dosisanbefaling
Olanzapin
Ved akut agitation 2,5 til 10 mg/dosis hver 2. til 4. time pn, Max samlet dosis 20 mg/døgn
| Quetiapin | |
| > 2 mdr. til 3 år | initielt 0,125 mg/kg/dosis x 1 dgl, + 0,1 – 1 mg pn p.o. Max samlet 0,5 mg/kg/døgn |
| > 3 år til < 6 år | fast 3 – 6,25 mg x 1 dgl, samt 3 – 6,25 mg pn hv 2 time til effekt, max samlet 25 mg/døgn |
| > 6 år til < 12 år | 12,5 mg x 1 dgl, samt 12,5 mg pn hver 2 time, max samlet 50 mg/døgn
|
| > 12 år | 25 mg x 1 dgl, samt 25 mg hver 2 time pn til effekt, max samlet 100 mg/døgn |
Tabel 8
Dexmedetomidin
En selektiv α2 adrenerg receptor agonist, der både har analgetisk og sedativ effekt. Ved hyperaktivt delir hos voksne bruges dexmedetomidin som adjuverende behandling hos non-respondere på Haloperidol. Stoffet bruges også effektivt til behandling af postoperativt delir (emercence delir) og kan administreres nasalt. Bør ikke benyttes hos hjertesyge børn.
Intravenøs infusion startes i øvre doseringsinterval, 1,2 – 1,4 μg/kg/time. Infusionen bør så vidt muligt reduceres i dagtid og øges om natten, med henblik på at tilstræbe en form for døgnrytme.
Referencer:
- Smith HAB, Besunder JB, Betters KA, Johnson PN, Srinivasan V, Stormorken A, et al. 2022 Society of Critical Care Medicine Clinical Practice Guidelines on Prevention and Management of Pain, Agitation, Neuromuscular Blockade, and Delirium in Critically Ill Pediatric Patients with Consideration of the ICU Environment and Early Mobility. Pediatric Critical Care Medicine [Internet]. 2022 Feb 1 [cited 2024 Jun 6];23(2):E74–110.
- Fuhrman & Zimmerman’s Pediatric Critical Care 5. Udgave. Elsevier 2017.
Kapitel 136 pp 4305-4320 - Capino AC, Thomas AN, Baylor S, Hughes KM, Miller JL, Johnson PN. Antipsychotic Use in the Prevention and Treatment of Intensive Care Unit Delirium in Pediatric Patients. The Journal of Pediatric Pharmacology and Therapeutics : JPPT [Internet]. 2020 [cited 2024 Jun 6];25(2):81. Available from: /pmc/articles/PMC7025750/
- ”Drugdoses” Frank Shann´s 17th edition, Database update April 2022
Kapitel 3 – Status epilepticus
| · Status epilepticus skal behandles aggressivt – time is brain
· Behandl med antiepileptisk medicin · Gennemgå ABCDE · Led efter udløsende årsager |
Behandling
Behandl kramper med antiepileptisk medicin efter 3 min. Start et stopur. I de 3 min og løbende derefter vurderes ABCDE. De fleste, især tidligere raske, børn med status epilepticus har dog ikke brug for andet ABC støtte end ilt-tilskud. Børn, der kræver intensiv behandling med antiepileptisk medicin, er derimod i risiko for ikke at kunne beskytte luftveje, hypoventilation, arytmier og hypotension.
Airway
Skab fri luftvej med fx sideleje, sugning, kæbeløft.
Intubation ved behov, fx langvarige kramper, respirationsdepression fra Midazolam infusion eller ved aspiration.
Breathing
Giv ilt, fx på maske. Maskeventilation ved behov.
Circulation
Vurder puls og BT. Anlæg i.v. adgang – overvej i.o. adgang tidligt og anlæg senest efter 30 min uden i.v. adgang.
Disability
Vurder krampetype – generaliseret eller fokal. Overvej PNES (psychogenic non epileptic seizures).
Mål blodsukker (gerne som syre/base evt. kapillær) og behandl BS < 4 mM/L med glukose 10%
3 ml/kg. Vurder tegn på hovedtraume og pupilforhold
Environment/exposure
Feber, petekkier. Ved feber og ved kramper over 30 min eller ved fokale kramper startes behandling for meningitis. Undersøg nuværende og tidligere medicinsk behandling og udspørg om barnet har fået sin medicin.
Undersøgelser
Blodsukker, syre/base, nyretal, levertal, calcium, magnesium, hæmoglobin, L+D, trombocytter, CRP, S-antiepileptika.
Overvej lumbalpunktur, men først i stabil fase, samt ammonium og tox-screening
Overvej CT skanning ved mistanke om rumopfyldende proces, fokale kramper, mistanke om øget ICP.
Ved behov for intubation og/eller hvis yderligere neuropædiatrisk assistance kræves, kontaktes lokale børnecenter mhp. stillingtagen til yderligere plan, herunder evt. lokal ekstubation eller overflytning til tertiær center. Undgå relaksering mhp monitorering af krampetilstand og særlig opmærksomhed på risiko for sedationsudløst hypotension.
Flowchart til behandling af Status epilepticus

Figur 3 Flowchart til behandling af status epilepticus hos børn > 1 måned
Antiepileptika
Diazepam / Midazolam buccalt (Buccolam) / Midazolam iv
Kan især til de små under 6 mdr. være respirationsdæmpende. Såfremt barnet allerede er i fast behandling med benzodiazepimer, f.eks. Rivotril eller Frisium, kan suppleres med Kloralhydrat rektalt, 500 mg < 5 år, 1 gram 5 – 10 år, 2 gram > 10 år.
Valproat (Orfiril)
Valproat fås som iv. medikament (Orfiril injektionsopløsning med 3 mL ampuller, der indeholder 300 mg natriumvalproat). Dosis er 40 mg Valproat/kg. Injiceres over 5-10 min. Virkningen ses efter 1 – 5 min. Må ikke bruges hos børn med kendt leversygdom eller mistanke om neurometabolisk / mitokondrie sygdom. Der er kun behov for at måle serum Valproat og vanlige følgeprøver hvis der vælges at give vedligeholdelsesbehandling.
Levetiracetam (Keppra/Kevesy)
Dosis er 60 mg/kg givet som rolig bolus over 5 -10 min, maks. enkeldosis 3500 mg, maks. koncentration 15 mg/ml. Levetiracetam/Keppra/Kevesy findes i præfabrikerede blandinger i dosis 5 og 10 mg/ml (Kevesy). Hvis der anvendes hætteglas Keppra er der 500 mg i et hætteglas (5 ml á 100 mg/ml), som skal fortyndes til en koncentration på max 15 mg/ml. 1 hætteglas 500 mg (5 ml) tilsættes 28 ml, 2 hætteglas 1000 mg (10 ml) tilsættes 56 ml og 3 hætteglas (15 ml) tilsættes 85 ml isotonisk glukose eller NaCl. Stoffet har ingen kendte interaktioner. Hvis der vælges vedligeholdelsesbehandling gives 15-20 mg/kg x 2 dagligt enten iv. eller p.o.
Midazolam kontinuerlig infusion
Midazolam gives som bolus 0,2 mg/kg iv, efterfulgt af infusion 0,1 mg/kg/time op til max 2 mg/kg/time. Bolus kan gentages hver 5.-10. minut, med optrapning af infusion til effekt eller max 2 mg/kg/time Der er risiko for respirationsdepression og hypotension. Omkring 15% af børnene kræver ventilation i respirator ved maximal dosis. Kontinuerlig Midazolam infusion og gentagen bolus skal foregå på afdeling med mulighed for intensiv behandling i samarbejde med anæstesipersonale. Aftrapning kan foregå med 0,05 mg/kg/time hver 3. time, typisk efter 1 døgns anfaldsfrihed.
Phosphenytoin (Pro-Epanutin)
Må kun gives til børn og unge over 5 år med mindre særlige forhold er gældende. Der er indsat doseringsskema for Pro-Epanutin som bilag sidst i dokumentet. Der er risiko for arytmi og hypotension (Ekg og blodtryk bør monitoreres ved intensiv observation under indgift og frem til 20 min. efter indgift). Til forskel fra Phenytoin giver Phosphenytoin ikke vævsnekrose og kan gives hurtigere. Virkningen indsætter imidlertid ikke hurtigere, idet Phosphenytoin først i kroppen skal omsættes til Phenytoin. Man regner med, at Phenytoin bør virke efter 15 minutter efter indgift. Phosphenytoin kan også gives i.m., men virker da først efter 30 min. Dosis er den samme. Pro-Epanutin udskrives i PÆ (Phenytoin Ækvivalenter), således at 1,5 mg Phosphenytoin = 1 mg PÆ. Pro-Epanutin (50 mg PÆ/ml) fortyndes med lige dele NaCl (0,9 %) eller glukose (5%). Opløsningen, der nu er på 25 mg PÆ/ml bruges til injektion. Dosis gives som bolus over 5-7 min. Se-Phenytoin måles 1–2 timer efter indgift akut (Foretages akut efter tlf. aftale med nogle klinisk biokemiske afdelinger). Hvis værdien ligger i niveau (40 – 80 mikromol/L) gives intet ekstra. Ved lavere værdier gives 5 mg PÆ/kg ekstra iv. Hvis Phosphenytoin fortsættes, gives næste dosis 8–10 timer senere og derefter hver 12. time (spædbørn dog efter 8 timer). Vedligeholdelsesdosis er 6–8 mg PÆ/kg/døgn for børn < 2 år og 5–6 mg PÆ/kg/døgn for større børn. Dosis i øvrigt afhænger af se-Phenytoin, som bør måles dagligt, så længe der gives iv. medicin. Dosis er den samme, når man overgår til Phenytoin p.o.
Fenemal
Bolusdosis er 20 mg/kg iv. Injiceres over 10 min. Effekt kan ikke forventes før ca. 20 min. efter infusion er givet. Ved fortsat behandling gives næste dosis (2 – 4 mg/kg) 8 timer senere og derefter hver 12. time. Daglige se-Fenemal målinger er nødvendige i starten.
Lacosamid
Har vist sig at have gunstig effekt ved behandlingsrefraktær status epilepticus. Dosis i.v. 6 mg/kg, max enkeltdosis 400 mg som mætningsdosis, efterfulgt af vedligeholdelsesdosis på 6 mg/kg/døgn. Gives over 15 til 60 min. Kan gives uden yderligere fortynding eller kan fortyndes med Natriumclorid 9 mg/ml (0,9 %), glukose 50 mg/ml (5%) eller Ringer-Lactat.
Øvrige særlige tilfælde
I.m. Midazolam og Pro-Epanutin kan gives ved manglende i.v. / i.o. adgang (samme dosis som i.v.)
Kloralhydrat rektalt kan også være et alternativ: 500 mg < 5 år, 1 gram 5 – 10 år, 2 gram > 10 år. Kloralhydrat er et gammelt, men effektivt præparat, der ofte virker synergistisk med Diazepam. Optages i løbet af få minutter efter rektal administration.
Pyridoxin
Overvej hos børn under 2 år med kramper af ukendt ætiologi. Dosis er 100 mg iv og, hvis der ikke er effekt, gentages dette op til en dosis på 300 mg. Der fortsættes med 30 mg/kg/dag i 3 doser 3-5 dage. Herefter evt. PLP oralt (pyridoxal 5’-phosphat) 30-60 mg/kg/dag i 4-6 daglige doser i 3 dage.
Superrefraktær status epilepticus:
Overvej overflytning til sygehus med mulighed for kontinuerlig EEG-monitorering. Der stiles efter sedation til EEGgrafisk anfaldsophør. Ketogen diæt eller epilepsikirurgi kan have en plads i håndteringen.
Ved manglende anfaldskontrol under midazolam infusion er evidensen for videre anbefalinger lav. Konferér med børneneurolog, neurofysiolog og/eller neurointensivist.
Overvej at stoppe midazolam, fortsæt vanlig antiepileptisk medicin og vælg én af nedenstående:
| Ketamin infusion
Anbefalet ved cirkulatorisk instabilitet |
2-3 mg/kg bolus efterfulgt af infusion 10 mg/kg/min (0,6 mg/kg/time). Kan øges med 5 mg/kg/min (0,3 mg/kg/time) hver 10. minut til effekt. Max infusionshastighed 100 mg/kg/min (6 mg/kg/time) |
| Aftrapning | Når der ingen anfald er i 24 timer aftrappes med 5 mg/kg/minut hver time. Overvej at opstarte midazolam 1-2 mg/kg/min for at undgå delir. Ved genkomst af anfald, optrappes til virkning og afventes 48 timer før nyt forsøg |
| Propofol infusion
Kontraindiceret hos børn på ketogen diæt og børn med mitochondriesygdom |
1-2 mg/kg bolus efterfulgt af infusion 1-2 mg/kg/time. Kan øges med 0,3 mg/kg/time hver 10. minut til effekt. Max infusionshastighed: 4 mg/kg/time. Max behandlingsvarighed 48 timer. Hold øje med PRIS |
| Aftrapning | Når der ingen anfald er i 24 timer aftrappes med 0,3 mg/kg/time hver time. |
| Phenobarbital som boli | 20 mg/kg bolus over 10 minutter
Gentag bolus på 10 mg/kg hver 30. til 60. minut til effekt. Mål s-Phenobarbital dagligt. Serum-værdier over 500 mikromol/L vil kræve doser på 15 mg/kg/døgn fordelt på 4-6 doser. |
| Aftrapning | Når der ingen anfald er i 24 timer aftrappes med 25 % per dag. Ved genkomst af anfald, genoptages boli til virkning og afventes 48 timer før nyt forsøg |
Tabel 9
Hvis der ikke er effekt trods maksimalt tolereret dosis af en af strategierne, prøves en anden. Ketamin og Propofol vil kunne kombineres før Phenobarbital evt. forsøges.
Hyppige årsager til status epilepticus
| Ikke kendt med epilepsi | Kendt med epilepsi | |
| Børn | Feberkramper | |
| Børn og unge | Neuroinfektion eller neuroinflammation ex ADEM
Strukturel CNS læsion Metabolisk (især hypoglykæmi) Elektrolytforstyrrelser Uræmi Forgiftninger |
Non-compliance / behandlingssvigt
Systemisk infektion |
| Især unge | Abstinens |
Tabel 10 Hyppige årsager til status epilepticus
Definitioner
Status epilepticus
En tilstand med epileptiske anfald af abnorm lang varighed, som efter et tidsrum medfører risiko for permanent cerebral skade.
Konvulsivt status epilepticus
Langvarigt bilateralt (generaliseret) tonisk-klonisk anfald > 5 min. eller gentagne bilaterale (generaliserede) tonisk-kloniske anfald, hvor patienten ikke genvinder fuld bevidsthed imellem anfaldene.
Refraktær status epilepticus
Status epilepticus, som fortsætter trods brug af benzodiazepin og et i.v. antiepileptikum.
Superrefraktær status epilepticus
Status epilepticus, som fortsætter/recidiverer mindst 24 timer, efter at generel anæstesi er påbegyndt.
Nedenstående anfaldstyper bliver ikke berørt i denne vejledning
Non-konvulsivt status epilepticus
Andre former for status epilepticus fx myoklon status epilepticus eller fokal motorisk status epilepticus uden bevidsthedspåvirkning (epilepsia partialis continua).
Referencer:
- Status epilepticus børn > 1 md revideret 2023 på https://paediatri.dk/dps-vejninger-mm eller https://paediatri.dk/neurologi-vejl
- AES: Evidence-based guideline – Treatment of convulsive status epilepticus in children and adults(2016)
Kapitel 4 – Neuroprotektion
Traumatisk hjerneskade er den hyppigste årsag til forhøjet intrakranielt tryk (ICP) og medvirkende til betydende mortalitet og morbiditet hos børn. Også CNS-infektioner, spontane intrakranielle blødninger, cerebrale infarkter herunder sinustrombose, cerebral hypoxi, hydrocephalus og cerebrale tumorer kan give anledning til forhøjet intrakranielt tryk. Grænsen for forhøjet intrakranielt tryk er fortsat defineret ved værdier > 20 cmH2O hos voksne, men er aldersafhængigt lavere for mindre børn, svt:
| Alder, år | ICP, mmHg |
| 0-5 | ≤15 |
| 6-17 | <16-19 |
| >17 | ≤20 |
Let forhøjede værdier tåles i relativt længere tid, mens moderat og svært forhøjede værdier tåles i betydeligt kortere tid. Desuden har varigheden af forhøjet ICP betydning; den såkaldte ”ICP dose”.
Forhøjet intrakranielt tryk er en tidskritisk tilstand og akut intervention afgørende. Kompensatoriske mekanismer som displacering af cerebrospinalvæske opretholder det intrakranielle tryk relativt konstant, men ved akut indsættende øget cerebralt volumen, eksempelvis som følge af traumatisk hjerneblødning, vil de vanlige adaptive mekanismer ikke være nok, og perfusionen af hjernen vil kompromitteres. Herudover kan dannelse af intrakranielle trykgradienter føre til forskydning og mekanisk skade af hjernevævet, fx ved herniering under falx, langs tentorium eller gennem foramen magnum.
Det intrakranielle volumen består af hjernevæv, cerebrospinal væske (CSV), samt blod, hvoraf sidstnævnte kan inddeles i det venøse -og det arterielle blodvolumen. CSV produceres konstant med en hastighed på 0,35 ml/min hos både børn og voksne. Inddelingen i venøst og arterielt blodvolumen er vigtig, da disse volumina kan reduceres ved forskellige behandlingstiltag. Når kraniet betragtes som en lukket kasse, vil enhver volumenforøgelse give anledning til forhøjet ICP, hvilket kan illustreres ved Monro-Kelli doktrinen:
VolTotal = VolVeneblod + VolArterieblod + VolHjernevæv + VolCSV + VolPatologisk = Konstant

Billede 1
Så længe fontanellerne er åbne, er kraniet lettere eftergiveligt. Det forklarer, hvorfor nyfødte kan tolerere større patologiske volumina bedre end større børn, om end akutte ændringer i volumen sagtens kan give ICP-stigninger pga. dura maters lave elasticitet. Klinisk giver en frembulende eller spændt fontanelle mistanke om forhøjet intrakranielt tryk.
I takt med ossifikation og lukningen af fontanellerne, bliver kraniet ueftergiveligt. Det medfører, at det samlede intrakranielle volumen bliver konstant. Enhver volumenforøgelse vil derfor medføre stigende intrakranielt tryk. Der findes en del adaptive mekanismer, som alle er tidsafhængige. Det indebærer, at akut volumenforøgelse tolereres mindre godt med akut stigende ICP til følge; illustreret ved nedenstående tryk-volumen-kurve:

Billede 2 tryk-volumen-kurve
Hjernens stofskifte er aldersafhængig, og har den største energiomsætning i alderen 3-12 år. Langt størstedelen af hjernens stofskifte (omkring 97%) sker ved oxidativ forbrænding af glukose, og hjernen er således afhængig af en konstant tilførsel af glukose.
Hjernens gennemblødning er nøje reguleret gennem hele opvæksten og i voksenalderen. Det cerebrale blood flow (CBF) er, hos den neonatale og præmature, 0,25 ml/g/minut. Ved 6 måneders alderen har barnet samme blood flow som voksne (0,5 ml/g/minut) og er stigende indtil 5 års alderen hvor blood flowet når 0,9 ml/g/minut.
Blodets strømningshastighed varierer ligeledes gennem opvæksten og kan visualiseres med ultralyd ved hjælp af transcraniel doppler (TCD), dog med en betydelig interobservatør forskel. Inden for det 1. leveår varierer strømningshastigheden mellem 40 cm/sekund og 75-100 cm/sekund, hvorefter det falder til cirka 50 cm/sekund, som er normalværdien hos voksne raske personer.
Hjernens autoregulation har til formål at opretholde CBF trods ændringer i hjernens perfusionstryk (CPP). CPP er defineret ved middelarterietrykket (MAP) – det intrakranielle tryk (ICP).
Hjernens stofskifte er aldersafhængig, og har den største energiomsætning i alderen 3-12 år. Langt størstedelen af hjernens stofskifte (omkring 97%) sker ved oxidativ forbrænding af glukose, og hjernen er således afhængig af en konstant tilførsel af glukose.
Hjernens gennemblødning er nøje reguleret gennem hele opvæksten og i voksenalderen. Det cerebrale blood flow (CBF) er, hos den neonatale og præmature, 0,25 ml/g/minut. Ved 6 måneders alderen har barnet samme blood flow som voksne (0,5 ml/g/minut) og er stigende indtil 5 års alderen hvor blood flowet når 0,9 ml/g/minut.
Blodets strømningshastighed varierer ligeledes gennem opvæksten og kan visualiseres med ultralyd ved hjælp af transcraniel doppler (TCD), dog med en betydelig interobservatør forskel. Inden for det 1. leveår varierer strømningshastigheden mellem 40 cm/sekund og 75-100 cm/sekund, hvorefter det falder til cirka 50 cm/sekund, som er normalværdien hos voksne raske personer.
Hjernens autoregulation har til formål at opretholde CBF trods ændringer i hjernens perfusionstryk (CPP). CPP er defineret ved middelarterietrykket (MAP) – det intrakranielle tryk (ICP).
Autoregulationen opretholder normalt CBF ved MAP 60-160 mmHg. Ved lavere værdier kan der opstå hypoxi og iskæmi. Ved højere værdier kan arteriolerne ikke modstå det høje tryk, hvilket kan medføre cerebralt ødem. Hjernens autoregulation er ikke helt klarlagt hos børn, men noget tyder på, at den fungerer inden for samme interval som voksnes.
Det normale ICP hos børn i hvile og liggende stilling er 5-10 mm Hg. Vedvarende værdier over 15 mm Hg er patologiske.
Hvornår skal man mistænke forhøjet intrakraniel tryk
Ved relevant hovedtraume og bevidsthedspåvirkning, men selv uden traume kan ses forhøjet ICP hos det bevidsthedspåvirkede barn, fx ved spontan intrakranial haemorrhagi mm. Ensidig eller bilateral pupildilatation med manglende lysreaktion er en vigtig indikator. Det er vigtigt at notere eventuelle neurologiske deficits.
Vurdering af GCS er afgørende, og der anvendes en modificeret Glasgow Coma Skala målrettet pædiatriske patienter:

Billede 3 Pediatric Glasgow Coma Scale
Behandling
Behandlingen kan inddeles i tiden før ICP kendes, og frem til ICP måles og barnet er indlagt på intensiv afdeling.
I alle faser af behandlingen er de medicinske behandlingsmodaliteter de samme, men i takt med den invasive monitorering, kan behandlingen – og effekten – i højere grad titreres til ønsket effekt.
I alle aspekter af behandlingen er det vigtigste at undgå hypotension og hypoxi, da disse med størst sikkerhed er vist af have betydning for mortalitet og morbiditet.
I den initiale fase frem til neurokirurgisk intervention kendes ICP ikke, men antages højt. Den neuroprotektive behandling kan simplificeres ved en vanlig ABC-tilgang med særligt fokus på interventioner, der nedsætter ICP. Det er vigtigt at have fokus på tidsfaktoren frem til neurokirurgisk behandling.
Behandling før ICP kendes
- A:
Intubation indiceret ved: GCS under 9, hastigt descenderende patient og/eller lang kørevej. Ved traume, obs. på spinal stabilisering ved intubation. Altid modificeret akut indledning mhp. PaCO2 lav i normalområdet – anvend muskelrelaksantia.
- B:
Oxygenering: Tilstræb PaO2 10-12/SpO2 94-98%, PEEP titreret til lavest mulige værdier over 5.
Ventilation: TV og RF titreret til EtCO2 4,5-5,5.
- C:
Sikre sufficient cerebral perfusion: BT-mål:
| Alder, år | MAP, mmHg |
| 0-5 | ≥ 55-60 |
| 6-17 | ≥ 70 |
| >17 | ≥ 80 |
Invasiv BT-monitorering etableres såfremt det ikke forsinker evt. transport/kirurgi.
- D:
Optimere det venøse tilbageløb: Let eleveret hovedgærde 15-30 grader og hovedet i neutral position.
Osmotisk behandling ved mistanke om forhøjet ICP: Hyperton NaCl: 1 mmol/kg ved GCS < 14. Hvis GCS < 9 eller dilaterede pupiller gives 2 mmol/kg.
Sænke den cerebrale metabolisme: Dyb anæstesi, relaksation.
Ved Traumatisk brain injury (TBI): Tranexamsyre 10 mg/kg (max 1 g) ved GCS 9-13. Øges til 20 mg/kg (max 2 g) ved GCS < 9. Blodsukker i normalområdet.
- E:
Normotermi.
Når ovenstående er effektueret, foretages hyppig revurdering af vitalværdier og pupilforhold, og transport til hospital med neurokirugisk kompentence iværksættes forudgået af telefonisk konference.
Neurokirurgiske interventioner, der akut sænker det intrakranielle tryk, inkluderer eksempelvis akut kraniotomi med evakuering af hæmatom, anlæggelse af eksternt ventrikeldræn (EVD) og kraniektomi, hvor en større del af kraniepladen fjernes, for siden at kunne re-placeres. Ved sidstnævnte strategi fjernes den lukkede kraniekasse hvorved Monro-Kellie-doktrinen ophæves.
Kirurgi har til formål at opnå ICP-kontrol, men udelukker ikke efterfølgende ICP-stigning, og tæt monitorering af ICP er ofte indiceret i det post-operative forløb på intensiv afdeling. Monitorering kan ske ved anlæggelse af en ICP monitor, via et EVD eller anden avanceret multimodal neuromonitorering. I nogle tilfælde fravælges ICP-monitorering af neurokirurger, og i så tilfælde er klinisk overvågning af bevidsthedsniveau og pupilforhold vigtig, og kontrol af intrakranielle forhold er ofte nødvendig i form af billeddiagnostik.
Når ICP kendes på PICU patienter:
- A:
Ved forventet længerevarende intensivt forløb, bør omlægning til nasal intubation (obs basis fraktur)/tracheotomi overvejes, når ICP stabilitet er opnået.
- B: Oxygenering: Tilstræb PaO2 10-12/SpO2 94-98%, PEEP titreret til lavest mulige værdier over 5. Ventilation når ICP-labil: Kontrolleret ventilation mhp. konstant EtCO2.
- C: Sikre sufficient cerebral perfusion: CPP-mål, NB: 0-punkt svt. meatus acusticus eksternus.
| Alder, år | CPP, mmHg |
| 0-5 | ≥ 40 |
| 6-17 | ≥ 50 |
| >17 | ≥ 60 |
CPP værdier under 40 mmHg er med sikkerhed korreleret til øget mortalitet og morbiditet, så anførte værdier er minimum grænseværdier.
Noradrenalin-infusion er 1. valg
Hgb-mål: > 5,6 mmol/L
- D: Optimere det venøse tilbageløb: Let eleveret hovedgærde 15-30 grader og hovedet i neutral position. Osmotisk behandling: Hyperton NaCl (HTN) i koncentration 1 mmol/ml er standard. Kan gives som infusion eller som bolus. Som infusion tilstræbes 0,2-2 ml/kg/time.E:Normotermi på PICU ptt.Tromboseprofylakse.Opstart tidlig enteral ernæring + laksantia.
Behandlingsmål: Den laveste værdi over normalområdet, der medfører ICP-kontrol. Tilstræb altid se-natrium < 170 mmol/ml, og nødigt > 160 mmol/ml.
Sænke den cerebrale metabolisme: Dyb anæstesi, evt. relaksation.
Ekstern drænage via EVD om muligt.
Blodsukker i normalområdet.
Profylaktisk antiepileptika anbefales i nogle internationale guidelines, men anvendes ikke rutinemæssigt i DK.
- E:Normotermi på PICU ptt.Tromboseprofylakse.Opstart tidlig enteral ernæring + laksantia.
Sedationsstrategi:
- I ICP-labil fase aldrig Dexdor – kan øge ICP.
- Sedation med Propofol kun i korte perioder (max 4 mg/kg/time, max 24 (48) timer).
- Ved forventet længerevarende forløb med marginal ICP-kontrol vælges oftes Midazolam.
- Analgetika med såvel Remifentanil, Fentanyl eller morfin som infusion.
- Acceptér, at der ofte er behov for markant højere dosering af sedativa og analgetika end i andre kliniske sammenhænge.
- Tillæg af thiopental-infusion ved manglende ICP-kontrol – bør forudgås af vurdering af mulighed for kirurgisk optimering og kun iværksættes ved den kredsløbsstabile pt.
- Først ved sikker ICP-kontrol i minimum 24 timer og uden restriktioner for fx lejring og pleje kan aftrapning påbegyndes som beskrevet i afsnit om sedation.
- Acceptér at aftrapning sker fra højere baseline og derfor er tidskrævende.
Referencer:
- Guidelines for the Management of Pediatric Severe Traumatic Brain Injury, Third Edition: Update of the Brain Trauma Foundation Guidelines.
- Kochanek PM, Tasker RC, Carney N, Totten AM, Adelson PD, Selden NR, Davis-O’Reilly C, Hart EL, Bell MJ, Bratton SL, Grant GA, Kissoon N, Reuter-Rice KE, Vavilala MS, Wainwright MS.Pediatr Crit Care Med. 2019 Mar;20(3S Suppl 1):S1-S82. PMID: 30829890
- Udomphorn Y, Armstead WM, Vavilala MS Cerebral blood flow and autoregulation after pediatric traumatic brain injury.Pediatr Neurol. 2008 Apr;38(4):225-34. doi: 10.1016/j.pediatrneurol.2007.09.012. PMID: 18358399 Free PMC article. Review.
Afshari A, Clausen NG, Neuroanæstesi i: Børneanæstesi. 3. udgave, Kapitel 14
Kapitel 5 – Respiratorisk svigt
Respiratorisk svigt hos børn er en af de mest almindelige årsager til hospitalsindlæggelse, og hjertestop hos børn opstår oftest på hypoxisk basis forudgået af respiratorisk svigt.
Klinisk er der ofte tale om en progredierende akut eller pludselig forværring af den respiratoriske funktion i et sygdomsforløb, hvor relevant behandling kan iværksættes, hvis man erkender den fysiologiske forværring i tide. Børn har små luftveje, blød larynxbrusk, blød thoraxvæg, hurtigt trætbar muskulatur og lavere FRC, hvilket giver væsentligt øget risiko for luftvejsobstruktion, dynamisk luftvejskollaps og atelektaser. Samtidig er børn en patientkategori, der hurtigt udtrættes ved respiratorisk påvirkning. Sekundære tegn til respiratorisk svigt med nedsat bevidsthed og påvirkning af kredsløbet bør opfattes som faresignaler, hvor der er umiddelbar risiko for livstruende kollaps.
Klinisk Undersøgelse
Vurdering af det respiratoriske arbejde (Work of Breathing – WOB), er essentielt, når man undersøger et barn med respiratorisk svigt.
- Respirationsfrekvens
- Indtrækninger – herunder spil af alae nasi og brug af accessoriske respirationsmuskler (head-bobbing hos de mindste børn)
- Paradoks respiration
- Stetoskopi og saturation
- rtg. thorax eller lunge-ultralydsscanning
Årsager til respiratorisk svigt
- Obstruktivt
- ekstrathorakal (pseudocroup, fremmedlegeme, epiglottitis)
- intrathorakal (astma, bronchiolitis, laryngo- eller tracheomalaci)
- Restriktivt (pneumoni, pARDS, lungeødem, pneumothorax)
- Hypoventilatorisk (neuromuskulært svigt, forgiftninger). Beskrives ikke i denne udgave.
Behandling af obstruktivt og restriktivt respiratorisk svigt beskrives i detaljer under de enkelte tilstande.
Iltbehandling, High-flow og CPAP/NIV
Børn kan modtage respiratorisk støtte med iltbehandling via normalt næsekateter, High-flow Nasal Cannula (HFNC) og CPAP/NIV. Komfort og samarbejde med de forskellige modaliteter er en udfordring hos børnene, men det lykkes ofte ved hjælp af tålmodighed, et kompetent plejepersonale og støttende forældre. HFNC er ofte lettere at få til at fungere, da kontinuerlig CPAP/NIV med en tætsluttende maske er sværest at få barnet til at acceptere. Kortvarig maske-CPAP kan tit lykkes hos lidt større børn og hos børn under et år er et nasalt CPAP-system en god behandlingsmulighed. Evidensen i forhold til HFNC versus CPAP er ikke entydig, hverken inden invasiv respiratorbehandling eller efter ekstubation. HFNC er beskrevet nemmere at bruge og mere komfortabel for barnet. Efter ekstubation har CPAP en kortere behandlingsvarighed indtil børnene kan undvære respiratorisk støtte, men det kræver derimod mere sedation og er nogle gange ikke muligt at gennemføre. Behandlingssvigt kan forekomme ved begge modaliteter og antallet af re-intubationer er sammenlignelige. Behandlingsvigt målt på behovet for at skifte til den modsatte modalitet, er lidt højere ved HFNC.
Indikationer
Anvendes typisk til børn med moderate- til svære respiratoriske problemer såsom bronkiolitis, astma eller hypoksæmi, under forudsætningen at barnet kan holde frie luftveje.
Er ofte velegnet i overgangsfasen post-ekstubation ved fortsat behov for respiratorisk støtte.
Kontraindikationer
- Nasal obstruktion (f.eks. choanal atresi, epistaxis, store polypper)
- Børn med behov for akut intubation til beskyttelse af luftvejene f.eks. lavt bevidsthedsniveau
- Hyperkapnisk respirationssvigt
- Livstruende hypoxi med behov for akut intubation. Highflow/CPAP er ikke en erstatning for intubation.
- Aspiration af fremmedlegeme
- Opkast, gastrointestinal obstruktion (aspirationsrisiko)
- Maxillofaciale traumer og kirurgiske indgreb via næse/mund
Monitorering
- Observer barnets bevidsthedsniveau, respirationsarbejde, respiationsfrekvens, farver, puls, saturation og graden af sekret og hostekraft.
- Anvend nasogastrisk sonde som udluftning af luft i ventriklen.
Behandling
- Ved HFNC indstilles flow og FiO2 (se tabel).
- Bedste effekt ved HFNC og nasal-CPAP fås når barnet har lukket mund, og der kan derfor være behov for at anvende sut hos små børn. Nasal-CPAP anvendes derfor ikke til børn > 1 år.
- Bemærk at highflow ikke er en erstatning af regelret CPAP til behandling eller forebyggelse af atelektaser. Nasal Highflow vil let kunne maskere atelektasedannelsen i lyset af høj FiO2 mulighed og tilsyneladende normal SpO2. Anvend intermitterende maske CPAP som supplement til highflow
- nCPAP med modtryk 6-8 cmH2
- Ved manglende bedring indenfor 1 times observation eller akut forværring må øvrige tiltag overvejes, herunder NIV (BiPAP) eller regelret intubation.
- NIV med IPAP 6-8 cmH2O, EPAP 4-5 cmH2O.
| Flow-indstillinger ud fra vægt | |
| 0 – 15 kg | 1,5 – 2 L/kg/min |
| 16 – 20 kg | 25 L/min |
| 20 – 30 kg | 35 L/min |
| 31 – 50 kg | 40 L/min |
| > 50 kg | 50 L/min |
Opsætning, valg af katetre, hygiejne mv. henvises til lokale instrukser pga. forskelle i udstyr.
Respiratorbehandling
Anbefalingerne for respiratorterapi af børn i denne vejledning er baseret på den seneste opdatering af internationale guidelines PALICC-2. Respiratorbehandling af kritisk syge børn ligner i høj grad respiratorbehandling af voksne, og en del af behandlingsanbefalingerne er baseret på ekstrapolation fra voksne studier. Overordnet princip i respiratorterapi er lungeprotektiv ventilation (LPV) med brug af lavt tidalvolumen (TV) og relativt højt PEEP, begge afstemt i forhold til driving pressure og plateau tryk. Der findes ingen prospektive studier, som omhandler anvendelse af LPV til pædiatriske patienter, men retrospektive studier har vist færre komplikationer, signifikant lavere mortalitet og flere respirator-frie dage.
Indikation til respiratorterapi
- Respiratorisk svigt
- Cirkulatorisk svigt
- CNS sygdom
- Sikring af luftvejene
Generelle anbefalinger til ventilation i respirator
| · Ventilationsmodus: Volumenkontrolleret- og trykkontrolleret ventilation betragtes som ligeværdige alternativer, så længe de leverede tidalvolumina lever op til LPV-strategi.
· Tidalvolumen: 6-8ml/kg (evt. 4-6 ml/kg for at opnå det anbefalede plateau tryk og driving pressure) · Plateau tryk < 28 cm H2O. · Driving pressure < 15 cm H2O · PEEP: Indstilles i forhold til FiO2 jvf. tabel nedenfor (fra ARDSNet) · RF og I:E-ratio: Alderssvarende RF. – Lang ekspirationstid ved obstruktive tilstande (I:E=1:3 – 1:4 etc.) – Lang inspirationstid ved restriktive tilstande (I:E= 1:1 – 2:1 etc.) · FiO2: Lavest muligt til SaO2:88-92% · Behandlingsmål PaO2: 8-11 kPa (SpO2: 88-92%) · Behandlingsmål PaCO2: 4,5-6,0 kPa (acceptabel pH >7,20) |
Man bør hos alle børn tage individuel stilling til den laveste/højeste acceptable SaO2, samt pH. Der er stigende fokus på anvendelse af lavest mulig FiO2 for at nedsætte skadelig effekt af høje iltkoncentrationer. Permissiv hyperkapni med pH >7,20 kan accepteres, for at opnå LPV, medmindre patienten har sygdomme, hvor hyperkapni kan forværre patientens tilstand.
PEEP indstilles til højeste værdi iht. ARDS Net PEEP- tabel. Skal dog være kompatibel med plateautryk < 28 cm cmH2O, driving pressure < 15 cmH2O og TV= 6-8 ml/kg. PEEP 14-20 anvendes meget sjældent hos børn.
| FiO2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 | 1,0 |
| PEEP cm H2O | 5 | 6 – 8 | 8 – 10 | 10 | 10 – 14 | 14 | 14 – 18 | 18 – 24 |
Tabel 11
Baggrund for LPV strategi
Afvigelser fra LPV-strategi (højere TV og lavere PEEP end rekommanderet) er relativt hyppige og forbundet med øget mortalitet samt længere varighed af MV. Et nyligt ikke-randomiseret prospektiv studie af børn i respirator viste, at sænkning af plateautryk < 28 cm H2O og driving pressure < 15 H2O, anvendelse af PEEP/FiO2 kombinationer iht. ARDSNet -tabel, permissiv hyperkapni (pH 7,30–7,45 for mild pARDS eller pH 7,20–7,30 for moderat/svær pARDS) samt konservative behandlingsmål for SpO2: 92–97% og 88–92% for mild og moderat/svær pARDS, resulterede i reduceret 60-dages mortalitet.
Væsentlige udfordringer ved respiratorbehandling, forslag til strategi
- Respirator dyssynkroni
- Øget sedation, relaksering, ændre trigger-følsomhed (flow eller tryk)
- Udtalt airtrapping
- Nedsæt RF
- Lang ekspirationstid med I:E ratio 1:3 – 1:4 – 1:5
- Vedvarende svær hyperkapni
- Tung sedation/muskelreksation, reducér deadspace
- Vedvarende svær hypoksæmi
- Sjældent HFOV
- iNO ved pulmonal hypertension, tegn på højresidigt hjertesvigt eller ved svær refraktært hypoksæmi som bro til evt. ECMO
- ECMO, se under pARDS
Forberedelse til ekstubation
Da respiratorbehandling kan være forbundet med mange komplikationer, ønskes varigheden af behandlingen så kort som muligt. Der er begrænset litteratur om aftrapning og valg af ekstubationstidspunkt hos børn, hvorfor det i praksis beror på en klinisk vurdering.
Der anbefales:
- Kontrol af grundmorbus
- ABC-stabilitet på aktuel behandling
- Etableret/stabil spontan respiration (f.eks. PS)
- Vågent barn uden abstinenser
- Test af lækage omkring trachealtuben
Ved klinisk vurdering af ekstubationstidspunkt ses behov for reintubation i 2-20 % uafhængigt af længden af respiratorbehandling. Det største problem efter ekstubation af børn er den øvre luftvejsobstruktion.
Der kan udføres Spontaneous Breathing Test (SBT) vha. CPAP (5 – 10 cm H2O) eller Pressure Support (PS) med lille trykstøtte (op til 10 cm H2O). Over 30-120 minutter observeres der for tegn på respiratorisk stress.
Flere studier har vist, at protokolleret aftrapning af respiratorbehandling hos børn kan forkorte varigheden af respiratorbehandling samt forkorter indlæggelse på PICU.
Tilstande med obstruktiv luftvejssygdom
Ekstrathorakal obstruktion
Virale infektioner / pseudocroup
Den hyppigste årsag til ekstrathorakal luftvejsobstruktion er pseudocroup, der primært skyldes viral infektion (hyppigst parainfluenza-virus). Infektionen giver anledning til subglottisk inflammatorisk ødem og deraf følgende inspiratorisk stridor. Den gøende hoste og inspiratoriske stridor er klassiske kliniske tegn herpå. Barnet er oftest agiteret og kan have svære indtrækninger. Tilstanden giver sjældent anledning til behov for intensiv terapi.
Akut behandling
- Beroligende og professionel adfærd omkring barnet for at mindske agitation.
- Inhaleret adrenalin:
- Adrenalin 1 mg/ml, 1-2 ml blandet med isoton NaCl til i alt 4 ml. Kan gentages hver 10-15 min. Gives via forstøver på maske eller via nasal kateter.
- Peroral/systemisk steroid:
- Solu-Medrol 2 mg/kg i.v. gives, hvis der er brug for flere adrenalininhalationer.
- Ved desaturation kan nasal high-flow (HFNC) (flow 1,5 -2 L/kg/min) eller nasal-CPAP (modtryk 6-8 cm H2O) forsøges til at aflaste WOB. Vanskeliggøres ofte af barnets panik, og beroligende medicn kan overvejes (k.eks. clonidin/dexdor/kloralhydrat)
- Intubation og respiratorterapi ved udtrætning, svær desaturation og/eller hyperkapni. (obs vælg gerne en tubestørrelse 0,5 mindre mhp. at kunne passere det ødematøse område.
I sjældne tilfælde af svær pseudocroup kan inhalationsbehandling med heliox (hvis tilgængeligt) bruges som aflastning før intubation.
Fremmedlegeme
Fremmedlegemeaspiration ses jævnligt hos mindre børn, typisk < 3-5 år. Debut af hoste, stridor, dyspnø sker meget pludseligt, især under spisning eller leg med små dele.
Akut behandling
Håndteres iht. ERC-anbefalinger:
- Ved effektiv hoste: Ikke nødvendigt med specielle manøvrer.
- Ved ineffektiv hoste: Der bør gennemføres manøvrer til at fjerne fremmedlegemer i luftvejene (slag i ryggen/tryk i brystet). Kun synlige fremmedlegemer skal forsøges fjernet.
- Ved bevidstløst barn: Algoritme for basal genoplivning følges.
Indlæggelse på PICU skyldes de akutte komplikationer:
- Post-obstruktions lungeødem efter total eller nær-total luftvejsobstruktion
- Luftvejsinflammation førende til øget luftvejsmodstand
- Atelektaser/pneumonier
- pARDS
Epiglottitis
Livstruende hævelse af epiglottis pga. bakteriel infektion, som kan udvikles over få timer. Tilstanden er sjældent forekommende pga. vaccinationsprogrammet (Hæmophilus influenzae), men kan også skyldes andre bakterielle infektioner. Obstruktionsrisiko er stor hos mindre børn.
Epiglottitis adskiller sig fra virale infektioner i form af
- Barnet er alment påvirket
- Inspiratorisk stridor, der i de senere stadier kan være aftagende (faresignal pga. udtrætning)
- Dyspnø
- Højfebrilia
- Hvis barnet er stort nok, vil det pga. synkesmerter og sekret sidde op og læne sig fremover med udtalt savlen.
Akut behandling
Hurtig erkendelse af epiglottitis er altafgørende. Vanlig inhalationsterapi er uden effekt.
- Sikring af frie luftveje, i svære tilfælde akut intubation. Luftvejshåndtering foretages så vidt muligt på operationsstue i samarbejde mellem en ØNH-kirurg og børneanæstesiolog.
- Verificering af diagnosen via nasal fleksibel skopi med inspektion af epiglottis. Anæstesi induceres med sevofluran (spontan respiration længst muligt). Teamet skal være forberedt på tab af luftvej og behov for hyperakut tracheotomi.
- Antibiotika opstartes (cefuroxim som empirisk terapi, herefter efter mikrobiologisk fund).
Intrathorakal obstruktion
Status astmaticus
Astma er kendetegnet ved inflammation og luftvejs hyperreaktivitet. Akutte eksacerbationer resulterer i reversibel luftvejsobstruktion med bronkospasme, mucus hypersekretion og dynamisk hyperinflation betinget af begrænset ekspiratorisk flow. Klinisk ses barnet med et signifikant øget respirationsarbejde i form af forceret ekspiration med ”pibende” vejrtrækning ved stetoskopi og indtrækninger. Potentielt livstruende symptomer:
- CNS påvirkning, træthed/falder hen, og nedsat respons på smerte.
- Hypoxæmi trods ilttilskud
- Hypoventilation med overfladisk respiration, tyst thorax og/eller udtrætning
- Hyperkapni (PaCO2 > 6 kPa), især progredierende
- Bradykardi og /eller hypotension
- Konkurrerende komorbiditet (neurologisk sygdom, hjertesygdom)
Akut behandling
- Ilt-tilskud, SaO2 92-97
- Væskeresuscitation ved dehydratio.
- Inhalationsbehandling: Korttidsvirkende β-2-adrenerg agonist.
Salbutamol (Ventoline®) 0,15 mg/kg (min. 2,5 mg, max. 5 mg) x3/time de første timer, herefter x1 hver 1.-4. time.
Inhalation af β2-agonist bør fortsættes, hvis der er sikker klinisk effekt, gerne med inhalationer der gives ”back-to-back” dvs. der hele tiden startes en ny inhalation. Vær opmærksom på, at børn under 1 år oftest ikke har receptorer for β2-agonister.
- Antikolenergika: Fremmer muligvis bronkodilation, men har en langsom virkning
Ipratropium (Atrovent®)
- <20 kg: 250 µg x 4 i 24 timer (250 µg blandes i 3 ml NaCl)
- >20 kg: 500 µg x 4 i 24 timer
Ipratropium kan også blandes med salbutamol og budesonid ved behov.
- Systemisk steroid:
- Solu-Medrol 2 mg/kg som mætningsdosis (maks. 50 mg), derefter 1 mg/kg x 4 i.v.
- Magnesiumsulfat i.v: Afslapper glat muskulatur og fremmer bronkodilatation. Anvendes ved manglende bedring under inhalationsbehandling og systemisk steroid.
- Bolus 0,1 mmol/kg i.v. (maks. 8 mmol) over 20 min. Behandlingen kan gentages, dog under kontrol af s-Mg som skal holdes < 2 mmol/l
- Salbutamolinfusion kan overvejes
- Salbutamol bolus 2-5 µg/kg i.v. over 5 minutter som mætningsdosis, efterfulgt af vedligehold infusion 5-10 µg/kg/t, dosis kan øges op til 20 µg/kg/t. Dosis reduceres ved takykardi >200. (Obs. bivirkninger med laktatstigning og kalium-fald).
- Sedation, relaksation og respiratorbehandling.
- Andre behandlinger uden evidens
- Adrenalin inhalation (børn < 2-3 år)
Adrenalin 1 mg/ml, 1-2 ml blandet med isoton NaCl til i alt 4 ml
- Mukolytika – inhaleret Pulmozyme® 2,5 mg x 1.
- Mukolytika – inhaleret Natriumchlorid
- Inhalationsbehandling med Sevoflurane
- Ketamin
Non-invasiv ventilations støtte (NIV) ved status astmaticus
Behandling med high-flow-nasal cannulation (HFNC), continuous positive airway pressure (CPAP) og NIV i pædiatriske populationer er steget i det sidste årti. NIV ved akut astma er forbundet med lavere risiko for invasiv mekanisk ventilation og dødelighed. Modaliteten skal anvendes under tæt monitorering af effekt (reduceret respirationsarbejde og aftagende hyperkapni).
- NIV kan påbegyndes med CPAP indstilling med modstand på 5 cm H2O, og ved behov optitreres til 7-8 cm H2
- NIV indstilling med støtte (PS, Pressure Support) på 6-12 cm H2 Jo større indblæsnings støtte, des mere risiko for maskelækage. Ses ikke hurtig lindring (aftagende respirationsarbejde og reduceret hyperkapni) skrides til intubation.
- Potentielle bivirkninger ved NIV inkluderer barotraume, pneumothorax og aspiration. Ved længerevarende NIV behov skal anlægges sonde.
- Ved effekt er compliance generelt god. Ved behov kan let sedation anvendes f.eks. med en a2-receptor agonist, lavdosis propofol eller ketamin afhængig af lokal erfaring/strategi.
Invasiv respiratorbehandling ved status astmaticus
- Indikationer:
- Respirationsstop
- Tiltagende ventilatorisk svigt/hypercapni
- Bevidsthedspåvirkning
- Behandlingssvigt på HFNC/CPAP/NIV
- Anæstesi til intubation kan anbefales Ketamin/Rocuronium, evt. Fentanyl. Alternativt
Intubation på operationsgangen med sevofluran pga. den kraftige bronchiedilaterende effekt, samt længst mulig bevaret egen-respiration.
- Volumenkontrolleret og trykkontrolleret ventilation betragtes som ligeværdige, så længe principperne for LPV følges.
- OBS: PIP reflekterer sjældent det reelle alveolære tryk grundet bronkospasme og mucus. Monitorer Pplateau (stil efter P plateau <28 cm H2O)
- Prioriter lang ekspirationstid og monitorer i-PEEP.
- I:E-forholdet op til 1:4 til 1:5
- Ekstern PEEP sættes lavt, f.eks. 0-5 cm H2O. Herefter op- eller nedjusteres PEEP afhængig af ændringerne i barnets tilstand. Ved justering af ekstern PEEP, kan risikoen for hyperinflation, barotraume, pneumothorax og hypotension forværres, så monitorering af iPEEP anbefales. Ved akut forværring tjek for svær airtrapping diskonnekt barnet fra respiratoren kortvarigt og thorax komprimeres.
- Hyperkapni er almindeligt under mekanisk ventilation og permissiv hyperkapni accepteres (pH ned til 7,20). Natriumbikarbonat kan evt. anvendes som buffer.
- Dyb sedation evt. med ketamin eller sevofluran. Ofte er der initielt behov for muskelrelaksation mhp. at undgå dynamisk obstruktion
- Kontakt ECMO-center, hvis den kliniske tilstand efter intubation fortsat er ustabil. Se under pARDS.
Bronchiolitis
Øvre luftvejsinfektion der efterfølges af symptomer på nedre luftvejsinfektion i form af hoste og hvæsende vejrtrækning hos børn < 2 år. Udløses typisk af RSV eller andre luftvejsvira.
Vanskeligt forløb og respiratorbehov forekommer hyppigere hos
- børn under 3 måneder
- ex-præmature/bronkopulmonal dysplasi, BPD
- børn med medfødt hjertesygdom
- immunkompromitterede børn.
Især de ex-præmature og mindre børn kan debutere med apnøer som første symptom.
RSV giver heterogen lunge påvirkning og beskrives nemmest som at have astma og pneumoni samtidigt. Det vanskeliggør respiratorbehandling, hvorfor spontan respiration bør understøttes mest muligt.
Akut behandling
- Sikre frie luftveje med fx NaCl-inhalationer, NaCl nasalt samt evt. sugning
- Ilt-tilskud for at sikre SaO2 92-97%
- Sænke iltkrav ved at undgå feber, stress og uro
- nasal highflow (HFNC) 1,5-2 L/kg/min eller CPAP 5-8 cmH2O for at mindske hypoventilation/hyperkapni eller hypoksi, der vil føre til takypnø og yderligere forværring i airtrapping
- Ved manglende effekt af CPAP kan NIV/PS forsøges. Let sedation med α2-agonister kan anvendes mhp. kooperation til NIV
- β2-agonist kan forsøges ved bronkospasme og bør kun fortsættes ved sikker effekt.
- Hyperton NaCl kan ved forsøges ved vedvarende sekretproblemer. Anbefales forsigtig tilgang fx blandet halvt med isoton NaCl. NB: kan være bronkoirriterende og udløse bronkospasmer.
- Ingen evidens for rutinemæssig behandling med steroid.
- Respiratorbehandling ved udtrætning eller svær hypoxæmi. (se næste afsnit)
Tilstande med restriktiv lungesygdom
Pædiatrisk akut respiratorisk distress syndrom (pARDS)
Pædiatrisk akut respiratorisk distress syndrom er en alvorlig tilstand karakteriseret ved inflammatorisk skade på alveolerne og tegn på nedsat gasudveksling. pARDS diagnosen og behandlingsalgoritmerne er opdateret i 2023 ved PALICC-2. Nu beskrives en ”Possible pARDS diagnosis” til børn i HFNC samt et ønske om, at pARDS alvorligheden først defineres 4 timer efter den initiale diagnose er stillet. Der er introduceret en mulighed for at stille pARDS diagnosen med en saturationsmåling (uden en PaO2). Derudover klassificeres pARDS i fire typer afhængigt af invasiv eller non-invasiv ventilation og mild/moderat eller svær pARDS. Grundlæggende er behandlingsalgoritmen dog stadig meget som hos voksne med ARDS, og inddeles i en respiratorisk behandlingskomponent og supplerende behandling.
| Diagnose af pædiatrisk akut respiratorisk distress-syndrom (pARDS) | |||||
| Alder | Ekskluder patienter med perinatal lungesygdom. | ||||
| Tidsramme | Inden for 7 dage efter kendt klinisk påvirkning. | ||||
| Oprindelse af ødem | Ikke fuldt ud forklaret ved hjertesvigt eller overhydrering. | ||||
| Rtg. af thorax | Nye infiltrater/fortætninger (unilaterale eller bilaterale), der er forenelige med akut pulmonal parenkym sygdom og som ikke primært skyldes atelektase eller pleuralvæske | ||||
| Oxygenering | IMV: OI ≥ 4 el. OSI ≥ 5 NIV: PaO2 / FiO2 ≤ 300 el. SpO2 / FiO2 ≤ 250 Stratificering af pARDS sværhedsgrad: Anvendes ≥ 4 timer efter den initiale diagnose pARDS |
||||
| IMV-pARDS: | Mild/moderat: OI < 16 eller OSI < 12 | Svær: OI ≥ 16
eller OSI ≥ 12 |
|||
|
|
NIV-pARDS:
Special populationer |
Mild/moderat NIV-pARDS:
PaO2 / FiO2 > 100 eller SpO2 / FiO2 > 150 |
Svær NIV-pARDS: PaO2 / FiO2 ≤ 100 el. SpO2 / FiO2 ≤ 150 | ||
| Cyanotisk hjertesygdom | Ovenstående kriterier, med akut forværring af oxygenationen, som ikke kan forklares ved hjertesygdom. | ||||
| Kronisk lungesygsom | Ovenstående kriterier, med akut forværring af oxygenationen i forhold til baseline | ||||
Respiratorisk behandling
Non-invasiv behandling:
- Nasal 02/HFNC kan forsøges og ved forværring kan CPAP/NIV opstartes.
- Bedring bør ses inden for de første 6 timer i NIV, men ved forværring trods optimale betingelser som sikring af fugtet luft, optimal interface, sedation og evt. synchronisering bør patienterne intuberes.
Invasiv ventilation:
- Intubation med tube m/cuff
- Ingen evidens for at anbefale enten tryk- eller volumenkontrolleret respiratormodus.
- Lungeprotektiv behandling (se ovenfor under respirator terapi)
Supplerende behandling ved pARDS
- Sedation skal doseres mhp optimering af den mekaniske ventilation, så oxygenering og ventilation optimeres. Dette kan kræve dyb sedation.
- Neuromuskulær blokade kan ikke anbefales rutinemæssigt, men kan bruges med passende sedation til optimering af effektiv og protektiv mekanisk ventilation.
- Hydreringsgrad følges nøje. Overhydrering er yderst uhensigtsmæssigt og erfaringsmæssigt optimeres børnene bedst med negativ væskebalance.
- Bugleje kan overvejes til børn med svær pARDS, der ikke responderer på anden terapi.
- Lungerekruttering anbefales ikke.
- Steroidbehandling anbefales ikke rutinemæssigt (manglende evidens blandt børn), men kan overvejes i situationer, hvor man vil reducere inflammation i lungerne ved svær pARDS.
- iNO er ikke rutine behandling ved pARDS, men kan bruges ved påvist pulmonal hypertension, svært højresidigt svigt eller som bro til ECMO.
- HFO kan overvejes til børn, hvor ventilatoriske mål i konventionel respiratorterapi med LPV ikke kan nås.
- APRV kan ikke anbefales.
- Surfactant har kun en rolle til udvalgte neonatale patienter.
- ECMO bør overvejes, hvis ikke der kan opnås acceptable forhold med lungeprotektivt ventilation. ECMO betragtes som en rescue-behandling til børn med behandlingsrefraktær svær hypoxæmi. Indikation for denne behandling er arterielle ilttension < 8 kPa trods 100 % O2, vedvarende højt plateautryk > 28 cm H2O og manglende udsigt til bedring inden for de nærmeste timer. Konferer med ECMO-center på Rigshospitalet tlf.: 35 45 16 98 eller 35 45 13 27 (børn < 2 år).
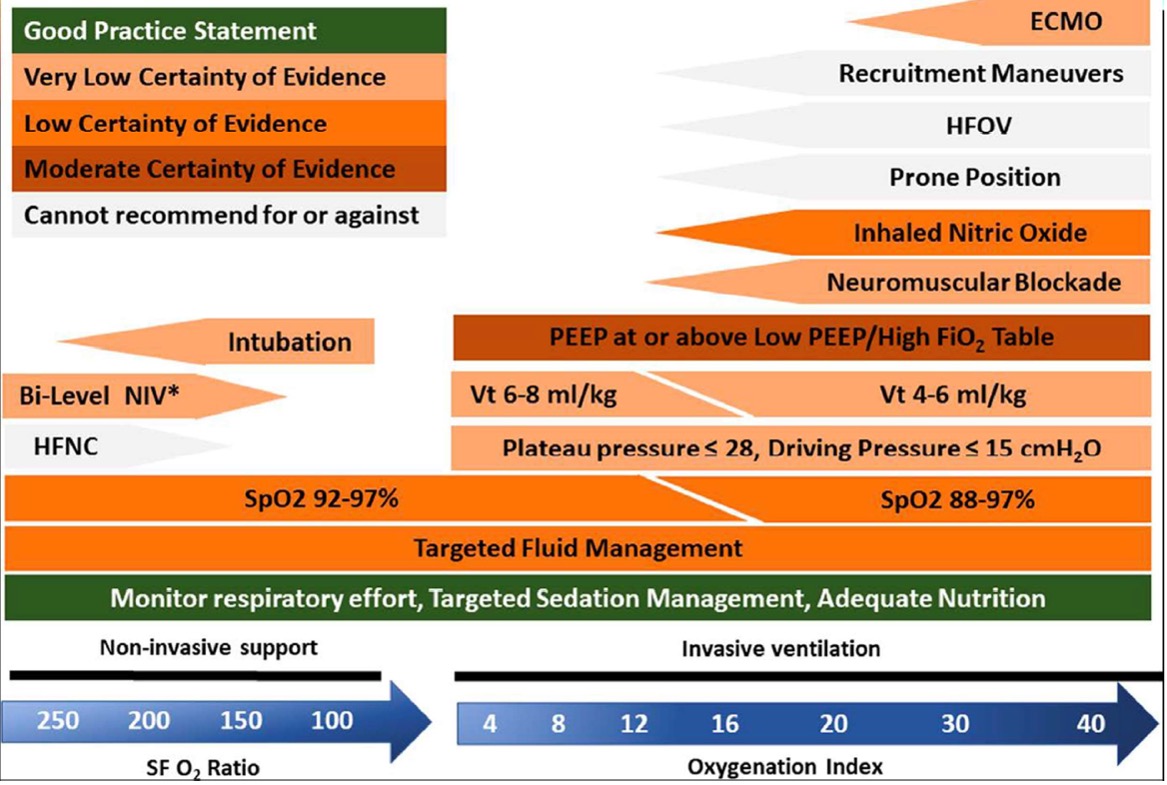
Figur 4 Illustration af behandling af pARDS
Referencer:
- Ramnarayan P et al.: “Effect of High-Flow Nasal Cannula vs Continuous Positive Airway Pressure Therapy on Liberation From Respiratory Support in Acutely Ill Children Admitted to Pediatric Critical Care Units:A Randomized Clinical Trial”. JAMA 2022 Jul 12;328(2):162-172.
- Brower RG, Matthay MA, Morris A et al. The ARDS Network. Ventilation with lower tidal volume as compared with traditional tidal volumes for acute lung injury and acute respiratory distress syndrome. N Engl J Med. 2000;342(18):1301-8
- Executive Summary of the Second International Guidelines for the Diagnosis and Management of Pediatric ARDS (PALICC-2). PCCM 2023; 24
- Ferreira FV, Sugo EK, Aragon DC et al. SBT for Prediciton of Extubation Success in Pediatric Patients Following Congenital Heart Surgery: A randomized Controlled Trial. Pediatr CCM 2019; 20:940-946
- Adherence to Lung protective Ventilation Principles in Pediatric Acute Respiratory Distress Syndrome: A Pediatric Acute Respiratory Distress Syndrome Incidence and Epidemiology Study. Bhalla AK, Klein MJ et al. Crit Care Med 2021; 49:1779-89
- Lung Protective Ventilation for Pediatric Acute Respiratory Distress Syndrome: A Nonrandomised Controlled Trial. Wong JJM, Dang H et al. CCM 2024; 52:1602-11
- Conservative versus liberal oxygenation targets in critically ill children (Oxy-PICU): a UK multicenter, open, parallel-group, randomized trial. Peters MJ, Gould DW, Ray S et al. Lancet 2024; 403:355-64
Kapitel 6 – Cirkulation
| Behandling af shock
· Akut behandling efter ABCDE. Sikre fri luftveje, giv 100% ilt på maske, overvej intubation. · Anlæg intravenøs adgang. IO kan anvendes. Vasopressor/inotropi kan gives perifert indtil central adgang haves. · Tidlig diagnostik: Blodprøver (incl. syre-base og bloddyrkning). EKG, rtg af thorax og ekkokardiografi.
Septisk shock · Væskebolus 10 ml/kg, op til 40-60 ml/kg inden for første time. · Vasopressor/inotropi bør overvejes efter 40 ml/kg. Noradrenalin eller adrenalin er førstevalg. · Opstart bred antibiotisk behandling indenfor første time. · Korrektion af anæmi, hypocalcæmi og hypoglykæmi. · Overvej steroid ved katekolamin-refraktært shock.
Anafylaktisk Shock · Adrenalin 0,01 mg/kg intramuskulært (maks. 0,3-0,5 mg per dosis). Kan gentages efter 3-5 minutter ved manglende effekt. – eller: · Adrenalin autoinjektor intramuskulært (< 25 kg 0,15 mg; > 25 kg 0,3 mg). · Intravenøst adrenalin behandling kun ved kardiovaskulært kollaps (kun monitorerede patienter og kun af personale med kendskab). · Fjern potentielle triggere. · Ved kredsløbspåvirkning, væskebolus 10 ml/kg. · Ved bronkospasme: Inhalation beta2-agonist (Salbutamol 0,15mg/kg, max 5mg). · Ved stridor/luftvejsødem: Inhalation adrenalin (0,5-1 mg blandet i NaCl til i alt 4 ml).
Hypovolæmisk shock · Væskebolus 10 ml/kg op til 40-60 ml/kg indenfor første time. · Forsæt aggressiv væskebehandling ved pågående tab. · Ved blødning gives balanceret transfusion (2:2:1) og blødningskilde identificeres (stands blødning).
Kardiogent shock · Forsigtig Væskebolus 5-10 ml/kg over 30 min. · Tidlig opstart af vasopressor/inotropi. Målrettes efter diagnostik og konfereres tidligt med højtspecialiseret afdeling.
|
Introduktion
Tidlig opsporing og erkendelse af kardiovaskulær instabilitet anses som af væsentlig betydning for et godt outcome hos børn. Da ingen hæmodynamiske parametre kan stå alene i vurderingen af den kardiovaskulære funktion af børn, er en grundig klinisk undersøgelse særlig vigtig.
Især nyfødte og små børn har et umodent myokardium, hvilket betyder at evnen til at øge kontraktiliteten er begrænset, og som følge heraf ses et relativt fikseret slagvolumen. Små børns cardiac output er derfor i høj grad afhængig af hjertefrekvensen, og takykardi ses ofte som kredsløbsmæssig kompensatorisk mekanisme i situationer med øget belastning af hjerte eller kredsløb. Denne kompensatoriske mekanisme når sin øvre grænse, når hjertefrekvensen krydser grænsen for hvor hurtigt hjertet kan nå at fylde sig igen (tid i diastole). Myokardiel dysfunktion, som ofte er en kombination af udtømte kompensatoriske mekanismer, myokardiel iskæmi (højt ilt forbrug pga. takykardi, og lavt ilttilførsel pga. lavt BT og lav koronarperfusion), samt immaturt myokardium, betyder at svært shock i fravær af intervention, har potentiale til hastigt at progrediere mod manifest kredsløbs kollaps.
Hypotension er ofte et sent og meget alvorligt symptom. Bradykardi skal altid betragtes som et periarrest symptom, hvor barnet er tæt på cirkulatorisk kollaps.
Klinisk Undersøgelse
- Puls, blodtryk, saturation og respirationsfrekvens
- c et p.
- Perifer perfusion (kapillærrespons, centrale/ vs perifere pulse, pulsamplitude, farve (bleg, cyanose), temperatur)
- Oliguri/anuri
- Påvirket bevidsthed (uro, sløv/somnolent (AVPU)
- Hepatomegali, halsvenestase og krepitation (mistanke om akut hjertesvigt)
Supplerende undersøgelser
- Røntgen af thorax
- EKG
- Ekkokardiografi
- Syrebasestatus (pH, laktat, calcium, Natrium, Kalium, Hgb/Hct, blodsukker). Kan tages arterielt, venøst eller kapillært.
- Bloddyrkning ved mistanke om infektion, samt relevante podninger (sekret, urin, drænvæske etc.)
- Blodtype + forlig (BAC/BAS test)
- Blodprøver: Hæmoglobin, leukocytter inkl. diff.tælling, kreatinin, karbamid, albumin, ALAT, bilirubin, LDH, INR, trombocytter, CRP, pro-BNP, evt. sporstoffer og ammonium.
- DIC-prøver på mistanke om hæmoragisk diatese
Obs: Der kan tages samme blodprøver på intraossøs adgang som på iv adgang, men husk prøverne kan ikke altid analyseres på samme apparatur, og har andre referencer.
Monitorering
Et hæmodynamisk påvirket barn indlagt på intensiv bør monitoreres med følgende:
- EKG, saturation og blodtryk.
- Invasivt blodtryk bør bruges ved behov for vasopressor/inotropi, behov for nøjagtig kontrol af blodtryk (f.eks. ved forhøjet intrakranielt tryk/malign hypertension) eller ved behov for hyppig syrebasestatus (f.eks. svær respiratorisk påvirkning)
- CVP og ScvO2 kan bruges som supplement ved ustabile patienter, men kan ikke stå alene i vurdering af væskebehov.
- Ekkokardiografi kan være en vigtig parameter i forhold til kardiel dysfunktion, og gentagne undersøgelser anbefales for at se effekt af behandlingen. Undersøgelse i forhold til morfologi eller specifikke kardiologiske mål bør kun udføres af kardiologer med speciale i børn.
- Avancerede invasive målinger fx Cardiac Output måling via arteria pulmonalis kateter er der kun indikation for på et børnehjertekirurgisk center.
Normalværdier

Tabel 12 Normalværdier
Shock
Patofysiologisk tilstand karakteriseret ved, at blodcirkulationen og dermed ilttilbuddet til vævene er utilstrækkeligt til at imødekomme kroppens metaboliske behov.
Distributivt shock
Septisk Shock
Definition: Sepsis er en tilstand karakteriseret ved livstruende organsvigt forårsaget af et dysreguleret respons på infektion, og er en af de førende dødsårsager blandt børn globalt. I 2024 er de pædiatriske kriterier for pædiatrisk sepsis og septisk shock revideret. (Tabel 13: “The Phoenix Sepsis Score” nedenfor)
Akut behandling
- Sikre frie luftveje
- Giv 100% ilt på Hudson maske med reservoir (flow min. 10 L/min)
- Intubation bør overvejes, hvis der er betydelige tegn på overhydrering med væskeophobning, respirationssvigt eller ved behov for metabolisk kontrol
- Anlæg iv adgange (evt. IO, husk blodprøver og bloddyrkning)
- Hvis hæmodynamisk ustabil gives væskebolus 10 ml/kg over 5-10 min
- Væskebolus kan gentages op til 40-60 ml/kg hvorefter inotropi/vasopressor opstartes.
- Opstart bred antibiotisk behandling – helst efter relevante dyrkninger, men dette må ikke forsinke behandlingen.
- Korrektion af anæmi, hypocalcæmi og hypoglykæmi.
- Overvej steroid ved katekolaminresistent shock
- Overvej immunglobuliner ved toxisk shock syndrom
Behandling specifik
Væskebehandling:
- Balancerede væsker som Ringer-lactat/acetat eller Plasmalyte anbefales pga. risikoen for hyperkloræmisk acidose. Isoton NaCl kan accepteres som initiale væskebehandling.
- Blod kan være indiceret efter vanlige retningslinjer. Transfusionsgrænse med hæmoglobin < 6 mmol/L i den akutte fase og ved ustabile patienter. Herefter er grænsen 4,3 mmol/L hos ellers raske børn.
- Når patienten er hæmodynamisk stabiliseret, fortsættes vedligeholdelses væskebehandling i henhold til det basale væske/glucose behov og elektrolytter. (se afsnit om væsketerapi)
Vasopressor/Inotropi:
Skal overvejes ved tegn på overhydrering, og senest efter væskebolus sv.t. 40-60 ml/kg.
- Adrenalin og Noradrenalin betragtes som ligeværdige førstevalg ved svært shock, og har begge vist bedre outcomes i forhold til dopamin. Principielt har noradrenalin været førstevalg ved tilstande karakteriseret ved vasodilatation og højt cardiac output (varm perifert), mens adrenalin er førstevalg ved tilstande med vasokonstriktion og lavere cardiac output (kold og marmoreret perifert)
- Kan gives i perifer iv adgang, indtil en central adgang er tilgængelig
- EKKO overvejes til vurdering af pumpefunktion
- Ved katekolamin resistent shock kan overvejes at supplere med vasopressin
- Ved manglende behandlingsrespons overvejes overflytning til højtspecialiseret afdeling med ECMO-kompetencer.
Antibiotika:
- Der opstartes bredspektret antibiotika på baggrund af klinik. (Piperacillin/tazobactam eller meropenem)
- Bør administreres intravenøst hurtigst muligt og optimalt indenfor 1 time efter ankomst
- Ved specifik mistanke om meningokoksygdom bør antibiotika administreres IV inden for 15 minutter, alternativt anbefales intraossøs eller intramuskulær behandling
- Det er vigtigt at lede efter fokus, og dermed sikre relevant prøvemateriale
- Kirurgi kan være nødvendigt i særlige tilfælde (f.eks. ved septisk artritis, abscesser, nekrotiserende fasciitis m.fl.)
- Antibiotika revurderes løbende og indsnævres hurtigst muligt i henhold til fokus og mikrobiologiske fund
Kortikosteroidterapi:
- Patienter i systemisk binyrebarkhormonbehandling bør dækkes med ”steroidparaply” efter vanlige retningslinjer (døgndosis x 2)
- Ved katekolaminresistent shock overvejes iv Hydrokortison 2 mg/kg som startdosis, herefter 1 mg/kg hver 8. time.
Elektrolytter:
- Stiler mod Ca2+ > 1,1 mmol/l.
- Korrigeres med Calcium-gluconat 10 % (sv.t. 0,23 mmol/ml) 0,5 ml/kg. eller Calcium-klorid 5,5 % (sv.t. 0,5 mmol/ml) 0,2 ml/kg.
- Begge kan gives ufortyndet i perifer iv adgang over 5 minutter under EKG monitorering. Calciumgluconat foretrækkes grundet mindre vævstoksiske egenskaber ekstravasalt og fravær af klorid
- Kan gentages umiddelbart ved manglende respons
- Hypocalcæmi (og hypokaliæmi) kan være behandlingsrefraktære ved samtidig ubehandlet hypomagnesiæmi. Behandles med Magnesium-sulfat iv. 0,4 mmol/kg, givet over 20 min.
Dissemineret intravaskulær koagulation (DIC):
DIC mistænkes ved hudblødninger større end 2 mm kombineret med septisk shock.
- Biokemisk DIC uden symptomer behandles ikke specifikt, men ved behandling af udløsende
årsag (se afsnit on DIC / Koagulation)
Immunglobuliner:
Er som udgangspunkt kun indiceret ved nekrotiserende bløddelsinfektioner og invasive Gr. A streptokok infektioner med toxisk shock syndrom (her overvejes ligeledes clindamycin mhp hæmning af yderligere toxinproduktion)
Blodsukker:
Børn med sepsis er i øget risiko for hypoglykæmi.
- Ved lavt BS < 3 mmol/l gives glukose 10 % (100 mg/ml) 3 ml/kg.
- BS måles initialt efter 10 min og kontrolleres til normaliseret. Herefter med 1-2 timers mellemrum indtil sikkert stabilt, hvorefter BS måles hver 4. time
Anafylaktisk shock
Definition
“Anafylaksi er en alvorlig og potentiel livstruende systemisk overfølsomhedsreaktion karakteriseret ved hurtig indsættende luftvejs-, respiration- eller kredsløbsproblemer. Er normalt, men ikke altid, yderligere forbundet med hud- og slimhindeforandringer.”
Risikofaktorer for udvikling af svær anafylaktisk reaktion
- Kardiel eller respiratorisk komorbiditet, særligt svær astma
- Allergi
- Børn (små luftveje), særligt mindre børn med pågående øvre luftvejsinfektion
Hyppigste årsager
- Fødevarer: Jordnødder, æg, soja, skaldyr, fisk
- Insektbid
- Medicin: Beta-lactam antibiotika, NSAID, non-depolariserende muskelrelaksantia
- Andet: gummi/latex (sutter, legetøj)
- I ca. 20 % af tilfældene identificeres ikke en årsag (idiopatisk)
Udredning / diagnostik
Diagnosen anafylaktisk shock stilles klinisk. Ved akut opstået hypotension/takykardi, bronkospasme eller øvre luftvejsobstruktion, efter eksponering for en potentiel trigger, bør akut behandling institueres på mistanke. De fleste reaktioner opstår umiddelbart (indenfor 30 minutter efter eksponering), men kan forekomme med op til 4 times latens.
Hastig sygdomsprogressionen er ofte et udtryk for sværhedsgrad og behov for akut behandling.
En detaljeret anamnese er ofte afgørende for at bekræfte udløsende årsager, men det er meget vigtigt, hurtigt at erkende shock på anafylaktisk baggrund og instituere den korrekte behandling uden unødige forsinkelser. Også selvom typiske hudforandringer som urticaria, erythem og/eller angioødem ikke nødvendigvis er til stede (fraværende i op til ca. 20% af tilfældene).
Anafylaksi mistænkes således i følgende kliniske scenarier:
- Akut opstået (minutter-timer):
- Hud- og/eller slimhindesymptomer (generaliseret kløe, flushing, urticaria, angioødem)
– kombineret med mindst én af følgende tilstande:
- Luftvejs- og/eller vejrtrækningsproblemer (synkebesvær, hæshed, stridor, dyspnø, bronkospasme, cyanose, respirationsstop) eller
- Blodtryksfald* med ledsagesymptomer (takykardi, synkope, konfusion, inkontinens, kollaps)
- To eller flere af følgende symptomer opstået akut efter udsættelse for et potentielt allergen:
- Hud- og/eller slimhindesymptomer (generaliseret kløe, flushing, urticaria, angioødem)
- Luftvejs- og/eller vejrtrækningsproblemer (synkebesvær, hæshed, stridor, dyspnø, bronkospasme, cyanose, respirationsstop)
- Blodtryksfald* med ledsagesymptomer (takykardi, synkope, konfusion, inkontinens, kollaps)
- Svære gastrointestinale symptomer (krampagtige smerter, opkastning, diarré)
| *lavt systolisk blodtryk for alder
1 – 12 mdr.: < 70 mm Hg 1 – 10 år: < 70 mm Hg + [2 x alder] 11 – 18 år: < 90 mm Hg eller > 30 % fald i systolisk blodtryk |
Akut behandling
- Adrenalin 0,01 mg/kg intramuskulært (maks. 0,3-0,5 mg per dosis). Ved manglende effekt gentages samme dosis efter 3-5 minutter
– eller:
- Adrenalin autoinjektor intramuskulært: Børn < 25 kg: 0,15 mg. Børn > 25 kg 0,3 mg
- Kun ved kardiovaskulært kollaps er der indikation for intravenøs behandling med fortyndet adrenalin. Dette bør kun administreres til monitorerede patienter og af personale med kompetencer i intravenøs adrenalin administration
- Sikre frie luftveje i kombination med ilt tilskud på maske
- Fjern potentielle triggere, hvilket også indebærer at pausere ikke livsvigtigt medicin og infusioner
Adjuverende akut behandling
- Ved kredsløbspåvirkning:
- gives væske 10 ml/kg 0,9% NaCl, som i.v. bolus (kan gentages)
- Ved bronkospasme:
- Inhalation beta2-agonist: Salbutamol 0,15mg/kg (max 5mg) (kan gentages)
- Ved stridor/luftvejsødem:
- Inhalation adrenalin: 1 mg i 4 ml NaCl (kan gentages)
- Ved refraktært luftvejsødem trods adrenalin inhalationer, skal tidlig intubation kraftigt overvejes
Evt. supplerende behandling efter initial ABC-stabilisering
- Antihistamin: Clemastin 0,025mg/kg iv/im (max. 2 mg)
Antihistamin kan mindske kutane symptomer, men har ingen effekt på respiratoriske og kardiovaskulære symptomer og forhindrer ikke progression.
- Kortikosteroid: Methylprednisolon 2mg/kg iv (max 80mg)
Kortikosteroider og leukotrienantagonister har ikke dokumenteret effekt på anafylaksi, og anbefales derfor ikke som rutine behandling. Omvendt, ved refraktær og vedvarende astma/shock kan kortikosteroider overvejes som supplerende behandling
Monitorering
- Afhængig af lokale ressourcer overvejes efter stabilisering overflytning til Universitetshospital.
- Barnet indlægges til observation, ved alvorlige reaktioner med respiratorisk og/eller cirkulatorisk påvirkning initialt på intensiv. Skal have været cirkulatorisk og respiratorisk stabil i minimum 8 timer før udskrivelsen. Børn indlægges ofte natten over.
- Risikopatienter bør observeres under indlæggelse i længere tid. Det gælder:
- Mindre børn
- Alvorlig reaktion med protraheret behandlingsforløb
- Reaktioner hos børn med svær/ustabil astma
- Reaktioner med risiko for fortsat absorption af allergen
- Børn med tidligere bifasisk reaktion
- Børn, der udvikler reaktion om aftenen eller natten, eller hvor evt. sociale omstændighed medfører nedsat evne til at reagere på en forværring
- Børn, som opholder sig i områder med vanskelig tilgang til akutbehandling
Hypovolæmisk shock
Hyppigste årsager hos børn
- Gastrointestinale tab: Opkast, diarré
- Urogenitale tab: Diabetisk ketoacidose, diabetes insipidus, adrenal insufficiens/Mb. Addison, nyresygdom (nefrotisk syndrom), diuretika/iatrogent
- Nedsat væskeindtag: Stomatitis, pharyngitis, anorexi, konfusion/cerebral påvirkning
- Andre tab/translokation: Perspiratio/feber, kapillær leak, tyndtarmsobstruktion/ileus, peritonitis, akut pankreatit, forbrændinger, ascites
- Blødning
Udredning / diagnostik, hypovolæmisk shock mistænkes ved
- Relevant anamnese som anført ovenfor under årsager
- Kliniske markører med tegn på insufficient kredsløb og utilstrækkelig perifer vævsperfusion. Hurtigt erkendelse af shock på baggrund af hypovolæmi er vigtig, og akut behandling må ikke forsinkes af mere avanceret udredning
Akut behandling
- Iv/io adgang etableres
- Ved kredsløbspåvirkning gives intravenøs væskebehandling. Væskebolus 10 ml/kg med balancerede krystalloid eller NaCl
- Ved behov gentages yderligere væskebolus 10 ml/kg balancerede krystalloider op til 40-60 ml/kg indenfor den første time
- Ved blødning gives balanceret transfusion (se afsnit om transfusion)
Behandlingsmål: Normalt blodtryk og frekvens for alder, normal pulsfylde og kapillærrespons < 2 sek., diureser > 1 ml/kg/time og normal cerebral tilstand.
Adjuverende akut behandling
Ved tegn på shock refraktær for væskeresuscitation eller overhydrering.
- Opstart infusion noradrenalin 0,1 mg/kg/min til effekt og titrer herefter (kan startes på perifer eller intraossøs adgang)
- Overvej behov for intubation, a-kanyle, CVK og/eller overflytning til højere specialiseret behandlingssted (Børneintensiv)
- Overvej differentialdiagnoser ved vedvarende tegn på hypovolæmisk shock, herunder andre shock typer eller kombinationer af shock. Transthorakal EKKO bør udføres af højeste lokale kompetence.
Kliniske tegn på overhydrering inkluderer:
Hepatomegali, øget respirationsarbejde, tiltagende desaturation (OBS: gradvis øgning af FiO2 kan maskere dette), stase på røntgen thorax/UL lunger. Særligt ved små børn kan ses periorbitale ødemer, ødemer af genitalia eksterna og/eller spændt fontanelle.
Valg af resuscitationsvæske:
Vi rekommanderer brug af balanceret krystalloid frem for isotonisk 0.9% NaCl til den initiale væskeresuscitation af børn med hypovolæmisk associeret organ dysfunktion.
Når man sammenligner brug af balancerede krystalloider med isotonisk 0.9% NaCl til væske resuscitation hos børn, er der en stigende grad af evidens, der tyder på at brug af isotonisk 0.9% NaCl er associeret med hyperkloræmisk acidose, systemisk inflammation, akut nyreskade, koagulopati og måske øget mortalitet.
Kardiogent shock
Årsager
- Arytmier (bradykardi (AV-blok), takykardi (SVT, VT/VF))
- Højresidigt svigt (perikardieeksudat, pulmonal hypertension, lungeemboli)
- Venstresidigt svigt (myokardit, kardiomyopati, sepsis)
- Biventrikulært svigt (septisk kardiomyopati, acidose, forgiftning, traume/hjertekontusion)
- Hjerteklapsygdomme
- Strukturelle hjertesygdomme
Symptomer
- Vedvarende hypotension, trods relevant væskebehandling
- Cyanose og kolde/blege ekstremiteter
- Oliguri
- Påvirket bevidsthed
Akut behandling
- Organunderstøttende (sedation, intubation, normotermi evt. køling til 36 oC)
- Restriktiv væsketerapi med balanceret krystalloid. Intravenøs bolus 5-10 ml/kg over 30 min
- Diuretika: Furosemid 0,25-1 mg/kg (over 3-5 min) som iv. bolus eller infusion 0,1-1 mg/kg/t.
Ved mistanke om kardiogent shock og inden opstart af specifik behandling (se nedenfor) bør der konfereres med højtspecialiseret afdeling. Hvis tilstanden ikke hurtigt stabiliseres (få timer), vil der altid være behov for overflytning til højtspecialiseret afdeling.
Bradykardi
- Isoprenalin 0,02 – 0,2 µg/kg/min, optitreres til ønsket effekt
- Ekstern pacing til alderssvarende frekvens (kræver at barnet er sederet)
Takyarytmi
- Vagusstimulation, f.eks. isposer og/eller carotismassage
- Adenosin til at bryde eller identificere rytme (husk at tage EKG under administration). Gives som hurtig iv. bolus efterfulgt af skyl og kan gentages ved manglende effekt
- dosis 0,1 mg/kg
- dosis 0,2 mg/kg (max. 6 mg)
- dosis 0,4 mg/kg (max. 12 mg)
- Cordarone infusion 25 µg/kg/min i max 4 timer, gerne kortere, hvis passende frekvens indtræder før. Derefter 5-15 µg/kg/min.
- DC-konvertering. Der er risiko for, at takyarytmi kan slå over i bradyarytmi (ekstern pacing kan blive nødvendigt). 0,5-1 joule/kg i generel anæstesi, evt. kraftig sedation. Øg joule ved manglende effekt til max 4 joule/kg
- Overvej efter konsultation med relevant kompetence at opstarte Digoxin og/eller metoprolol
Højresidigt hjertesvigt
- Optimer preload. Forsigtig væske-load (IV bolus 5-10 ml/kg over 30 min)
- Sænk afterload (pulmonal vaskulær resistens, PVR). Ilttilskud, hyperventilation for at modvirke en evt. metabolisk acidose (PCO2 lavt i normalområdet), infusion eller inhalation med prostacyclin epoprostenol (Flolan) eller inhaleret nitric oxide (iNO) 3-20 ppm (start højt og trap langsomt ud, når stabil). Sænker alle PVR.
- Optimer højre ventrikels kontraktilitet. Vælg det medikament, du kender bedst, afvent ikke anlæggelse af CVK og overvej at seponere ved takyarytmi
- Infusion Dobutamin (1-10 µg/kg/min)
- Infusion Adrenalin (0,05-0,2 µg/kg/min)
- Infusion Dopamin (1-10 µg/kg/min)
- Ved lavt systemisk BT og tegn på at organerne ikke tåler dette (laktat stigning, lav SvO2 eller kliniske tegn): Tillæg Noradrenalin – start i lavt (fx 0,01-0,05 µg/kg/min og optitrer)
Venstresidigt hjertesvigt
- Optimer preload. Forsigtigt væske-load (IV bolus 5-10 ml/kg over 30 min)
- Understøt højre ventrikel (se ovenfor)
- Optimer venstre ventrikels kontraktilitet. Vælg det medikament, du kender bedst, afvent ikke anlæggelse af CVK og overvej at seponere ved takyarytmi samtidig med at venstre ventrikels afterload reduceres
- Infusion Dobutamin (1-10 µg/kg/min)
- Infusion Adrenalin (0,05-0,2 µg/kg/min)
- Infusion Dopamin (1-10 µg/kg/min)
- Infusion Milrinone (0,4 µg/kg/min – fast dosis), kan evt. forudgås af bolus Milrinone (20-50 µg/kg over 10 min), da effekten ved infusion indtræder efter 4 – 6 timer
- Ved lavt systemisk BT, som ikke tolereres klinisk/paraklinisk, kan Noradrenalin med forsigtighed tillægges. Dette kan dog forværre LV svigt
Biventrikulært svigt
- Optimering med ovenstående (RV og LV svigt)
Hjerteklapsygdomme
- Hvis de er betydende og har medført svigt: Konferér med højt specialiseret enhed
Strukturelle hjertesygdomme
- Ved mindste mistanke om ductusafhængigt kredsløb hos børn under 3 mdr. opstartes Prostaglandin E uden yderligere forsinkelse. Infusion med Prostaglandin E (Startdosis 0,05 – 0,1 µg /kg/min. (kan ofte reduceres til 0,01 mg/kg/min når tilstanden er stabil).
Obs på risiko for apnø ved behandlingen.
Hvis ovenstående behandling ikke bedrer tilstanden umiddelbart, kontaktes RH mhp. overflytning og/eller mekanisk støtte / ECMO.
Højtspecialiseret afdeling bør også kontaktes ved mistanke om kardiogent shock og inden avanceret inotropi eller lign. opstartes. Børne-hjerteintensiv på RH: tlf.: 35 45 16 98
Blandingsvejledninger til infusion
| • Noradrenalin
Noradrenalin 0,06 mg/kg blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. 1 ml/time af blandingen = 0,01 μg/kg/min. Vanlig dosis 0,05 – 0,5 μg/kg/min. Højere dosis kan være nødvendigt, men effekten bør sikres. • Adrenalin Adrenalin 0,06 mg/kg blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. 1 ml/time af blandingen = 0,01 μg/kg/min. Vanlig dosis 0,05 – 0,5 μg/kg/min. Højere dosis kan være nødvendigt, men effekten bør sikres. • Dopamin Dopamin 6 mg/kg blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. 1 ml/time af blandingen = 1 μg/kg/min. Vanlig dosis 2 – 10 μg/kg/min. • Dobutamin Dobutamin 6 mg/kg blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. 1 ml/time af blandingen = 0,1 μg/kg/min. Vanlig dosis 2 – 10 μg/kg/min. • Milrinone Milrinone 0,6 mg/kg blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. 1 ml/time af blandingen = 1 μg/kg/min. Vanlig dosis 0,1 – 0,5 μg/kg/min. • Isoprenalin Isoprenalin 0,06 mg/kg blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. 1 ml/time af blandingen = 0,01 μg/kg/min. Vanlig dosis 0,02 – 0,2 μg/kg/min. • Vasopressin Vasopressin 20 U/ml. 2 ml (40U) blandes med isoton NaCl eller glucose 5 % til et totalvolumen på 100 ml. Koncentration 0,4 U/ml. Vanlig dosis 0,1 – 0,5 μg/kg/min. • Phenylephrin (Metaoxedrin) 0,1 mg/ml. Gives ufortyndet. Vanlig dosis 0,1 – 0,3 μg/kg/min. |
The Phoenix Sepsis Score – Sepsis definition
Phoenix Sepsis Score er udviklet til at identificere potentielt livstruende organsvigt hos børn med mistænkt eller bekræftet infektion. Indholdet i scorerne afhænger af barnets respiratoriske, kardiovaskulære, neurologiske og koagulations status. Sepsis blev defineres som en Phoenix Sepsis Score på mindst 2 point, og septisk shock identificeres med mindst 1 point i den kardiovaskulær komponent. Scoren kan bruges på børn under 18 år og kan ikke bruges neonatalt.
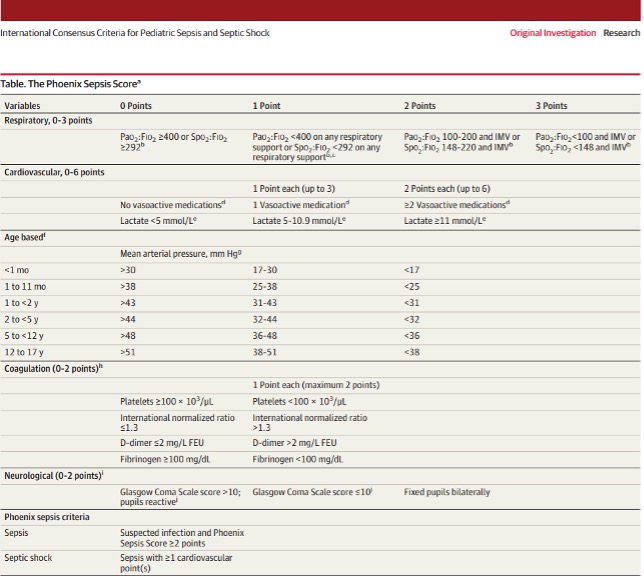
Tabel 13 The Phoenix Sepsis Score
Referencer:
- Singh et al.: ”Recommendations for hemodynamic monitoring for critically ill children – expert consensus statement issued by the cardiovascular dynamics section of the European Society of Paediatric and Neonatal Intensive Care (ESPNIC)”. Cirtical Care (2020) 24:620.
- Weiss SL, Peters MJ, Alhazzani W, Agus MSD, Flori HR, Inwald DP, et al. “Surviving sepsis campaign international guidelines for the management of septic shock and sepsis-associated organ dysfunction in children. Vol. 46, Intensive Care Medicine. 2020. 10–67 p.
- Schlapbach, L. J. et al. Society of Critical Care Medicine Pediatric Sepsis Definition Task Force. International Consensus Criteria for Pediatric Sepsis and Septic Shock. JAMA331, 665–674 (2024)
- https://danskallergi.dk/fagligt/instrukser-og-vejledninger/anafylaksi/
- https://ugeskriftet.dk/videnskab/anafylaksi-hos-born-og-voksne
- https://www.uptodate.com/contents/anaphylaxis-emergency-treatment?search=anaphylaxis%20children&topicRef=391&source=see_link
- https://www.resus.org.uk/library/additional-guidance/guidance-anaphylaxis/emergency-treatment
- Cardona V et al.: World allergy organization anaphylaxis guidance 2020. World Allergy Organ J. 2020 Oct 30;13(10):100472
- Muraro A et al.: European Academy of Allergy and Clinical Immunology, Food Allergy, Anaphylaxis Guidelines Group. EAACI guidelines: Anaphylaxis (2021 update). Allergy. 2022 Feb;77(2):357-377
- Shaker MS et al.: Anaphylaxis-a 2020 practice parameter update, systematic review, and Grading of Recommendations, Assessment, Development and Evaluation (GRADE) analysis. J Allergy Clin Immunol. 2020 Apr;145(4):1082-1123
- Carter MC et al.: Idiopathic anaphylaxis yardstick: Practical recommendations for clinical practice. Annals of Allergy, Asthma & Immunology. 2020 Jan 1;124(1):16-27
- Gavin Wooldridge: “Pediatric cardiogenic shock”
- Ron Waksman: “Standardized Definitions for cardiogenic shock research and mechanical circulatory support”.
- Susannah Fleming: “Normal ranges of heart rate and respiratory rate in children from birth to 18 years: a systematic review of observational studies”
Kapitel 7 – Abdominalt / Ernæring
Få ernæring til at fungere – mulige tiltag ved manglende GI-funktion
Reduktion af mængde:
Reducer til sidste tolereret mængde – revurder efter 2 – 4 timer,
- Pause 2 – 4 timer og genoptag sidste tolereret mængde, revurder efter 2 – 4 timer
- Pause i 24 timer (evt. trofisk ernæring) og gentag optrapning.
- Overvej kontinuerlig administration
Forebyggende ved behandling med opioider:
- Naloxon: po/ps 0.01 mg/kg x 2
- Methylnaltrexon sc: max 12 mg hv. 2. dag
Laksantia:
- Movicol: po/ps ½ brev junior x 1 (mature børn > 28 dg), 1 brev junior x 1 – 2 (børn 2 – 11 år). 2 brev junior x 2 -3 (børn > 11 år).
- Actilax: po/ps Børn < 4 år; 250 mg/kg x 1 (1 dråbe pr. 2 kg), Børn 4 – 10 år; 2,5 – 5 mg (5 – 10 dråber) x 1. Børn > 10 år; 5 – 10 mg (10‐20 dråber) x 1
Prokinetika:
- Erythromycin: iv 1 – 3 mg/kg x 4
Antiemetika:
- Dexamethason: iv 0,15 mg/kg x 1, max 8 mg. Ondansetron: 0,1 – 0,2 mg/kg x 1 – 3, max 4 mg
Mobilisering: Efter sygelighed og sedationsgrad
OBS: Ernæring til abdominal kirurgisk patienter foregår altid i samarbejde med kirurg.
Generelle ernæringsbehov
Beregn ernæringsbehovet ud fra fase af kritisk sygdom, habituelle tørvægt og ernæringstilstand. Opbyg ernæringen langsomt efter skema:
| Fase | % af ernæringsmål | |
| Dag 1-3 | Resuscitation | 0 -> max. 60 |
| Dag 4-7 | Stabilisering | 60 -> 100 |
| Dag 7+ | Stabil | 100 |
Enteral ernæring
Overvej kontra(relative)-indikationer:
- Obstruktion / Ileus/ Tarmiskæmi
- Øvre GI blødning
- Nylig abdominalkirurgi (plan for enteral ernæring i samråd med kirurg)
- Dekompenseret shock med højt inotropi behov
- Svær acidose
Sonde anlægges:
- Relative kontraindikationer: Ansigt / basis kranie fraktur. Kirurgi svt mund, svælg, næse, esofagus, ventrikel.
- Udmål og kontroller placering – noteres.
Enteral ernæring kan startes som trofisk ernæring hvorefter fødetolerance vurderes efter 24 – 48 timer, bolus administration foretrækkes
Bolus: 1-2 ml/kg hver 2 – 4. time, 20 – 40 ml ved > 40 kg
Kontinuerligt: 0,5-1 ml/kg/time, 10 ml/time ved > 40 kg
Volumen øges gradvist iht. acceptable aspirater med henblik på ernæring indtil planlagt mængde er opnået.
Bolus: øges med 5 – 10 ml/kg hver. 4. time.
Kontinuerligt: øges med 1 – 2,5 ml/kg/time, hver 4. time
Aspirater kontrolleres hver 2 – 4. time. Replaceres op til acceptabelt volumen.
5 ml/kg accepteres, max 200 ml (> 40 kg)
OBS: Enteral ernæring og tilladelige aspirater hos abdominal kirurgiske patienter aftales med kirurg.
OBS: Under optrapning af enteral ernæring gives glucose eller PN til ønsket kalorie mængde.
Blodsukkerkontrol
Det anbefales generelt at holde BS 6 – 10 mmol/l.
Hos småbørn (< 1 år) skal rettes særlig opmærksomhed på tilstrækkelig glukose tilbud og blodsukkerkontroller.
Anbefalet glukose tilbud til kritisk syge børn afhænger af vægt og sygdomsfase (mg/kg/min):

HYPOGLYKÆMI: BS < 2,6 mmol/L
ABC-vurdering + iv adgang. Behandling må ikke forsinkes af yderlig udredning.
Manglende iv adgang:
Vågen og samarbejdende barn: Peroral sukkerholdige væske (mælkemåltid børn < 1 år)
CNS påvirket: Glucagon im (<25 kg: 0,5 mg, >25 kg: 1,0 mg)
IV adgang:
- 2,0 ml/kg glucose 10% bolus
- Opstart at inf glucose svt 4 – 8 mg/kg/min (glucose10%: 2.4 – 4,8 ml/kg/time)
- Sikre stabilt enteral indtag.
- BS kontrolleres hv. 10 min indtil stabilt > 3.0, ved BS under 2,6 gentages bolus iv glucose 10% + evt øget konc af glucose inf.
- Behandling fortsættes til stabilt BS > 3,0 mmol/L, stabil, klinisk bedring og genoptaget enteralt indtag.
OBS: Udredning.
OBS: Glucose 10% er en hyperton væske.
Parenteral ernæring
Overvej indikation:
- Gives som regel ikke i den første uge af kritisk sygdom
- Ved ikke fungerende GI-kanal
- Når ernæringsbehov ikke kan nås efter første uge
- Øget ernæringsbehov eller tab som ikke kan erstattes enteralt
Overvej kontra(relative) indikationer:
- Shock
- Svære syre/base- eller elektrolytforskydninger
- Svær trombocytopeni eller koagulopati
- Svær leverinsufficiens (pga. fedtindhold)
- Svær nyreinsufficiens (pga. proteinindhold)
- Allergi over for indholdsstoffer
Kontrol af blodprøver. Blodprøver tages efter 5 dage og min. hver uge efterfølgende.
- BS, S-triglycerid, ALAT, konj. bilirubin, S-Carbamid, Natrium, kalium, calcium, Hgb, albumin, Fosfat.
Komplikationer ved PN:
- Umiddelbare metaboliske forstyrrelser som hyper-/hypoglykæmi, elektrolytforstyrrelser og hypertriglyceridæmi.
- Refeeding syndrom; hypokaliæmi, hypomagnesæmi og hypofosfatæmi
- Kateterrelateret infektion; almindelig komplikation ved PN terapi hos børn, oftest Koagulase Negative Stafylokokker.
- Katetertrombose
- Kolestatisk icterus, PN-associeret leverpåvirkning (PNALD)
Parenteral ernæring optrappes over 3 døgn til den fulde planlagte mængde
Grafisk opsætning:


Generelle ernæringsbehov
En betydelig andel af kritisk syge børn er fejlernærede allerede ved indlæggelsen på intensiv afdelingen, op mod 16-20 % er underernærede, og ca. 14 % er overvægtige (danske data foreligger ikke). Både underernæring og fedme er associeret med dårligere outcome, herunder øget dødelighed, højere risiko for infektioner og længere indlæggelsestid. Ernæring er derfor en central del af intensivbehandlingen, om end der fortsat er store udfordringer og uafklarede spørgsmål, især når det kommer til vurdering af energibehovet. Energibehovet varierer betydeligt både fra barn til barn, men også hen over forløbet af kritisk sygdom.
Akut kritisk sygdom kan inddeles i 3 faser
- En tidlig fase med hyperinflammation, katabolisme, metabolisk ustabilitet og eskalerende behov for organunderstøttende behandling.
- En stabiliserende fase med aftagende organunderstøttende behandling.
- En stabil fase med anabolisme, ny vækst og mobilisering.
Ernæringsbehandlingen til det kritisk syge barn skal målrettes disse faser. Figur 5 viser en konceptuel illustration af energibehovet, og strategien for ernæringsbehandling henover de forskellige faser.

Figur 5 Metabolisme under forskellige faser af kritisk sygdom. (28)
Den endogene energiproduktion kan dække over halvdelen af energibehovet under akut kritisk sygdom, hvorfor der er risiko for overernæring ved for tidlig og for aggressiv ernæring. De internationale guidelines anbefaler, på basis af good clinical practice, at screene børnene for risiko for underernæring ved indlæggelsen på intensiv. Dette kan gøres ved angivelse af z-scores på højde og vægt i forhold til alder og køn. Det største randomiserede studie om effekten af tidlig fuld ernæring ved parenteralt tilskud i den første uge fandt, som det også er vist hos voksne, ingen gavn, men derimod dårligere outcome ved tidlig fuld parenteral ernæring. Denne effekt kunne påvises i alle aldersgrupper, inkl. mature nyfødte, men også hos børn med øget risiko for underernæring. Den seneste litteratur understøtter tidlig opstart og optimering af enteral ernæring, også hos mere komplekse patient populationer, hvor det tidligere har været anset som kontraindiceret, f.eks. patienter med behov for farmakologisk og ekstrakorporal kredsløbsunderstøttende behandling. Samlet set synes ernæringsscreening med henblik på at øge behandlingen tidligt med parenteralt tilskud af makronæringsstoffer unødvendig, og der vil kun i særlige situationer være behov for tidlig opstart af parenteral ernæring, f.eks. ved absolutte kontraindikationer til enteral ernæring eller visse metabolske tilstande. Det anbefales i stedet gradvist at øge den perorale/enterale ernæring gennem den første uge, samt give tilskud af mikronæringsstoffer.
Energibehov, indirekte kalorimetri

For at opnå en mere målrettet ernæringsbehandling, og undgå svær under- eller overernæring, anbefales stærkt at måle energibehovet (Resting Energy Expenditure – REE) ved indirekte kalorimetri (IC) især hos børn med mere end 7 dages indlæggelse. Dette er velvidende, at IC er behæftet med 10-15% måleusikkerhed og at der endnu ikke findes randomiserede studier med patientrelevante outcomes ved IC vs. beregninger ved formler. Målemetoden er desværre generelt ikke særligt udbredt på de danske intensivafsnit. Har man ikke et kalorimeter til rådighed anbefales at anvende Schofields formler.
Tommelfingerregel
Mere simpelt kan kropsarealet (BSA) være vejledende. Er BSA eksempelvis 0,45 m2, tyder det på et REE på 450 kcal.
Specifikke ernæringsbehov
Kulhydratbehov
Mængden af glukose givet intravenøst skal balanceres mellem energibehovet, den endogene glukose produktion og oxidation, sygdomsfase, risiko for overernæring, hyperglykæmi samt det perorale eller enterale tilbud. Overdreven intravenøs glukose behandling kan medføre øget lipogenese, samt forårsager bivirkninger såsom dyslipidæmi, hepatisk steatose og hyperglykæmi. Under den akutte fase af kritisk sygdom, kan høje glukoseniveauer forværre de metaboliske komplikationer, herunder insulinresistens og nedsat leverfunktion. I en akut postoperativ setting har mængden af glukose indtag ikke vist sig at påvirke protein metabolismen. En reduktion af glukose administrationen har vist at kunne regulere blodglukoseniveauerne sikkert og reducere komplikationer, især i den akutte fase. Efterhånden som patienten kommer sig, mindskes insulinresistensen, hvilket tillader en gradvis forøgelse af glukoseindtaget for at understøtte rehabilitering og vækst. PEPaNIC studiet underkender faren ved energideficit gennem den første uge, hvorfor det anbefales at sigte lavt med intravenøs glukose dosering titreret med henblik på normoglykæmi (Endokrinologi side 94).
Blodsukkerkontrol
Hyperglykæmi er et naturligt stressrespons på kritisk sygdom. Hvorvidt en aktiv regulering af blodglukose (stram blodsukker kontrol) kan bedre outcome, har været forsøgt belyst. De første studier har dog vist modstridende resultater. Initielt indikerede en stram blodsukker kontrol, opnået ved insulin behandling, et bedre outcome ved lavere dødelighed, infektionshyppighed og kortere intensivophold, men med en øget forekomst af hypoglykæmi. Efterfølgende studier har ikke kunne genfinde den samme association, og risikoen for alvorlig hypoglykæmi har vagt bekymring. En meta-analyse fra 2018 konkluderede, at stram blodsukker kontrol hos kritisk syge børn ikke var forbundet med lavere dødelighed, lavere forekomst af sepsis eller kramper, men betød markant øget risiko for hypoglykæmi. Analysen peger dog på en mulig reno-protektiv effekt (nedsat behov for dialyse), primært hos de hjertekirurgiske børn. Et multicenter studie finder ingen fordel ved regulering af blodsukker til lavere niveauer end 6–10 mmol/L, hvorimod en øvre tærskel værdi for hyperglykæmi ikke er undersøgt.

Tabel 14 Anbefalet glukose tilbud til kritisk syge børn afhængig af vægt og sygdomsfase (mg/kg/min). (34)
Hypoglykæmi defineres som BS < 2,6 mmol/L hos børn. Dog er det foreslået i litteraturen, at blodsukker holdes over 2,8 mmol/L hos nyfødte og 3,6 mmol/L hos børn.
Barnet vurderes efter vanlig ABC-tilgang inkl. behov for iv adgang. Yderlig udredning af udløsende årsag må ikke forsinke den akutte behandling. Det vågne og samarbejdende barn gives straks sukkerholdige væske enteralt (mælkemåltid ved børn< 1 år). Hos det CNS påvirkede barn gives iv glucose 10% 8100 mg/ml), bolus 3 ml/kg (ved manglende iv adgang kan glucagon gives initielt). Der fortsættes med iv infusion, og blodsukker kontrolleres hvert 10 minut, indtil det sikkert ligger over 3.0. Behandling fortsættes, indtil der er klinisk bedring, og barnet kan indtage stabilt enteralt.
Proteinbehov
Under den katabole fase ved akut kritisk sygdom vil proteolyse resultere i tab af muskelmasse, hvilket kan have betydning for morbiditet såvel som mortalitet. For at modvirke dette forsøges det at opretholde en positiv proteinbalance. Hos stabile kritisk syge børn anbefales det derfor tidligt i forløbet at give sondeernæring indeholdende protein. Den optimale proteinmængde kendes ikke hos børn. Det anbefales, at den daglige proteinmængde hos børn minimum er 1,5 g/kg/d, da studier har fundet, at det forebygger negativ protein balance. Men studier med mere patientrelevante outcomes mangler. Sammensætningen af aminosyrer skal afspejle den normale kost. Det er væsentligt, at man får tilført de essentielle aminosyrer. De semi-essentielle aminosyrer regnes imidlertid også for essentielle hos kritisk syge børn.
Lipidbehov
Lipider har en højere kalorie tæthed end protein og kulhydrat og er en vigtig bestanddel af cellemembraner, hormoner, vitaminer og andre biokemiske processer. Derfor indgår lipider også som en bestanddel af den enterale ernæring, hvoraf nogle er essentielle (Omega-3 og Omega-6). Det samlede kaloriebidrag fra lipider anbefales at være 20-30% af REE. For stort indtag kan medføre stigning af triglycerid og påvirkning af leveren. Hos børn sederet i flere dage med høje doser Propofol, kan det være relevant at måle triglycerid og leverenzymer.
Mikronæringsstoffer og immunonutrition
Fra et fysiologisk perspektiv virker det meningsfuldt at give mikronæringsstoffer gennem alle faser af kritisk sygdom. Men da der indtil videre ikke findes randomiserede studier om effekten af behandling med mikronæringsstoffer, er de aktuelle anbefalinger bygget på expert opinion og de generelle anbefalinger for raske børn.
Der er ikke indikation for immunonutrition som glutamin, Omega 3-fedtsyrer, Arginin eller Immunonutrition cocktails til kritisk syge børn.
Følgende stoffer er til rådighed i Danmark:
| Anbefalede døgn doser af mikronæringsstof tilskud til børn | ||||
| Vægt | <5 kg | 5–12 kg | 12–30 kg | >30 kg |
| Peroral/enteral | Fuld dosis sondeernæring dækker normalbehov for mikronæringsstoffer | |||
| Multivitaminpille | Nej | Nej | Ex. Livol Multi 3-11 år | Ex. Apovit Multi > 11 år |
| Vitamin flydende | Nej | Nej | Mivitotal 5-10ml | Mivitotal 15 ml |
| D vitamin | >2 uger: hele året | > 4 år: okt – april | ||
| Infusion | Skal tilsættes alle infusioner af makronæringsstoffer | |||
| Cernevit Komb® | Nej | Nej | Nej | 1 Hætteglas |
| Vitalipid® Fedt opløselige | 4 ml Vitalipid® Infant | 10 ml Vitalipid® Infant | 10 ml Vitalipid® Infant | 10 ml Vitalipid® Adult |
| Soluvit® Vandopløselige | 1.5 ml/kg | 1.5 ml/kg (max 8 ml) | 8 ml | 10 ml |
| Peditrace®. Sporstoffer | 1 ml/kg | 1 ml/kg (max 10 ml) | <20 kg: 10 ml
>20 kg: Tracel Novum |
Tracel Novum® 10 ml |
Tabel 15 Anbefalede døgn doser af mikronæringsstof tilskud til børn
Enteral ernæring
Der findes aktuelt ingen klar definition på gastrointestinal dysfunktion hos kritisk syge børn, men symptomer, som forhindrer enteral ernæring, er rapporteret hos 40 – 80 %. Kvalme, diarré, aspirater/ventrikel retention og opdrevet abdomen er de hyppigst rapporterede symptomer på intolerance overfor enteral ernæring.
Anlæggelse og kontrol af ventrikelsonde
Indikationer:
Tilbyde sufficient næring via gastrointestinal kanalen, aflastning af ventriklen ved ventrikelretention eller store aspirater, aflastning af ventriklen for luft, eksempelvis under CPAP-behandling.
Sonden anlægges efter læge ordination. Proceduren kan i ukomplicerede tilfælde varetages af sygeplejersken og anlægges primært via næsen. Relative kontraindikationer er svær ansigts- og kranieskade, hvor basis kranii er involveret samt efter kirurgi svt. mund, svælg, esophagus og ventrikel. I disse tilfælde skal sonden anlægges af relevant speciale.
Sondestørrelsen justeres ud fra barnets vægt og primære formål – se tabel 15. Placering af sonden ved næsefløjen findes ved udmåling afstanden fra næse til øreflip og herfra til min. 1.5 cm under processus xiphoideus. Kontrol af sondens placering foretages ved røntgen, hvor spidsen skal ses placeret i ventriklen under diafragma-niveau, og mærket ved næsefløjen noteres i journalen. Der aspireres altid forud for administration i sonden.

Tabel 16 Forslag til valg af sondestørrelse
Sondens placering noteres i journalen.
Kontrol af sonde placering:
1. Aspirer maveindhold
2. Ph-måling af aspirat. Ph < 5,5
3. Ved Rtg af Thorax
4. Sprøjt luft i sonden og lyt efter bobler over epigastriet (ingen garanti)

Figur 6 Anlæggelse og kontrol af ernæringsonder for neonatale børn – Guideline ved Dansk Pædiatrisk Selskab
Ventrikelretention:
Ventrikelaspirat eller gastrisk residualvolumen (GRV), anvendes ofte som surrogatparameter for ventrikel tømning / graden af ventrikel retention, men ingen klar definition er angivet hos børn. Øget GRV forekommer hos op til 50% af kritisk syge børn og omfatter både den administreret enterale ernæring og produktionen af ventrikelsekret. Der er ikke en lineær sammenhæng mellem GRV og graden af forsinket ventrikeltømning, og målingen af GRV er behæftet med usikkerhed (påvirkes af lejring, placeringen og diameter af sonden, type af sonde, sygeplejerskens teknik samt administration af ernæring – bolus eller kontinuerlig).
Forslag: Kontrol af GRV hver 2 – 4 time, accept af GRV 5 ml/kg, max 200 ml. (> 40 kg)
OBS: Hos abdominal kirurgiske børn aftales maksimal indhold i ventriklen med kirurg.
Obstipation:
Forekommer hyppigt hos kritisk syge børn, og defineres ofte ved manglende afføring i > 3 dage. Opioider anvendes ofte i behandlingen af kritiske syge børn enten med henblik blik på smertelindring eller analgosedation, hvorfor risikoen for opioid-induceret obstipation er høj. Behandling med sedativa, vasopressorer og relaksantia, samt immobilisering er også disponerende faktorer. Særligt hos børn er forebyggelse og behandling af obstipation vigtig, idet et opdrevet og meteoristisk abdomen i høj grad kompromitterer respiratoraftrapning og mobilisering med risiko for udvikling af yderlige komplikationer.
Laksantia:
Tidlig opstart af forebyggende behandling mod obstipation er vigtig, særligt hos børn som er immobiliserede og i opioid behandling. Laksantia som Movicol og Actilax kan med fordel startes samtidig med enteral ernæring og reguleres efter effekt.
Antiemetika:
Dexamethason: Virkemekanismen for den antiemetiske effekt af glukokortikoider er ukendt. Effekt og anvendelse er bedst belyst ved kemoinduceret kvalme og opkastninger, men anvendes i stigende udstrækning også ved postoperativ kvalme og opkastning, og kan med fordel kombineres med anden antiemetisk behandling på grund af den synergistiske effekt.
OBS: Anden immun-supprimerende behandling, pågående infektion og blodsukker.
Ondansetron: Ondansetron er en 5-HT3 antagonist (serotonin receptor subtype) som findes flere steder i CNS, blandt andet svt. terminale ganglion af n. vagus. Effekten af Ondansetron optimeres ved samtidig indgift af Dexamethason.
Prokinetika:
Erytromycin: Erythromycin er et makrolidantibiotikum, der fungerer som en motilinagonist, og dermed øger den gastrointestinale (GI) motilitet. Motilin er et hormon, som udløser glatmuskelkontraktioner. Randomiserede studier har vist forbedret fødeintolerance hos pædiatriske patienter inkl. neonatale og spædbørn ved behandling med erythromycin sammenlignet med placebo. Erythromycin kan anvendes både intravenøst og enteralt, og doser mellem 1,5 mg/kg til 12,5 mg/kg hver 6. time har været anvendt. Erythromycins effekt er dosisafhængig, og lavere doser (1-3 mg/kg) kan øge GI-motilitet uden at øge forekomsten af bivirkninger (14). Behandling over 2-3 dage bør undgås.
Metoclopramid: Ikke til børn < 1 år. Anvendes generelt med forsigtighed.
Opioid antagonister:
Naloxon er en perifert virkende m-opioid receptor antagonist. Oralt administreret Naloxon har en betydelig first-pass metabolisme i leveren og derfor kun en bio-tilgængelighed på ca. 1 -2 %. På grund af den begrænsede systemiske optagelse er den primære effekt i mave-tarmkanalen med minimal risiko for revertering af den analgetisk effekt. Oral naloxon synes sikkert at anvende, forsigtighed tilrådes ved leverpåvirkning, særligt ved tilstande med øget shunt. Dog er der ingen klare anbefalinger på dosis hos børn.
Methylnaltrexon er ligeledes en perifert virkende m-opioid receptor antagonist, som anvendes til opioid induceret forsinket ventrikeltømning og nedsat tarmperistaltik. Grundet stoffets kvaternære struktur passerer methylnaltrexon ikke blod-hjerne-barrieren, hvorfor den analgetiske effekt af opioid ikke påvirkes. Man skal være opmærksom på dette hos patienter, hvor blod-hjerne barrieren ikke er intakt. Da Methylnatrexon gives subkutant, er det ikke et oplagt første valg til børn.
| Anbefalede medicindoser mod obstipation, ventrikelretention, kvalme og opkastning | ||||
| Obstipation | ||||
| Osmotisk effekt | Movicol junior | >28 dage: ½ brev x 1 | 2-11 år: 1 brev x 1 – 2 | >11 år: 2 brev x 2 -3 |
| Peristaltik fremmende | Actilax | < 4 år: 250 mg/kg x 1
(1 dråbe pr. 2 kg) |
4 – 10 år: 2,5 – 5 mg
(5 – 10 dråber) x 1 |
>10 år; 5 – 10 mg
(10‐20 dråber) x 1 |
| Opioid antagonister | Naloxon po / ps | 0,01 mg/kg x 2 | 0,01 mg/kg x 2 | 0,01 mg/kg x 2 |
| Methylnaltrexon sc max 12 mg | 0,15 mg/kg hver 2. dag | 0,15 mg/kg hver 2. dag | 0,15 mg/kg hver 2. dag | |
| Ventrikelretention | ||||
| Prokinetikae | Erythromycin | 1 – 3 mg/kg x 4 | 1 – 3 mg/kg x 4 | 1 – 3 mg/kg x 4 |
| Metoclopramid, helst ikke | < 1 år: Nej | 0,1-0,15 mg/kg max x3 | 0,1-0,15 mg/kg max x3 | |
| Kvalme og opkastning | ||||
| Serotonin antagonist | Ondansetron iv, max. 4 mg | 0,1 – 0,2 mg/kg x 1 – 3 | 0,1 – 0,2 mg/kg x 1 – 3 | 0,1 – 0,2 mg/kg x 1 – 3 |
| Steroid | Dexamethason iv, max 8 mg | 0,15 mg/kg x 1 | 0,15 mg/kg x 1 | 0,15 mg/kg x 1 |
Tabel 13 7 Anbefalede medicindoser mod obstipation, ventrikelretention, kvalme og opkastning
Enterale og orale ernæringsprodukter
Orale og enterale ernæringsprodukter findes som modermælk, modermælkserstatning, sondeernæring, drikke eller i pulverform. Produkterne skal som fuld-gyldige indeholde alle essentielle makro- og mikronæringsstoffer nødvendige for aktuelle fysiologiske behov og vækst i aldersgrupperne 0-1, 1-6, 6-12 og >12 år. Ikke-fuldgyldige produkter, i form af juicedrikke eller special is, kan være lettere at indtage, men har ernæringsmæssige mangler. Standard produkterne er oftest baseret på helprotein fra valle men med lavt eller ingen laktoseindhold, og er uden gluten. Spaltede (peptidbaserede) ernæringsprodukter anvendes ved malabsorption eller kompromitteret tarmsystem. Energitætheden i sondeernæring og drikke varierer i 3 niveauer: Lav med 60 kcal/100 ml, standard med 100-120 kcal/100ml eller høj 150 kcal/100ml. Proteinindholdet er 2,0-5,7 g/100 ml. Energitætte -men ikke højprotein- produkter anvendes til børn <1 år. Fra 12-årsalderen (>45 kg) kan voksenprodukter anvendes. Protein- og energitætte produkter kan anvendes ved behov for væskerestriktion, men det øgede indhold af kulhydrater og aminosyrer medfører høj osmolaritet og kan give bivirkninger i form af dumping og diarré. Anvendelsen af fiberholdige produkter er udbredt til børn >1 år, men der savnes studier på kritisk syge børn. Især må der udvises tilbageholdenhed ved hæmodynamisk instabilitet og højdosis vasopressorterapi.
Der findes produkter med specielle sammensætninger i typen af fedtstof, protein eller saltindhold til patienter med bestemte sygdomme eller mangeltilstande.
Parenteral ernæring (PN)
I de tilfælde ernæringsbehovet ikke nås kan overvejes parenteral ernæring, men timingen for opstart af PN skal overvejes. Generelt anbefales at vente med at starte PN i op til syv dage, såfremt barnet ikke kan opnå 80% af sit ernæringsbehov enteralt på dette tidspunkt og forventet varighed af PN er mere end tre dage.
| Indikationer | Kontraindikationer |
| Ikke fungerende GI-kanal | Shock |
| Når ernæringsbehov ikke kan nås | Svære syre/base- eller elektrolytforskydninger |
| Øget ernæringsbehov eller tab som
ikke kan erstattes enteralt |
Svær trombocytopeni eller koagulopati |
| Svær leverinsufficiens (pga. fedtindhold) | |
| Svær nyreinsufficiens (pga. proteinindhold) | |
| Allergi over for indholdsstoffer |
Tabel 18 Indikationer og kontraindikationer for parenteral ernæring
Parenterale ernæringsprodukter er overordnet sammensat af en fedtemulsion (f.eks. SMOFlipid, Intralipid), glucose og aminosyrer (AmiPed, Vamin, Aminoven, Vaminolac). Man kan vælge at indgive hver kilde særskilt, men oftest vil de være samlet i standardblandinger, enten via sygehusapotekets egne PN-blandinger eller de i Danmark tilgængelige industrialiserede blandinger som Numeta eller SMOFKabiven. Sidstnævnte er først registreret fra 2 år og generelt først anbefalet, når barnet vejer mere end 25 kg, da proteinindholdet vil være en begrænsende faktor.
Bemærk at lipid emulsionen i SMOFKabiven og -lipid er sammensat af olivenolie, sojabønneolie, MCT (middelkæde triglycerider) samt fiskeolie, mens et produkt som Numeta er sammensat af olivenolie og sojaolie, og sidstnævnte derfor har en højere del af flerumættede fedtsyrer.
| Produkt | Volumen ml | Energi kcal/
100 ml |
Glucose
g/100 ml |
Aminosyrer g/100 ml | Fedt g/ 100 ml | Osmolaritet mOsm/L | |
| Numeta g16e | m. fedt | 500 | 103 | 15,5 | 2,6 | 3,1 | 1230 |
| u. fedt | 376 | 96 | 20,6 | 3,5 | 0 | 1585 | |
| Numeta g19e | m. fedt | 1000 | 114 | 19,2 | 2,3 | 2,8 | 1460 |
| u. fedt | 775 | 111 | 24,7 | 3 | 0 | 1835 | |
| SMOFKabiven | m. fedt | 493 | 110 | 12,7 | 5,1 | 3,8 | 1500 |
| u. fedt | 399 | 91 | 15,7 | 6,3 | 0 | – | |
| SMOFlipid | – | 100 | 200 | – | – | 20 | 380 |
| Glucose 50% | – | 100 | 200 | 50 | – | – | 2775 |
| Vamin 18 | – | 500 | 46 | – | 11,4 | – | 1130 |
Tabel 19 Tabel over hyppigt brugte kommercielle ernæringsprodukter og indhold. G/100 ml er færdigblanding.
Der skal sikres en central intravenøs adgang (f.eks. CVK, PiCC-line, long-line) for indgift og infusionen af PN bør planlægges til at løbe over 22-24 timer. PN kan undtagelsesvis gives perifert, men da er det vigtigt, at bruge produkter med osmolaritet mindre end 900mOsm/L, f.eks. SMOFKabiven perifer eller Numeta fortyndet med sterilt vand.
Følgende blodprøver bør tages:
| Blodprøver | Anvendes som en del af |
| BS | Glykæmisk kontrol |
| S-triglycerid, ALAT, konjugeret bilirubin | Undgå overdosering af lipid, opfange fedtbelastningssyndrom |
| S-Carbamid | Proteinbehov |
| Natrium, kalium, calcium | Elektrolythomeostase |
| Hgb, albumin | Hydrering |
| Fosfat | Opfange refeeding |
Tabel 20 Blodprøver der bør tages ved anvendelse af parenteral ernæring
Vitaminer og sporstoffer bør altid tilsættes PN-produktet, se skema i afsnit om mikronæringsstoffer.
Infusionshastigheden for PN skal fastsættes, og afhænger af hvilket produkt der vælges. Eksempler på infusionshastigheder:
| Numeta G16E | Numeta G19E | SMOFKabiven | |
| Vejledende maksimumhastighed / (ml/kg/t) | 5,5 (med fedt) | 4,6 (med fedt) | 2,4 |
| 5,8 (uden fedt) | 4,7 (uden fedt) | – | |
| Maksimal dosis pr. døgn / (ml/kg/døgn) | 96,2 (med fedt) | 83,6 (med fedt) | 35 |
| 72,3 (uden fedt) | 64,8 (uden fedt) | – |
Tabel 21 Infusionshastighed
Max. infusion for fedtemulsion er 4g/kg/døgn for børn 0-1 år og 3g/kg/døgn for børn over 1 år. Man skal være opmærksom på, at væskebehovet ikke nødvendigvis er dækket udelukkende ved PN hos de større børn (> 2 år).
Komplikationer ved PN
- Umiddelbare metaboliske forstyrrelser som hyper-/hypoglykæmi, elektrolytforstyrrelser og hypertriglyceridæmi.
- Refeeding syndrom; hypokaliæmi, hypomagnesæmi og hypofosfatæmi
- Kateterrelateret infektion; almindelig komplikation ved PN terapi hos børn, oftest Koagulase Negative Stafylokokker.
- Katetertrombose
- Kolestatisk icterus, PN-associeret leverpåvirkning (PNALD)
OBS: Ved abrupt ophør i PN, f.eks. i forbindelse med operation eller andre procedurer, hvor PN ikke fortsættes, skal glukose tilføres i tilstrækkelig mængde for at undgå pludselig hypoglykæmi.
Specifikke gastrointestinale sygdomme
Der henvises til følgende opdaterede retningslinjer fra bl.a. Dansk Pædiatrisk Selskab:
Leversvigt:
https://paediatri.dk/images/dokumenter/Vejl_i_hoering_2024/padiatrisk_akut_leversvigt_090124.pdf
Akut Leversvigt – Børn indlagt på RH ITA 4131:
Pankreatitis:
https://paediatri.dk/images/dokumenter/retningslinjer_2022/Akut_Pancreatitis_DPS_endelig.pdf
Referencer:
- Albert BD. Challenges and advances in nutrition for the critically ill child. Curr Opin Crit Care. 2022;28(4):401-8.
- Joosten K, Verbruggen S. PN Administration in Critically Ill Children in Different Phases of the Stress Response. Nutrients. 2022;14(9).
- Tume LN. Nutritional support for children during critical illness: European Society of Pediatric and Neonatal Intensive Care (ESPNIC) metabolism, endocrine and nutrition section position statement and clinical recommendations. Intensive Care Med. 2020;46(3):411-25.
- Mehta NM, Skillman HE, Irving SY, Coss-Bu JA, Vermilyea S, Farrington EA, et al. Guidelines for the Provision and Assessment of Nutrition Support Therapy in the Pediatric Critically Ill Patient: Society of Critical Care Medicine and American Society for Parenteral and Enteral Nutrition. Pediatr Crit Care Med. 2017;18(7):675-715
- Fivez T. Early versus Late Parenteral Nutrition in Critically Ill Children. The New England journal of medicine. 2016;374(12):1111-22
- Schofield WN. Predicting basal metabolic rate, new standards and review of previous work. Human nutrition Clinical nutrition. 1985;39 Suppl 1:5-41.
- Joosten K, Embleton N, Yan W, Senterre T, nutrition EEECwgopp. ESPGHAN/ESPEN/ESPR/CSPEN guidelines on pediatric parenteral nutrition: Energy. Clin Nutr. 2018;37(6 Pt B):2309-14.
- Mesotten D, Joosten K, van Kempen A, Verbruggen S, nutrition EEECwgopp. ESPGHAN/ESPEN/ESPR/CSPEN guidelines on pediatric parenteral nutrition: Carbohydrates. Clin Nutr. 2018;37(6 Pt B):2337-43.
- Chen L. Tight glycemic control in critically ill pediatric patients: a systematic review and meta-analysis. Crit Care. 2018;22(1).
- Agus MSD. Tight Glycemic Control in Critically Ill Children. The New England journal of medicine. 2017;376(8):729-41.
- van Goudoever JB, Carnielli V, Darmaun D, Sainz de Pipaon M, nutrition EEECwgopp. ESPGHAN/ESPEN/ESPR/CSPEN guidelines on pediatric parenteral nutrition: Amino acids. Clin Nutr. 2018;37(6 Pt B):2315-23
- Kratochvil M, Klucka J, Klabusayova E, Musilova T, Vafek V, Skrisovska T, et al. Nutrition in Pediatric Intensive Care: A Narrative Review. Children (Basel). 2022;9(7).
- Tume LN, Valla FV. A review of feeding intolerance in critically ill children. Eur J Pediatr. 2018;177(11):1675-83.
- Chicella MF, Batres LA, Heesters MS, Dice JE. Prokinetic drug therapy in children: a review of current options. Ann Pharmacother. 2005;39(4):706-11.
- Boullata JI. ASPEN Clinical Guidelines: Parenteral Nutrition Ordering, Order Review, Compounding, Labeling, and Dispensing
Kapitel 8 – Nyresvigt
| · Akut nyresvigt forekommer hos kritisk syge børn hos op til 20 – 25 %.
· Akut nyresvigt hos børn graderes i henhold KDIGO-kriterierne. · Dialyse ved kritisk sygdom varetages på højt specialiserede afsnit. |
Akut nyresvigt er en betydende komplikation hos indlagte børn med en rapporteret incidens på op til 6 % og 20-25 % blandt kritisk syge børn, dog er antallet af dialysekrævende akut nyresvigt lavere end hos voksne. Både sværhedsgraden og antal episoder med nyresvigt er stærkt associeret med mortalitet og indlæggelsestid.
Behandlingsprincipperne ved erkendt akut nyresvigt omfatter forebyggelse af yderligere skade, håndtering af livstruende komplikationer, specifik terapi af den tilgrundliggende lidelse og evt. understøttende behandling i form af dialyse. Den mest anvendte definition på akut nyresvigt er KDIGO-kriterierne, idet de er valideret til både voksne og børn.
| Stadie | Serum kreatinin | Diureser / Urin output |
| 1 | 1,5 – 1,9 x baseline værdi
eller
Stigning > 26,5 µmol/L over 48 timer |
< 0,5 ml/kg/time i 6 – 12 timer |
| 2 | 2,0 – 2,9 x baseline værdi | < 0,5 ml/kg/time i > 12 timer |
| 3 |
>3,0 x baseline værdi eller
Stigning > 354 µmol/L eller
Opstart af dialyse eller
eGFR < 35 ml/min/1,73 m2
|
< 0,3 ml/kg/time > 24 timer
eller
Anuri > 12 timer |
Tabel 22: Inddeling af nyresvigt hos børn i henhold til KDIGO kriterierne
I Danmark administreres og styres dialysebehandling af intensivpersonale når det udføres som Continuous Renal Replacement Therapy (CRRT), modsat vil peritonealdialyse og hæmodialyse oftest primært styres af de nyremedicinske afdelinger.
Pædiatrisk CRRT er en ressourcekrævende opgave med forholdsvis lille patientgrundlag i Danmark. Behandlingen kræver specielle filtre og slangesæt, som gør det muligt at behandle børn med lav kropsvægt, særligt ved børn under 10 kg.
Børn med kritisk sygdom og potentielt dialysebehov overflyttes til børneintensive afsnit på hhv. Rigshospitalet, Odense Universitetshospital, Aarhus Universitetshospital eller Aalborg Universitetshospital.
Indikationer for opstart af CRRT
Indikationerne for pædiatrisk/neonatal CRRT er de samme som hos voksne, men med hyppigere forekomst af inborn error of metabolism.
Indikationerne kan sammenfattes som følgende:
- Akut nyresvigt
- Hyperazotæmi med systemisk påvirkning (f.eks. encephalopati eller perikardieeksudat).
- Behandlingsrefraktære elektrolytforstyrrelser og/eller metabolisk acidose.
- Væskeoverskud / kritisk overhydrering.
- Akut leversvigt & ammonium producerende inborn errors of metabolisme med:
- Ammonium >150 μmol/l og hurtigt descenderende neurologisk status/coma/cerebralt ødem eller moderat til svær encephalopati pga høj ammonium.
- Vedvarende højt ammonium (>400 μmol/l) trods relevant medicinsk behandling
- Hurtigt stigende ammonium (timer) til niveauer 300 μmol/l trods relevant medicinsk behandling
- Forgiftninger med dialysable toxiner f.eks. lithium
- Systemisk tumorlyse syndrom.
- Kritisk behandlingsrefraktær hypertermi.
Valg af kateter, modalitet, antikoagulans og flowindstillinger
I Danmark anvendes flere typer CRRT-maskiner, som kan bruges til behandling af både voksne og pædiatriske patienter. Valget af en CRRT-maskine afhænger af den enkelte intensive afdeling og regionalt udbud. Det skal dog bemærkes, at ingen af de tilgængelige maskiner officielt er godkendt til de mindste børn.
Disse CRRT-maskiner varierer i deres kapabilitet og kompleksitet, men fælles for dem er, at de kan tilpasses til de særlige behov, som kræves ved pædiatrisk CRRT, herunder brug af lavt blodvolumen. Opstart af CRRT hos de mindste børn kræver priming af filteret og slangerne med blod, for at forhindre hæmodilution og hæmodynamisk ustabilitet. Det gælder hvor volumen af filter- og slangesæt tilsammen udgør over 15 – 20% af patientens blodvolumen. Valg af kateter, modalitet, antikoagulans og flowindstillinger afhænger ofte af den enkelte afdelings erfaringer og præferencer samt det udstyr og de væsker, der er til rådighed. Derfor bør man følge de lokale instrukser og retningslinjer, som er udarbejdet på den enkelte afdeling.
Referencer
Moffett BS. Trajectory of AKI in hospitalized pediatric patients-impact of duration and repeat events. Nephrol Dial Transplant. 2022;37(8):1443-50.
Kapitel 9 – Systemisk / Endokrinologisk
Væskebehandling og elektrolytforstyrrelser
| · Hvis muligt vælges som første prioritet enteral administration
· Ordiner et samlet væskebehov (ml/t eller per døgn) og inkluder al væske (i.v. medicin infusioner og bolus, transfusioner, ernæring osv.). Som sidste prioritet kan ved behov suppleres med vedligeholdelsesvæske · Lav beregning af væskebehov baseret på Holliday & Segar (4:2:1), men juster med væskerestriktion for at undgå overhydrering · Yderligere væskerestriktion (50-60%) i risikogrupper såsom ved nyre-, lever- og hjertesvigt · Monitorér daglig vægt, væskebalance, kliniske status, elektrolytter og blodsukker · Undgå hypotone væsker for at reducere risikoen for hyponatriæmi · Vælg i stedet isotone balancerede væsker såsom plasmalyte 5% (vedligehold) · Hos småbørn (< 1 år) skal man være særlig opmærksomhed på tilstrækkelig glukose tilbud og hyppigere blodsukkerkontroller · Det anbefales generelt at holde blodsukker mellem 6 – 10 mmol/l, idet stram blodsukker kontrol er forbundet med risiko for hypoglykæmi og adverse events, mens hyperglykæmi er forbundet med hyppigere infektioner og osmotisk diurese · P-Natrium korrigeres langsomt, på nær ved neurologiske symptomer · S-Kalium skal akut korrigeres hvis > 5.5 – 6 mmol/L |
Væskebehandling
Vælg af parenteral væske
Ingen væske passer til alle situationer, så valg af væske skal revurderes løbende og efter behov. Der skal sikres tre komponenter i væskeblandinger:
- Natrium – betydende for serum osmolaritet. Som udgangspunkt vælges isotone væsker såsom 0.9% NaCl, plamalyte 5%, Ringer-/laktat eller -acetat
- Vær opmærksom på at væskens reelle tonicitet efter iv indgift, ikke altid afspejles i varedeklarationen (se skema 1 nedenfor)
- Glukose – basalt behov 4-6 mg/kg/min for småbørn (< 1 år) svt 2.4 – 3.6 ml/kg/t af i.v glukose 10% uden enteral supplement. NB: Behovet stiger ofte ved kritisk sygdom
- Ved behov kan suppleres med Kalium – f.eks. 20 – 40 mmol per liter iv væske

Skema 1 Hyppigt anvendte intravenøse væsker – Kilde: Natriumfolderen – Udarbejdet af læge Christian Overgaard Steensen i samarbejde med Lægemiddelstyrelsen og Styrelsen for Patientsikkerhed. Farverne reflekterer væskernes reelle tonicitet efter indgift.
NB: forsigtighed ved mistænkt forhøjet ICP, AKI/anuri eller hyperkaliæmi af anden årsag.
Væskebehandlingsplan
Der er tre faser i væskebehandling:
- Resuscitation og deficit korrektion ved dehydrering (se særskilte instrukser)
- Vedligeholdelse
- Erstatning af abnorme tab
Vedligeholdelse
Formålet er, at erstatte fysiologiske tab (lunger, hud, sved, urin og afføring) og sikre homeostase. Væskebehovet vil variere afhængig af patientens tilstand, og kræver hyppig evaluering.
Et samlet væskebehov kan som udgangspunkt beregnes efter nedenstående forslag, baseret på Holliday & Segar (se tabel nedenfor) formlen og skal justeres i takt med patientens tilstand ændres.
Da de fleste kritisk syge børn vil have en øget ADH sekretion og ofte modtager fugtet luft via respiratoren, reduceres væskebehovet markant og væskerestriktion vil være nødvendigt.

Grøn: Anbefales kun til de stabile patienter overvejende på egne konditioner
Gul: Anbefales til flertallet af kritisk syge børn, f.eks. ved behov for respirator, vasopressor mv.
Rød: Anbefales til kritisk syge patienter med særlig risiko for overhydrering, herunder lever-, nyre- og/eller hjertesvigt samt efter hjertekirurgi, med flere.
Ovenstående væskerestriktion kan i praksis ofte være svær at opnå, men kan forsøges opnået ved koncentrering af medicin, væsker med videre, hvor det er muligt:
- Medicin (infusioner, bolus, overvej koncentrering af væsker)
- Ernæring (start enteral tidligt, hvis ingen kontraindikationer, TPN tidligst 7. døgn)
- Blodprodukter (ved behov for FFP, overveje cryopræcipitat ved væskerestriktion)
- Ved behov for højt glukose tilbud skift til højere koncentration af Glukose hhv. 20 eller 50% (NB gives i central iv adgang)
- Ofte vil væskebehovet kunne dækkes af ovenstående så ”tynde væsker” helt kan undgås.
- Ved manifest overhydrering trods ovenstående, vil diuretika ofte være indiceret
- Ved fortsat manifest overhydrering trods væskerestriktion og diuretika skal CRRT overvejes.
SIADH
Som anført skal kritisk syge børn som udgangspunkt ikke have fuld vedligeholdelses væske, da de nemt bliver overhydreret, hvilket er forbundet med dårligere outcome, forlænget respiratorbehandling og dermed indlæggelsestid. Den øgede risiko for overhydrering skyldes særligt øget ADH sekretion (SIADH) men også ”fluid creep” (medicinvand/boli, infusioner og lignende), anvendelse af hypotone væsker og ukritisk anvendelse af Holliday & Segar formel. Resultatet er nedsatte diureser, retention af frit vand, hyponatriæmi og risiko for hjerneødem samt lungestase, ødematøse luftveje og forlænget respiratorbehov.
Erstatning af abnorme tab
Alle abnorme tab (voluminøse opkastninger, diarreer, stomi-output, dræntab, blødninger mv) skal beregnes og erstattes, hvis klinisk relevant, med balancerede krystalloider såsom plasmalyte 5% eller human albumin ved større proteintab, såsom pleuraeksudat og ascites. Ligeledes skal elektrolytter korrigeres akut efter vanlige retningslinjer.
Elektrolytforstyrrelser
(se i øvrigt Natriumfolderen: https://dasaim.dk/guides/hyponatriaemivejledning)
Hyponatriæmi
Ved symptomgivende hyponatriæmi, typisk < 125 mmol/l, og neurologiske symptomer (kramper) skal p-Natrium øges akut med hyperton NaCl 3%, 1 mmol/kg bolus, som gentages indtil symptomer aftager/stopper.
NB: ved mistanke om akut øget ICP øges p-natrium uanset udgangsværdi (se særskilt instruks).
Hvis der ikke er symptomer, øges p-Natrium langsomt med 0.5 til 1 mmol/L per time, max 6 – 8 mmol/l per døgn.
Hvordan korrektionen foretages afhænger af årsagen:
Hypervolæmisk hyponatriæmi: Forsøg med furix og væskerestriktion.
Hypovolæmisk hyponatriæmi: Korrigeres med volumen (0.9% NaCl, Ringerlaktat eller enteral væske)
Normovolæmisk hyponatriæmi: Væskerestriktion, stop eller reducer evt. diuretika, giv vedligeholdelsesvæske som 0.9% NaCl eller giv natrium tilskud
Pseudohyponatriæmi: Ses ved f.eks. hyperglykæmi (DKA diabetisk ketoacidose), hyperlipidæmi mv, hvor der er øget væsketræk ind i blodbanen og dermed en ”fortynding” af p-natrium. Totalnatrium i kroppen er imidlertid normal. Dette skal ikke korrigeres.
Hypernatriæmi
Forsøg først at finde årsagen.
Skal som udgangspunkt altid korrigeres langsomt, højest 0.5 mmol/L per time eller 8-10 mmol/L per døgn. Dette for at undgå hjerneødem og neurologiske forandringer.
Normovolæmi kan behandles med sterilt vand i sonden eller isoton glukose 5% iv.
Ved overhydrering undgås loop diuretika såsom furix, og forsøges med øget saltudskillelse f.eks. med et thiazid som Hydromed 1-2 mg/kg/dosis 1 – 2 gange dgl, eller alternativt Metolazon (Zaroxolyn) 0.1 – 0.2 mg/kg evt. suppleret med kaliumbesparende diuretika såsom Spironolacton (CAVE ved hyperkaliæmi/AKI) 1 mg/kg x 1 – 2 dgl
Hypokaliæmi
Definition S-Kalium < 3.5 mmol/L.
Årsager: Alkalose, Antibiotika, diuretika, DKA, Mg mangel, nyrelidelser, adm. af glukose eller insulin, IV væske med utilstrækkeligt K-tilskud, Beta-adrenerg stimulation (stress eller medicin som ventoline, adrenalin), refeeding syndrom, hypotermi mfl.
Sjældent symptomer før s-K+< 3.0 (muskelsvaghed, svækkede senereflekser, affladet T-tak.)
Behandling:
- Foretrækkes enteral tilskud, men hvis moderat/svær hypokaliæmi gives parenteralt
- Kaliumtilskud op til 40 (60) mmol/l kan gives i PVK
- Koncentreret Kalium infusion 1 mmol/ml gives i CVK. Fortyndet Kalium 0.5 mmol/ml kan gives i et PVK, maksimalt 0.5 mmol/kg/t i separat lumen og sikres, at der ikke skylles på denne infusionsslange
Hyperkaliæmi
Definition S-Kalium > (5.5) 6 mmol/L
Årsager: Cellehenfald (Tumorlyse syndrom, forbrændinger, rhabdomyolyse, DIC), iatrogen (tilsat for meget K+), blodtransfusioner, metabolisk acidose, vævshypoksi, insulinmangel, hyperglykæmi, hyperosmolaritet, nyresvigt, binyreinsufficiens, K+-besparende diuretika mfl.
Symptomer: Muskelsvaghed, paræstesier, EKG forandringer (høje T-takker, forlænget PR, bredere QRS), arytmier (bradykardi, AV blok, VF) og hjertestop.
Diagnostik: Blodprøve, (gentages pga risiko for fejlmåling), EKG, urin-stix, evt UL nyrer
Behandling:
- Stop al parenteral og enteral kaliumtilførsel
- Calcium iv for at stabilisere hjertet (membranstabiliserende) også trods normal s-Ca++ Calcium gluconat 9mg/ml (10%) svt 0.225 mmol/ml,
dosis: 0.5 – 1 ml/kg/dosis iv over 2-5 minutter. Alternativt gives
Calcium-chlorid konc 20 mg/ml svt 0.5 mmol calcium,
Dosis 0.1 til 0.2 ml/kg. - Kan gentages hver 10 min, og skal ikke gives sammen med NaHCO3
- Natriumbikarbonat (NaHCO3) ved samtidig acidose.
Dosis 1 mmol/kg iv (langsomt) skal ikke gives sammen med calcium (udfælder) - Glukose-insulin:
Insulin infusion 1 IE/ml, dosis 0.2 IE/kg/t iv samt
Glukose 10% (100mg/ml), dosis 5 ml/kg/t, eller som 20 til 50% glukose hvis CVK adgang haves. - Beta2-agonist:
Ventoline/salbutamol inhalation (5mg/ml) dosis 0.05 ml/kg (maks 10 mg= 2 ml) blandet i 0.9% NaCl til samlet volumen på 3-4 ml
Bricanyl infusion: 0.5 mg/ml = 500 mcgr/ml. Fortyndes med 0.9%NaCl til koncentration 5 mcgr/ml. Dosis: 4 mcgr/kg IV over 20 minutter - Furix (0.1-1 mg/kg/dosis op til 5 mg/kg v nyresvigt) til øget kalium elimination
- Resonium (langsom effekt) øget elimination.
Per os eller rektalt 125 mg – 250 mg/kg hver 8 time - Dialyse (se CRRT vejledning vedr hyperkaliæmi)
Monitorering
- Kliniske tegn på væske deficit eller overhydrering, hæmodynamiske status.
- Neurologisk status pga. risiko for hyponatriæmi og hjerneødem.
- Barnet skal vejes ved indlæggelsen samt dagligt – initielt indtil stabilisering.
- Blodprøver: Elektrolytter, især kalium og natrium, syre-base status, glukose
Tabel med estimeret samlet væskebehov baseret på vægt (Holliday & Segar formel)
De fleste kritisk syge børn vil have behov for væskerestriktion (50 – 75%), angivet med henholdsvis gul og rød farve.

Referencer:
- Hornarmand, K et al: Society of critical care medicine Guidelines on Glycemic control for critically ill Children and Adults 2024 DOI: 10.1097/CCM.000000000000617
- Brossier DW, Tume LN, Briant AR, Chaparro CJ, Moullet C, Rooze S, Verbruggen CAT, Marino LV, Alsohime F, Beldjilali S, Chiusolo F, Costa L, Didier C, Ilia S, Joram NL, Kneyber MCJ, Kuhlwein E, Lopez J, Lopez.Herce J, Mayberry HF, Medmeti F, Mierzewska-Schmidt M, Rodriguez MM, Morice C, Pappachan JV, Porcheret F, Boto LR, Schlapbach LJ, Tekguc HH, Tziouvas K, Parienti JJ, Goyer I: ESPNIC clinical practice guidelines: intravenous maintenance fluid therapy in acute and critically ill children – a systematic review and meta-analysis. Intensive Care Med 2022,48:1691-1708.
- Langer T, Limuti R, Tommasino C, van Regenmortel N, Duval ELIM, Caironi P, Malbrain MLNG, Pesenti A: Intravenous fluid therapy for hospitalized and critically ill children: rationale, available drugs and possible side effects. Anaesthesiology Intensive Therapy 2018, 50(1):49-58.
- Traum AZ, Somers MJG: Parenteral fluid therapy in children. Curr Treat Options Peds 2020, 6:117-127.
- Somers MJS, Mattoo TK, Kremen J: Maintenance intravenous fluid therapy in children. uptodate.com/contents/maintenance-fluid-therapy-in-children
- Selewski DT, barhight MF, Bjornstad EC, Ricci Z, Tavares MDS, Akcan-Arikan A, Goldstein SL, Basu R, Bagshaw SM: Fluid assessment, fluid balance, and fluid overload in sick children: a report from the Pediatric Acute Disease Quality Initiative (ADQI) conference. Pediatric Nephrology 2024, 39:955-979
- Lehtiranta S, Honkila M, Kallio M, Paalanne N, Peltoniemi O, Pokka T, Renko M, Tapiainen T: Risk of elektrolyte disorders in acutely ill children receiving commercially available plasmalike isotonis fluids a randomized clinical trial. JAMA Pediatrics 2021, 175(1):28-35
- VIP instrukser Region H elektrolytforstyrrelser (vip.regionh.dk)
- Pædiatriske vejledninger (Dansk Pædiatrisk Selskab)
- Norsk Pediatrisk legeforening (helsebiblioteket.no)
Kapitel 10 – Diabetisk ketoacidose
| · Patienten vil typisk være udmattet – træt med svingende GCS, udtalt forpustet (Kussmaul respiration for udluftning af CO2 pga. metabolisk acidose), svært dehydreret med oliguri og med mulig infektiøst udløsende DKA.
· Første tiltag er væskeresuscitation (svært dehydreret). · Undgå insulin bolus – Undgå at give insulin den 1. time, undgå herefter at slukke helt for insulin til acidosen er korrigeret og undgå at give NaHCO3 · Monitoreres med GCS hver time, SpO2, EKG, 2 x PVK og a-kanyle. · CVK forsøges undgået grundet høj tromboserisiko og ofte sedationsbehov, der vil vanskeliggøre GCS vurdering. · Genopret væskebalancen gradvist over 48 timer, for at sænke osmolariteten langsomt og minimere risiko for hjerneødem · Langsom ophævelse af acidosen, samt reduktion af ketonstofdannelsen med insulin/glukose infusion · Tilbageholdenhed med intubation trods let – moderat påvirket bevidsthed – ej heller til transport. Undtagelse ved svær vedvarende påvirkning GCS < 9 eller fald > 2 point. · Ved faldende GCS og/eller tiltagende neurologiske symptomer – overvej hyperton NaCl 3%, 5 mmol/kg, afvent ikke CT eller anden udredning. · Intubation kun ved vedvarende GCS < 9 eller fald > 2 point) mhp neuroprotektion · Hvis intubation ikke kan undgås, forsøges at matche patientens egen hyperventilation initielt og herefter stiles mod pCO2 lavt i normalområdet · Risikoen for komplikationer er størst de første 12-18 timer. Rehydreringen og korrektionen af acidosen vil tage dage, og normalt blodsukker er ikke et tidligt mål. Acidosen forværres ofte kortvarigt efter opstart af behandling, herefter gradvis bedring. · Hyppig konferering med børne-diabetolog. |
Definition
- p-Glukose > 11 mmol/l
- B-ketoner > 3mmol/l samt U ketoner
- Venøs pH < 7.3 eller SBE < 15 mmol
Behandling
- Efter 1. times væskebehandling ved primær modtagelse af patienten, opstartes i sidedrop hurtigtvirkende insulin 0,1 IE/kg/time – for børn < 5 år 0.05 IE/kg/time
(Bland 50 IE NovoRapid i 50 mL isoton NaCl sv.t. 1 IE/mL) - Startdosis insulin 0.1 mL/kg/time eller hos børn < 5 år: 0.05 ml/kg/time
- Hvis korrektionen af glukose/osmolariteten går for hurtig øges glukose mængden og derrnæst reduceres insulindosis, hvis behov.
- NB: Insulin skal ikke slukkes på noget tidspunkt, men ved behov justeres
- Reducér evt. infusionshastighed isoton NaCl til 5 mL/kg/time (max 225 mL/time)
Mål: gradvis stabilisering af blodsukker >11
Ved blodsukker > 15:
- Fortsæt isoton NaCl 5 mL/kg/t (max 225 mL) og tilsæt evt. *K, se nedenfor.
- Fortsæt insulin 0.1 IE/kg/t hhv. 0.05 IE/kg/t for børn < 5 år
Ved blodsukker 10-15:
- Fortsæt isoton NaCl og tilføj glukose 5%, og K+ 40 mmol/L*. (Evt. kan væske med Natrium-/Kalium/Glucose anvendes)
- Fortsæt insulin 0.1 IE/kg/t hhv 0.05 IE/kg/t for børn < 5 år
Ved blodsukker <10 eller fald i BS > 5 mmol/time:
- Fortsæt isoton NaCl, glukose 10%, K 40 mmol/L, men øg glukose-infusion mhp stabilisering af blodsukker ~10 mmol/l. Hvis det ikke er nok reducéres insulin infusionshastigheden.
*Kalium:
Ved K < 4.0 tilsættes i stedet 60 mmol/L
ved K < 3.0 tilsættes 80 mmol/L.
Natrium:
Patienterne har ofte grad af påvirket bevidsthed, og Natrium holdes højt i normalområdet.
Da hyperglykæmi giver pseudohyponatriæmi, skal Natrium korrigeres for højt BS efter formlen: s-Na + 0,36 x (blodsukker – 5,5)
Osmolaliten tilstræbes sænket langsomt.
Idet væsentligst Natrium og glukose bidrager til osmolariteten ved DKA, kan følgende formel bruges: S-Osmolær = 2 x Natrium + P-glukose (mmol/l).
Ved større fald end 4-5 mOsmolær/time, øges p-Natrium-indholdet med pn hyperton NaCl 3%, og overvejes reduktion i insulin infusionshastighed, men husk den skal ikke slukkes.
Monitorering
- Hver time: BG og blodketoner.
- Hver 2. time: S/B-status, kalium, natrium, kreatinin, samt BT, puls og temperatur. Korrigeret natrium og osmolalitet beregnes.
- Glasgow Coma Scale monitoreres løbende, initielt hver time.
- A-kanyle oftest indiceret.
- CVK kun på indikation, idet der er øget tromboserisiko.
Cerebralt ødem
Ved svær DKA er der ofte en grad af cerebralt ødem, som forventes at aftage < 1-2 døgn. Ved hastigt fald i GCS (> 2 point) eller vedvarende GCS < 9, følges vanlig neuroprotektiv regime:
- Eleveret overkrop 30 grader
- Mål blodsukker for at udelukke hypoglykæmi
- Tilpas væskebehandling så normalt blodtryk bevares, men uden at overhydrere (reducér væskeindgift til 70 % af givne behandling. Opstart vasopressor ved behov).
- Hyperton NaCl 1 mmol/ml (3 %): 5,0 ml/kg over 10-15 minutter. Læg gerne Na højt i normal-området. Ved beregning: Husk at korrigere Na for hyperglykæmi fra formlen: s-Na + 0,4 x (blodsukker – 5)
- Efter behandling for cerebralt ødem overvejes CT scanning for at udelukke specifikke årsager til cerebrale symptomer (herunder trombose, idet risiko er øget)
- Kontakt neurokirurg mhp evt. måling af intrakranielt tryk ved behov for intubation
- Intubation (ved vedvarende GCS < 9 eller hurtigt fald > 2 point)
- Ved respiratorbehandling sigtes mod pCO2 3.5-4.5 kPa
- Væsentlige risikofaktorer er svær ketoacidose, behandling med insulin i første time samt ved for hurtig korrektion af elektrolytter og acidose med bicarbonat. Desuden ved ny diagnosticeret diabetes, alder < 5 år og lang symptomvarighed.
Acidose
Ved moderat til svær DKA er der inkomplet respiratorisk kompenseret metabolisk (keto) acidose, samt osmotisk diurese førende til dehydratio. Børn vil ofte være i stand til at kompensere acidosen langt med Kussmauls respiration og meget lav pCO2, som kan være svær at matche ved respiratorbehandling. Den svære dehydratio kan ofte føre til grad af AKI. Ved korrektion af dehydreringen bruges initielt isoton NaCl, hvilket ofte kan lede til hyperkloræmisk acidose. Imidlertid foreligger 2 RCT studier på børn, hvor balancerede væsker testes mod isoton NaCl. Begge studier finder ingen signifikant forskel i tid til korrektion af acidosen, tid til remission af AKI, ingen forskel i indlæggelsestid eller transition til subkutan insulin. Anbefalingen er således fortsat isoton NaCl som rehydreringsvæske. Acidosen skal endvidere helst undgås behandlet med bicarbonat, der resulterer i øget pCO2 og potentiel øget dilatation af cerebrale kar og tilsvarende øget ICP.
For yderligere detaljer om bl.a. elektrolytbehandling og undtagelser for regler om infusionshastighed for insulin, samt om overgang til subkutan insulin og fødeindtag, henvises til dansk pædiatrisk selskabs instruks på www.paediatri.dk eller https://paediatri.dk/endokrinolog-vaekst-vejl
Løbende kontakt med Pædiatrisk endokrinolog er vigtig.
Referencer:
- Dansk Pædiatrisk Selskab paediatri.dk
- https://paediatri.dk/endokrinolog-vaekst-vejl
- com: Diabetic Ketoacidosis in Children: Treatment and complications. https://www.uptodate.com/contents/diabetic-ketoacidosis-in-children-treatment-and-complications?search=dka%20treatment&source=search_result&selectedTitle=1%7E150&usage_type=default&display_rank=1#H17
- Yung, J et al: Controlled trial of Hartmann´s solution versus 0.9% saline for diabetic ketoacidosis. Pediatr. Child Health. 2017. https://doi.org/10.1111/jpc.13436
- Williams et al. 0.9% saline versus Plasma-Lyte as initial fluid in children with diabetic ketoacidosis (SPinK trial): a double-blind randomized controlled trial. Crit Care. 2020 https://doi.org/10.1186/s13054-019-2683-3
- Nyholm, S: Instruks vedr. Diabetes ketoacidos, Barnintensivvårdsafdelingen (BIVA), Region Uppsala, 2020. https://publikdocplus.regionuppsala.se/Home/GetDocument?containerName=e0c73411-be4b-4fee-ac09-640f9e2c5d83&reference=DocPlusSTYR-3214&docId=DocPlusSTYR-3214
Kapitel 11 – Akut binyrebark insufficiens, Addison krise, samt hydrocortison substitution
| · Livstruende akut tilstand som kræver hurtig diagnose og behandling
· Mistanken rejses ved kritisk syge patienter med kendt længerevarende steroid forbrug, og/eller uforklaret bevidsthedspåvirkning/koma, hypotension evt. kredsløbskollaps, kvalme, opkastninger, dehydrering, akut abdomen Paraklinisk ses lav Natrium og høj Kalium, lavt BS og metabolisk acidose, lav s-kortisol. · Ved mistanke om akut binyrebark- insufficiens eller -/krise gives bolus hydrocortison (Solu-Cortef®) iv eller i.m (dosis < 1 år: 25 mg, 1-6 år: 50 mg og > 6 år: 100 mg) · Ved refraktært septisk shock (shock reversal) kan overvejes i.v hydrocortison 2 mg/kg (op til 50 mg) herefter 1 mg/kg hver 8. time (se kapitel 6 om septisk shock) |
Årsager
- Den underliggende årsag til binyrebarkinsufficiens kan skyldes ødelæggelse eller dysfunktion af selve binyrebarken (primær binyrebarkinsufficiens), eller en lidelse i hypothalamus-hypofyse-binyreaksen (sekundær/tertiær binyrebarkinsufficiens)
- Binyrebarkkrise er en tilstand forårsaget af akut mangel på binyrebarkhormoner (kortisol, aldosteron). Denne mangel kan være absolut (komplet) eller relativ. Det kan udløses af fysiologisk stress (infektion, operation/anæstesi, traume eller forbrændinger) hos en patient med underliggende eller ukendt sygdom i binyrebarken eller hypofysen.
Akut binyrebarkinsufficiens eller -krise bør overvejes/mistænkes hos patienter med
- Kendt primær binyrebarkinsufficiens
- Kendt hypofyseinsufficiens (uanset hvilken påvirket akse af hypofysehormon)
- Et langt mere alvorligt og uventet klinisk billede end den udløsende sygdom ville indikere, f.eks. udtalt svag patient, uforklarlig alvorlig dehydrering eller svært kredsløbschok/kollaps
- Langvarig glukokortikoidbehandling (>2-4 uger)
- Tidligere gentagne episoder med samtidighed påfaldende langvarigt og alvorligt forløb, alvorlig dehydrering, uforklarlig hypoglykæmi
Det kliniske billede er uspecifikt, men kan minde om symptomerne ved septisk shock
- Hypotension, dehydrering, kredsløbskollaps
- Ændret bevidsthed, træthed, sløvhed, forvirring
- “Akut abdomen”, mavesmerter
- Opkastning, kvalme, nedsat appetit
- Feber (muligvis infektion), kan forsvinde ved hydrocortison behandling
Diagnostik og undersøgelse
Ved klinisk mistanke – gives akut behandling inden diagnostik foreligger.
Typiske blodprøver vil vise hypoglykæmi, hyponatriæmi, hyperkaliæmi og metabolisk acidose.
S-kortisol er typisk lav (under nedre referencegrænse), ACTH høj (over 2x øvre referencegrænse), P-renin aktivitet høj og aldosteron lav.
Bemærk: Hos en syg og stresset patient (uden binyrebarkinsufficiens) bør serum kortisol og ACTH normalt være stærkt forhøjet. Hos en kritisk syg patient med binyrebarkinsufficiens kan værdierne af serum kortisol og ACTH inden for referenceområdet derfor stadig være patologiske og indikere manglende eller suboptimalt stressrespons. Hvis der er mistanke om akut binyrebarkinsufficiens, bør diagnostik ikke forsinke behandlingen. Hvis det er muligt, tages hormonprøver (ACTH, P-Renin, Aldosteron og S-kortisol) før start.
Behandling ved mistanke om akut binyrebark insufficiens
Der gives akut intravenøs bolus injektion med hydrocortison (Solu-Cortef®):
- < 1 år: 25 mg
- 1-6 år: 50 mg
- > 6 år: 100 mg
Derefter vedligehold hydrocortison 25 mg/m2 i.v. (max 25 mg) hver 6. time.
- Hvis IV-adgang ikke er umiddelbart tilgængelig, gives hydrokortison intramuskulært
- Overvej at gentage IV/IM hydrocortison-bolusdosis, hvis der er dårlig respons på indledende glukokortikoid- og væsketerapi
- IV-behandling bør gives i 24-48 timer, eller så længe patienten har gastrointestinale symptomer, der kan påvirke absorptionen af per oral medicin
- Efter klinisk bedring halveres dosis hver dag til den sædvanlige stressdosis (ca. 30-50 mg/m2/dag) eller vedligeholdelsesdosis, som gives oralt. Hvis en stressdosis er påkrævet, kan den gradvist reduceres til vedligeholdelsesdoser inden for få dage i samråd med endokrinolog.
NB: Brug ikke methylprednisolon (Solu-Medrol®), da dette ikke har nogen mineralokortikoid virkning.
Mineralokortikoider
- Administration af mineralocorticoid (Florinef®) er ikke nødvendig i den akutte fase. Korrektion og stabilisering af elektrolytter opnås med væsketerapi og hydrocortison, som har tilstrækkelig mineralocorticoid virkning i store doser
- Ved behov startes fludrocortison (Florinef®) i vedligeholdelsesdoser i samråd med endokrinolog
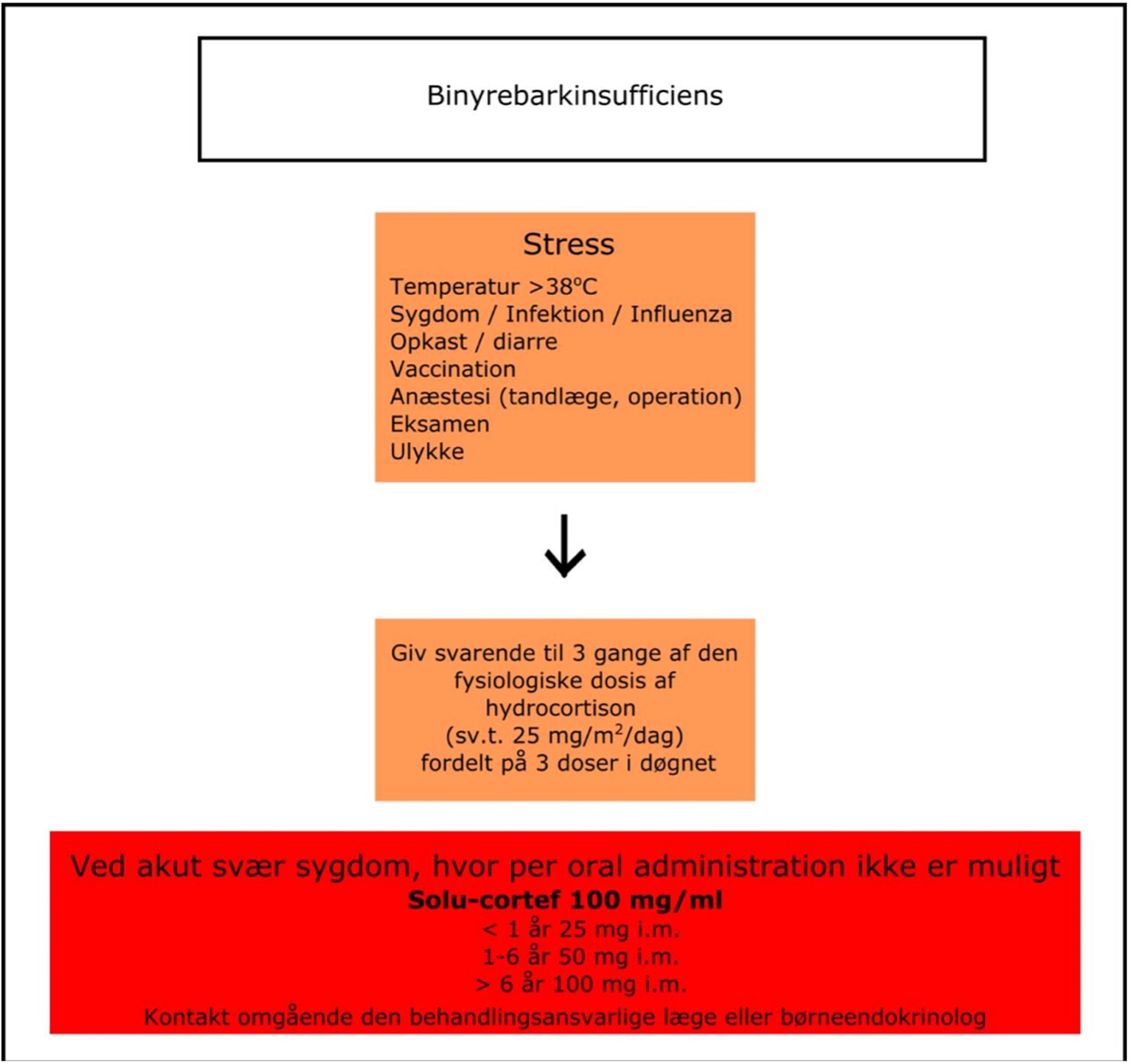
Skema 2 Dosering ved stress og kendt binyrebarkinsufficiens (56)
Ækvivalente doser for glukokortikoider
| Systemisk steroid | Dosis (mg) |
| Kortidsvirkende T½ (1.5 – 2 timer)
Hydrocortison/Solu-Cortef |
|
| 20 | |
| Intermediært virkende T½ (3 – 5 timer)
Prednisolon Prednison Methylprednisolon |
|
| 5 | |
| 5 | |
| 4 | |
| Langtidsvirkende T½ (≥ 5 timer)
Dexamethason Betamethason |
|
| 0.75 | |
| 0.60 |
Tabel 23 Ækvivalente doser for glukokortikoider
Eks: 5 mg prednisolon svt. 20 mg hydrocortison
Referencer:
- Norsk barnelegeforening https://www.helsebiblioteket.no/innhold/retningslinjer/pediatri/akuttveileder-i-pediatri/2.endokrinologi-metabolisme-og-elektrolyttforstyrrelser/2.3-binyrebarksvikt
- Dansk Pædiatrisk Selskab https://paediatri.dk/images/dokumenter/Vejl_i_hoering_2024/Iatrogen_binyrebarkinsufficiens.pdf
- promedicin.dk
Kapitel 12 – Medfødte stofskiftesygdomme
Indledning og baggrund
Behandling af inborn errors of metabolism (IEM) er mulig, og ofte succesfuld hvis den iværksættes tidligt. Ved sen behandling øges risikoen for neurologisk skade og død. Det betyder, at akut iværksættelse af behandling bør ske på klinisk mistanke om IEM (fx høj ammonium, metabolisk acidose, hypoglykæmi, påvirket bevidsthed) og barnet bør straks konfereres med Center for Sjældne Sygdomme, Rigshospitalet. Bagvagt, Afdeling for Børn og Unge, RH: 35451350.
Tiltag inden overflytning
- Akutbehandling startes (se nedenfor)
- Sikring af relevante parakliniske prøver (efter konf. Center for medfødte stofskiftesygdomme)
- +/- Sonde
- +/- KAD
- 2 iv. adgange
- Neuroprotektion overvejes ved tegn på CNS-påvirkning
- Intubation ved tegn på manglende evne til at forsvare luftveje eller hypoventilation (pga. toxiske metabolitter) eller andre tegn på cerebralt ødem
- Antibiotika startes på vid indikation, da udløsende årsag til IEM kan være infektion
Børn kendt med metabolisk sygdom vil have en behandlingsvejledning ved akut sygdom, som familien oftest vil præsentere ved indlæggelse, og som alternativt burde kunne forefindes i journalen.
Nedenfor gengives i punktform de vigtigste behandlingsregimer til akut behandling af barnet med ukendt metabolisk sygdom. For en mere udførlig guide henvises til Center for Medfødte stofskiftesygdommes hjemmeside.
Behandling
- Minimere yderligere akkumulering af toksiske metabolitter (fx ved at begrænse tilførsel af det fødemiddel, som barnet ikke kan omsætte)
- Korrigere den altid samtidige energimangel (samt forhindre katabolisme) ved at tilføre glukose
- Korrigere dehydrering
- Korrigere elektrolyt- og syre/base-forstyrrelser
Symptomer
Koma, dehydrering, acidose, hyperammoniæmi, elektrolytforstyrrelser, cerebralt ødem, respiratorisk insufficiens og sepsis er hyppige tilstande ved IEM, hvorfor indlæggelse på intensiv afdeling kan være nødvendig.
Evaluer barnet klinisk: Tjek for encefalopati/koma, irritabilitet, kramper, klonus, tonusændringer (perifer hypertoni, tonisk elevering af arme, trunkal hypotoni), takypnø/dyb respiration, dehydrering, tegn på sepsis.
Akutte blodprøver
- Syre-base status med anion-gap, elektrolytter (Na+, K+, Ca++), glukose og laktat
- Ammonium (skal på køl)
- Nyretal med karbamid, kreatinin
- Levertal
- Koagulationstal
- Kreatinkinase, urat, triglycerider
- Bloddyrkning, CRP, (evt. PCT), leukocytter + diff
- Plasma aminosyrer og plasma acylkarnitiner
- Urin mhp stix for ketonstoffer og urin metabolisk screening
Overvej evt. tidligt indikation for exomsekventering (Akut Sygt Barn Panel, som dækker > 2000 gener for IEM, epileptiske encefalopatier og leversygdomme efter konf med CIMD.)
Praktisk omkring barnet
- Stop barnets sædvanlige ernæring, herunder amning
- Start hurtigst muligt følgende væske:
- Giv en-gangsbolus glukose 200 mg/kg (2ml/kg af glukose 10%) over 10 minutter
- Giv en-gangsbolus isoton NaCl 10 ml/kg (kan gentages jf. normal chokterapi) over 10 minutter
- Giv glukose 10% i de mængder, der er angivet i tabel 23.
Kan der ikke anlægges IV adgang, kan glukose i stedet gives via nasal-sonde; her kan bruges IV opløsninger eller perorale opløsninger af glukose polymer (fx Maxijul eller Fantomalt). En fordel ved enteral indgift er, at højere koncentrationer kan gives. Tilstræb samlet kalorietilførsel på minimum 100 kcal/kg/døgn givet som glukose 10% med tillæg af intralipid og PO glukose.
| Alder
(år) |
Vægt
(kg) |
Glukose mængde | Kcal | IV infusion
10% glukose |
Nasogastrisk sonde infusion (hastighed, koncentration) | Bikarbonat
(mmol givet over første 3 timer |
| 0-1 | 10 mg/kg/min | 58 kcal/kg/dag | 150 ml/kg/dag | 150 ml/kg/dag, 10% | 1/3 x (vægt x Base deficit) | |
| 1-2 | 10 mg/kg/min | 58 kcal/kg/dag | 150 ml/kg/dag | 100 ml/kg/dag, 15% | 1/3 x (vægt x Base deficit) | |
| 2-6 | 8 mg/kg/min | 46 kcal/kg/dag | 120 ml/kg/dag | 60 ml/kg/dag, 20% | 1/4 x (vægt x Base deficit) | |
| >6 | <30 | 6 mg/kg/min | 35 kcal/kg/dag | 90 ml/kg/dag | 45 ml/kg/dag, 20% | 1/5 x (vægt x Base deficit) |
| >6 | 30-50 | 4.5 mg/kg/min | 26 kcal/kg/dag | 67 ml/kg/dag | 33 ml/kg/dag, 20% | 1/8 x (vægt x Base deficit) |
| >6 | >50 | 3 mg/kg/min | 17 kcal/kg/dag | 45 ml/kg/dag | 22 ml/kg/dag, 20% | 1/10 x(vægt x Base deficit) |
Tabel 24 Glukose og bikarbonat behandling
Ved manglende effekt, persisterende hypoglykæmi eller mistanke om cerebralt ødem:
Anlæg central veneadgang og giv samme volumina af mere koncentrerede glukoseopløsninger (fx 20 eller 50%).
Hold diurese >4 ml/kg/time; hvis mindre giv i.v. furosemid 0,5-1 mg/kg/dosis.
Hæmodialyse bør overvejes tidligt ved mistanke om Maplesirup Urine disease, urinstofcyklusdefekt og evt. organisk acidæmi (peritonealdialyse er ikke sufficient).
Ved acidose (pH<7.2 hos børn < 3 år; pH<7 hos børn >3 år) samt ved lav standardbikarbonat (<10 mEq/L) gives bikarbonat som angivet i tabel 1; efter 3 timer tages ny syre/base status; ved fortsat acidose gives yderligere bikarbonat.
Hyperammoniæmi
Ammonium bør altid måles ved encefalopati og mistanke om IEM. Der er lineær sammenhæng mellem peak-niveau / varigheden af hyperammoniæmi og den cerebrale prognose.
Ved hyperammoniæmi
- Sikres urin til metabolisk screening, plasma til aminosyrebestemmelse og acylkarnitiner, samt DNA til mutationsanalyse/exomsekventering. OBS ikke nødvendigt med sterilprøve og kan sikres med fx pose.
- Opstartes øjeblikkeligt medicinsk terapi ved ammonium mellem 200 og 400 µmol/l (IV natriumbenzoat, natriumphenylbutyrat og arginin først som bolus over 90 minutter og dernæst som kontinuerlig infusion)
- Opstartes øjeblikkeligt hæmodialyse ved ammonium på >400 µmol/l; peritonal dialyse er insufficient
- Såfremt P-ammonium ikke falder til 75% af udgangsværdi over første 8 timer på ovenstående behandling, indledes dialyse
Monitorering af behandling for IEM er primært klinisk; tjek glukose, elektrolytter, ammonium og syre-base status med intervaller efter situationen. Registrer neurologisk status og vær specielt opmærksom på tegn på forhøjet intrakranielt tryk.
Ved intraktable kramper (børn < 2 år) med normal rutine biokemi: giv 1) Pyridoxin og/eller 2) pyridoxal-5-phosphat
Reference:
Kapitel 13 – Koagulation
Hæmostase hos børn afviger fra voksne ved at trombocytter hos præmature og neonatale er hyporesponsive. Fibrinogen niveauet er højere, men funktionen er nedsat og børn har nedsat trombin dannelse og fibrinolyse. Der sker en gradvis stigning i niveauer indtil voksenniveau nås ved ca. 6. måneders alderen. Raske nyfødte og babyer bløder generelt ikke spontant.
Tromboseprofylakse
Venøs trombose hos børn er en sjælden hændelse, og modsat voksne har venøse tromber hos børn oftest en udløsende årsag. Der er lavet få studier med børn og tromboseprofylakse og behandling af tromboser. Det meste er ekstrapoleret fra studier om voksne, men børn får tromber af helt andre årsager. CVK er den hyppigste årsag til venøse trombose hos børn, og ca. 20 % af børn med CVK udvikler trombose
Hos børn der er indlagt på en almen intensiv afdeling, er LMWH at foretrække over UFH, da det administreres subkutant, har færre interaktioner, og har et mere forudsigelige dosis-respons forhold.
- Det anbefales af opstarte tromboseprofylakse ved indlæggelse på ITA, anlagt CVK og én anden risikofaktor
- Det anbefales at opstarte tromboseprofylakse ved enten indlæggelse på ITA eller anlagt CVK og to andre risikofaktorer
- Det anbefales at opstarte tromboseprofylakse hos børn med tre eller flere risikofaktorer
Risikofaktorer:
Forventet indlæggelse over 72 timer
Cancer (aktiv – ikke i remission)
Østrogen terapi startet inden for 1 mdr.
Inflammatorisk sygdom (ny-diagnosticeret, dårligt kontrolleret eller opblussen)
Mekanisk ventilation
Immobilisering
Overvægt (over 99 percentilen for alder)
Post pubertet
Svær dehydrering der kræver intervention
Kirurgi over 90 min inden for 14 dage
Systemisk eller svær lokal infektion (positive dyrkninger)
Traume som indlæggelses diagnose
| Lav-molekylære hepariner (LMWH) | Profylakse dosis |
| Enoaxparin
OBS: Nedsat dosis ved nedsat nyrefunktion > 2 mdr.
|
1 mg/kg en gang dagligt eller 0,5 mg/kg to gange dagligt s.c. |
| Tinzaparin
> 2 mdr. |
50 ie/kg en gang dagligt s.c. |
| Dalteparin
> 2 mdr. |
100 ie/kg en gang dagligt s.c. |
Ved mistanke om ophobning, f.eks. ved svært nyresvigt, kan måles anti-Xa dalværdi for at afklare om der er manglende clearance.
Ved behandlingssvigt eller svær overvægt kan overvejes at måle anti-Xa efter 3. dosis (4 timer efter administration, peak-værdi). Der foreligger ikke studier, der kobler dosisjustering titreret via anti-Xa til outcome. Anti-Xa målværdier og dalværdier er assayafhængige og varierer derfor mellem laboratorier. Det bør afklares lokalt med støtte fra den lokale koagulationsvagt, hvis der ønskes dosisjustering vha. måling af anti-Xa.
Behandling af venøs trombose
| Lav molekylært heparin (LMWH) | Terapeutiske doser |
| Enoaxparin1
> 2 mdr
|
1 mg/kg to gange dagligt s.c. |
| Tinzaparin2
2 – 12 mdr 1 – 5 år 5 – 10 år 10 – 16 år |
250 ie/kg en gang dagligt 240 ie/kg en gang dagligt 200 ie/kg en gang dagligt 175 ie/kg en gang dagligt |
| Dalteparin2
> 2 mdr |
100 ie/kg to gange dagligt eller 200 ie/kg én gang dagligt Max 18.000 IE/døgn |
1 Enoxaparin er relativt kontraindiceret ved nyreinsufficiens.
2 Evt. dosis reduktion ved tinzaparin og dalteparin ved nyreinsuffciens
| Ufraktioneret heparin (UFH) | ||
| Alder | Bolus efterfulgt af infusion | Monitorering |
| < 12 mdr
1 – 12 år
> 12 år |
Bolus 75 ie/kg efterfulgt af infusion 28 ie/kg/time
Bolus 75 ie/kg efterfulgt af infusion 20 ie/kg/time
Bolus 80 ie/kg efterfulgt af infusion 18 ie/kg/time |
APTT 1,5-2,5 gange kontrol |
| Bemærk at heparin har stor inter- og intra-individuel effekt, bl.a. efter sygdoms- og hydreringsgrad. Ved svær kritisk sygdom/multiorgansvigt bør udvises forsigtighed med bolus og start-infusionshastighed evt. reduceres. | ||
Justering af UFH gøres efter lokal instruks da APPT referenceinterval afhænger af assay og derfor varierer mellem laboratorier.
Trombolyse
Der er ingen konsensus om trombolyse behandling af tromber hos børn. Det anbefales, at man overvejer at trombolysere ved truede ekstremiteter, svær organ påvirkning eller i livstruende situationer. Det er sjældent ved venøs trombose, men inkluderer tilstande som bilateral nyrevene trombose, vena cava superior syndrom, cerebral sinustrombose med svær neurologisk påvirkning, ekstremitets DVT med truende iskæmi, intrakardiel trombe med kardiovaskulær instabilitet og massiv lungeemboli.
Der er en øget risiko for blødning ved brug af trombolyse, især hos neonatale og det anbefales at udføre ultralyd af cerebrum før og efter trombolyse. Alteplase (rtPA) er at foretrække over urokinase. Trombolyse hos børn er meget sjældent, og bør ikke udføres uden vejledning fra højt specialiseret afdeling.
Monitorering med hæmatologiske parametre anbefales, særligt fibrinogen, da fibrinogenomsætningen øges markant ved trombolyse. Ved blødning overvejes primært substitution af fibrinogen samt reversering med tranexamsyre.
Antitrombotisk behandling og neuroaxial blokade
Der henvises til ”Peroperativ regulering af antitrombotisk behandling” udarbejdet af Dansk Selskab for Trombose og Hæmostase, da anbefalingerne for børn er de sammen som for voksne. https://www.dsth.dk/retningslinjer-og-rapporter/
Komplikationer
Den primære komplikation ved behandling med antitrombotiske midler er blødning. Risikoen er lille ved behandling af børn, men kan ikke elimineres. En anden komplikation ved behandling med UFH og LMWH er heparin induceret trombocytopeni (HIT), der er sjældnere ved behandling med LMWH end UFH.
Komplikationerne ved venøs trombose er bl.a. post-trombotisk syndrom, der ses hos op til 33-50 % af venøse tromboser hos børn, og kan føre til livslang morbiditet.
Baggrund
Venøs trombose hos børn er en sjælden hændelse, og modsat voksne har venøse tromber hos børn oftest en udløsende årsag. CVK er den hyppigste årsag til venøse tromber hos børn, og ca. 20 % af børn med CVK udvikler tromber. Et lille studie har vist, at tromboseprofylakse med enoxaparin kan forebygge CVK relaterede tromber, men en større metanalyse har ikke kunnet vise det samme. Incidensen af venøs trombose hos børn er bimodal med højeste incidens under 1 år og over 13 år.
Der er lavet få studier med børn og tromboseprofylakse og behandling af tromboser. Det meste er ekstrapoleret fra studier om voksne, men børn får tromber af helt andre årsager.
Hos børn der er indlagt på en almen intensiv afdeling er LMWH at foretrække over UFH, da det administreres subkutant, har færre interaktioner, og det er lettere at opnå terapeutiske niveauer. Infusion med UFH gives til udvalgte patienter, hvor der er høj risiko for blødning og/eller nyresvigt pga. kortere T½, reversabilitet (protaminsulfat) og ikke renal clearance. Hvis man vil undgå injektion to gange dagligt subkutant, er der udviklet et subkutant kateter, der virker i op til en uge.
Transfusion
Erytrocyt transfusion
Beslutning om transfusion skal ikke kun være baseret på hæmoglobin (hgb) værdi, men på en samlet vurdering af klinisk tilstand, symptomer og biokemiske markører. Risiko for komplikationer, fordele og ulemper skal grundigt overvejes. Der bør også bruges andre muligheder for at øge tolerancen til anæmi og forbedre ilt balancen:
- Sedation
- Respirator behandling ved respiratorisk svigt
- Temperaturkontrol
- Optimering af blodtryk med inotropi eller vasopressor
- Behandling af arytmier.
Der skal altid måles hgb koncentration inden transfusion, og hgb skal også kontrolleres efter transfusion. Man kan kontrollere hgb 5-10 min efter afsluttet transfusion. Ligeledes kontrolleres kalium, calcium og syre-base status og korrigeres efter gældende retningslinjer. Det anbefales at transfundere 10 ml/kg.
Der anbefales at bruge bestrålet blod, hvis det er risiko for transfusion-associated graft versus host disease (ta-GVHD).
| Definitioner: | |
| Total blod volumen | Grad af blødning |
| · 1 mdr – 1 år: 80 ml/kg
· 1-8 år: 75 ml/kg · >8 år: 70 ml/kg |
· Minimal blødning <1 ml/kg/t
· Moderat blødning 1-5 ml/kg/t · Svær blødning >5 ml/kg/t · Massiv blødning – total blod volumen på 24 timer eller 50% af total blod volumen på 3 timer. |
Ved den blødende patient bestemmes total blod volumen og grad af blødning for at vælge transfusions strategi.
Ved den hæmodynamisk ustabile patient med aktiv blødning, gives balanceret transfusion i forholdet 2:2:1 med bolus på 10 ml/kg
(Kan beregnes vha.: 4 ml erytrocytter : 4 ml frisk frosset plasma : 2 ml trombocytter / kg).
Transfusionsgrænser:
Hæmodynamisk stabile
- Hgb <3,1 mmol/l: Skal altid transfunderes og der tilstræbes Hgb på 4,3 – 6 mmol/l efter transfusion.
- Hgb 3,1 – 4,3 mmol/l: Transfusion gives efter klinisk vurdering.
- Hgb ≥ 4,3 mmol/l: Transfusion anbefales ikke.
- Hgb ≥ 4,3 mmol/l umiddelbart postoperativt (ex. hjerteoperationer): Transfusion anbefales ikke, medmindre der er pågående blødning.
- Hgb ≥ 5,6 mmol/l: Ved svær TBI
Hæmodynamisk ustabile
- Hgb <4,3 mmol/l: Transfunderes ofte, men efter klinisk vurdering
- Hgb 4,3-6 mmol/l: Transfusion ofte indiceret ved et vedvarende ustabilt barn fx svær ARDS, refraktært septisk shock, hæmoragisk shock, akut hjerneskade eller hjertesyge børn.
Onkologiske og hæmatologiske børn transfunderes efter individuel indikation og i samarbejde med speciallæge i pædiatri.
Se flow chart sidst i kapitlet.
Dissemineret Intravaskulær Koagulation (DIC)
Definition og Patofysiologi
DIC er altid en sekundær tilstand, karakteriseret ved en universel aktivering af det hæmostatiske system, hvor symptomerne, trombose og blødning, vil afhænge af sygdomsgrad og underliggende sygdom.
Der er ikke udviklet validerede scoringsværktøjer til at stille diagnosen eller vurdere graden af DIC hos børn. Hyppigst anvendes ISTH’s DIC score (tabel 24), men i flere studier findes diskrepans mellem DIC score, klinisk tilstand og obduktionsfund. DIC scores kan primært anvendes til at vurdere udviklingen over tid.
| Scoringssystem til beregning af DIC score. Anvendes kun ved tilstande associeret med DIC.
≥5 foreneligt med ”åbenlys” DIC – gentage score dagligt <5 foreneligt med ”ikke-åbenlys” DIC – gentag score inden for 1-2 dage |
||||
| 0 | 1 | 2 | 3 | |
| Trombocyttal (x109/L) | >100 | 50-100 | <50 | |
| D-dimer* (mg/L) FEU | <0,8 | 0,8-8 | >8 | |
| INR | <1,3 | 1,3-1,5 | >1,5 | |
| Fibrinogen (µmol/L) | ≥2,9 | <2,9 | ||
| Modificeret til danske forhold ud fra Taylor Jr. et al. Termerne ”overt” og ”non-overt” er oversat til ”åbenlys” og ”ikke-åbenlys”.
*D-dimer målinger afhænger af det anvendte assay, og de anvendte intervaller svarer til ingen forhøjelse / let forhøjelse (x1-x10 af øvre referenceværdi) / svær forhøjelse af D-dimer (>x10 af øvre referenceværdi). Dertil anbefales at anvende aldersopdelte referenceintervaller for forhøjet D-dimer |
||||
Tabel 25 Scoringssystem til beregning af DIC score. Anvendes kun ved tilstande associeret med DIC
Underliggende sygdom
Årsagerne til DIC hos børn adskiller sig en anelse fra årsagerne hos voksne. Fortsat hyppigst er sepsis, dernæst traumer og nyopstået hæmatologisk cancer. Ved sepsis ses primært trombotiske manifestationer. Senere optræder blødning som følge af trombocytopeni og forbrugskoagulopati. Ved de hæmatologiske cancere ses blødning som det primære og hyppigste symptom.
Behandling – overordnet
Behandlingen af DIC hos børn er dårligt undersøgt, og støtter sig primært op ad studier foretaget på voksne, og følger samme principper.
Basale principper for behandling af DIC
- Aggressiv behandling af underliggende sygdom
- Understøttende transfusion med blodprodukter baseret på symptomer: trombose og blødning
- Hæmning af excessiv trombin dannelse – anvend evt. trombose profylakse med lavmolekylært heparin
- Regelmæssig monitorering – klinisk og paraklinisk
- Husk at abnorme blodprøver kan have andre årsager end DIC
- Kontakt højt specialiseret enhed og/eller koagulationsvagt
Behandling – Trombose
Antikoagulation
Lavmolekylært heparin og ufraktioneret heparin er den oftest anvendte understøttende antikoagulerende behandling ved DIC. Anbefalingen om anvendelse af tromboseprofylakse er ekstrapoleret fra voksenpopulationer, hvor tromboseprofylakse anbefales hos den ikke-blødende DIC patient.
Ved tegn på trombose overvejes terapeutisk dosering af heparin, enten ufraktioneret eller lavmolekylært. Anvendelsen hviler på spinkel evidens, er forbundet med blødningsrisiko, og de foreliggende studier er gamle. I de tidligere studier har ufraktioneret heparin være anvendt, og har den fordel at halveringstiden er kort, og der er mulighed for reversering med protaminsulfat. Monitoreringen er dog usikker, da APTT påvirkes af mange faktorer i tilfælde af DIC, og man risikerer både under- og overdosering.
Lavmolekylært heparin i terapeutisk dosering ved DIC hos børn er ikke undersøgt.
Antitrombin
Særligt ved septisk DIC ses et lavt niveau af antitrombin pga. både øget forbrug såvel som nedsat produktion. Hos børn ≥1 år er antitrombin <0,67% associeret med død og organsvigt. Der foreligger ikke randomiserede studier med anvendelse af antitrombin hos børn, og behandlingen hos voksne hviler på spinkel evidens. Dog foreligger flere retrospektive studier på børn der indikerer, at antitrombin kan gives sikkert i en tidlig fase af septisk DIC. Beslutningsstøtte kan evt. indhentes hos den lokale koagulationsvagt.
Dosis: (ønsket værdi – målt værdi) x vægt x 100 = dosis i IE
Behandling – Blødning
Frisk frosset plasma
Gives ved blødning og samtidig forlænget APTT og/eller INR, ca. x1,5 over øvre referenceværdi. Dosis er 10-20 ml/kg, givet over 30 min og under hæmodynamisk monitorering for at undgå overhydrering.
Protrombin komplex koncentrat (PCC)
Indeholder vitamin-K afhængige koagulationsfaktorer (II, VII, IX og X). Kan overvejes ved alvorlig blødning samtidig med svær overhydrering. Dog haves opmærksomhed på, at PCC er protrombotisk, særligt ved gentagen dosering. PCC er kontraindiceret ved heparin induceret trombocytopeni, da det indeholder heparin i lille mængde.
Fibrinogen
Hos den blødende patient stiles mod fibrinogen >4,4 µmol/L (svt. 1,5 g/L). Profylaktisk administration anbefales generel ikke, da transfusionsgrænsen hviler på spinkel evidens. Hos den ikke-blødende patient kan ovevejes fibrinogen koncentrat eller cryopræcipitat, hvis fibrinogen koncentrat ikke haves, ved fibrinogen < 3,0 µmol/L (svt. 1 g/L).
Dosis: (ønsket værdi i µmol/L – målt værdi i µmol/L) x vægt x 20 = dosis i mg
Trombocytter
Ved blødning eller behov for invasiv procedure med høj blødningsrisiko, anbefales at trombocyttallet ligger ≥50 x109/L. Der foreligger ikke en nedre grænse for trombocyttransfusion hos ikke-blødende patienter. Dog anbefales ved børn i kemoterapi, der udvikler DIC en transfusionsgrænse på 10 x109/L.
Blødningstendens kan skyldes nedsat trombocytfunktion, mere end nedsat trombocyttal, hvorfor trombocyttransfusion kan være indiceret ved trombocyttal ≥50 x109/L. Dosis er 10-15 ml/kg.
Tranexamsyre
Tranexamsyre er relativt kontraindiceret ved de fleste tilfælde af DIC, særligt septisk DIC, da fibrinolysen her allerede er hæmmet. Dog kan DIC udløst af hæmatologisk malignitet være karakteriseret ved hyperfibrinolyse. Tranexamsyre gives da kun efter aftale med højtspecialiseret enhed med kendskab til hæmatologisk malignitet.

Referencer:
- Newall F, Branchford B, Male C. Anticoagulant prophylaxis and therapy in children: current challenges and emerging issues. J Thromb Haemost [Internet]. 2018 Feb 1 [cited 2024 May 15];16(2):196–208.
- Sochet AA, Jaffray J, Branchford BR, Havlicek EE, Mosha M, Amankwah EK, et al. Hospital-Acquired Venous Thromboembolism and Invasive Mechanical Ventilation: A Report From the Children’s Hospital Acquired Thrombosis Consortium. Pediatr Crit Care Med [Internet]. 2024 Feb 1 [cited 2024 May 6];25(2):E82–90.
- Monagle P, Newall F. Management of thrombosis in children and neonates: practical use of anticoagulants in children. Hematol Am Soc Hematol Educ Progr [Internet]. 2018 Nov 30 [cited 2024 May 16];2018(1):399–404.
- Faustino EVS, Shabanova V, Raffini LJ, Kandil SB, Li S, Pinto MG, et al. Efficacy of Early Prophylaxis Against Catheter-Associated Thrombosis in Critically Ill Children: A Bayesian Phase 2b Randomized Clinical Trial. Crit Care Med [Internet]. 2021 Mar 1 [cited 2024 May 6];49(3):E235–46.
- Jinks S, Arana A. Venous thromboembolism in paediatrics. BJA Educ [Internet]. 2019 Sep 1 [cited 2024 May 6];19(9):305–12.
- Witmer C, Raffini L. Treatment of venous thromboembolism in pediatric patients. Blood [Internet]. 2020 Jan 30 [cited 2024 May 6];135(5):335–43.
- Long E, Pitfield AF, Kissoon N. Anticoagulation therapy: indications, monitoring, and complications. Pediatr Emerg Care [Internet]. 2011 Jan [cited 2024 May 6];27(1):55–61.
- Vidal E, Sharathkumar A, Glover J, Faustino EVS. Central venous catheter-related thrombosis and thromboprophylaxis in children: a systematic review and meta-analysis. J Thromb Haemost 2014 [cited 2024 May 15];12(7):1096–109.
- Doctor a, Chollete JM, Remy KE, Argent A, Carson JL, Valentine SL, Bateman ST, Lacroix J: Recommendations on RBC transfusion in general critically ill children based on hemoglobin and/or physiologic thresholds from the pediatric critical care transfusion and anemia expertise initiative. Pediatric critical care medicine 2018, 19(9): S98-113.
- Demaret P, Emeriaud G, Hassan NE, Kneyber MCJ, Valentine SL, Bateman ST, Tucci M: Recommendations on RBC transfusions in critically ill children with acute respiratory failure from the pediatric critical care transfusion and anemia expertise initiative. Pediatric critical care medicine 2018, 19(9): S114-120.
- Muszynski JA, Guzzetta NA, Hall MW, Macrae D, Valentine SL, Bateman ST, Spinella PC: Recommendations on RBC transfusions for critically ill children with nonhemorragic shock from the pediatric critical care transfusion and anemia expertise initiative. Pediatric critical care medicine 2018, 19(9): S121-126.
- Tasker RC, Turgeon AF, Spinella PC: Recommendations on RBC transfusions in critically ill children with acure brain injury from the pediatric critical care transfusion and anemia expertise initiative. Pediatric critical care medicine 2018, 19(9): S133-135.
- Karam O, Russell RT, Stricker P, Vogel AM, Bateman ST, Valentine SL, Spinella PC: Recommendations on RBC transfusions in critically ill children with nonlife-threatening bleeding or hemorrhagic shock from the pediatric critical care transfusion and anemia expertise initiative. Pediatric critical care medicine 2018, 19(9): S127-132.
- Cholette JM, Willems A, Valentine SL, Bateman ST, Schwartz SM: Recommendations on RBC transfusions in infants and children children with aquired and congenital heart disease from the pediatric critical care transfusion and anemia expertise initiative. Pediatric critical care medicine 2018, 19(9): S137-148.
- Steffen KM, Tucci M, Doctor A, Reeder R, Caro JJ, Muszynski JA, Spinella PC: The impact of restrictive transfusion practices on hemodynamically stable critically ill children without heart disease: a secondary analysis of the age of of blood in children in the PICU trial. Pediatric critical care medicine 2023, 24(2): 84-92.
- Kunwar S, Alam M, Ezekwueme F, Yasir M, Lawrence JA, Shah S, Gordon DK: Diagnostic Scores and Treatment Options for Acute Disseminated Intravascular Coagulation in Children. Cureus 2021, 13(9):e17682.
- Rajagopal R, Thachil J, Monagle P: Disseminated intravascular coagulation in paediatrics. Arch Dis Child 2017, 102(2):187-193.
- Kongstad C, Mikkelsen TS, Hvas AM: Disseminated intravascular coagulation in children with cancer: A systematic review. Pediatr Hematol Oncol 2020, 37(5):390-411.
- Niederwanger C, Hell T, Hofer S, Salvador C, Michel M, Schenk B, Treml B, Bachler M: Antithrombin deficiency is associated with mortality and impaired organ function in septic pediatric patients: a retrospective study. PeerJ 2018, 6:e5538.
- Levi M, Toh CH, Thachil J, Watson HG: Guidelines for the diagnosis and management of disseminated intravascular coagulation. British Committee for Standards in Haematology. Br J Haematol 2009, 145(1):24-33.
Kapitel 14 – Interhospital transport
Interhospital transport omfatter tre hovedaktører: Den henvisende afdeling, det modtagende børnecenter og den transporterende enhed.
Interhospital transport som proces begynder, så snart overvejelsen om at flytte barnet melder sig, og afsluttes først, når behandlingsansvaret er overgivet til modtagende afdeling.
Koordinering og beslutningstagning mellem de tre involverede parter er en udfordring. Det afhjælpes ved klare regionale aftaler og træning som en del af regional forberedelse på opgaven omkring det uventet kritisk syge barn.
Henvisende afdeling
Behandling af det akut dårlige barn er fagligt og mentalt udfordrende, og vil typisk foregå i et samarbejde mellem anæstesien og pædiater eller akutmediciner. Få af anæstesilægens arbejdsopgaver stiller samme krav til klinisk kunnen, kommunikation, logistisk forståelse og lederskab, som overflytning af det kritisk syge barn.
Ledelse
Stabilisering er ressourcekrævende, og tilkald af ekstra personale er ofte nødvendigt.
Ledelse og struktur er afgørende. Der bør tidligt i processen identificeres en teamleder, som fordeler opgaver til medlemmer i teamet. Mange opgaver kan løses uafhængigt og parallelt med hinanden, herunder kliniske tiltag, visitationsproces, praktisk klargøring til den efterfølgende transport og løbende orientering af familie.
Klinik
Den kliniske tilgang bør følge ABCDE-modellen.
Ideelt set, vil en senior læge og 1-2 sygeplejersker være allokeret udelukkende til barnets behandling og diagnostik, mens andet personale klargør udstyr og medicin herunder infusionsblandinger. Hvis overskuddet er til stede, forberedes medfølgende dokumentation, og infusioner trækkes op til transportfasen. Se faktaboks 1.
Faktaboks 1 Udvalgt praktisk klargøring til transport på henvisende afsnit
Klargøring af infusioner i 50ml sprøjter
- 10% glukose og krystalloider
- sedativa (propofol / midazolam / morfin / fentanyl). Kan i stedet gives i refrakte doser hos de mindste børn
- inotropi/vasopressorer
Bolusvæske
- krystalloid
- blodprodukter
Dokumentation
- tjek, at radiologisk billedmateriale kan overføres digitalt, specielt hvis overflytning til anden region
- tjek at opdateret journal kan læses umiddelbart af modtagende enhed, herunder medicin og prøvesvar
- udvalgte print kan være nødvendigt
Visitationsproces
Tidlig kontakt til børnecenter med henblik på visitation og behandlingsråd anbefales. Visitation bør generelt begynde i egen region, men specifikke tilstande kan fordre kontakt til center med landsdel- eller landsfunktion, herunder abdominal katastrofe, brandsår, mistanke om kongenit hjertesygdom eller forventet behov for ECMO. Visitation består ofte af flere telefonsamtaler og bør varetages af erfaren læge med evne til at udtrykke sig præcist og kortfattet. Modtagende børnecenter får overblik, og beslutter herudfra, om visitation er korrekt, og om patienten kan modtages.
Det besluttes, hvordan transporten skal gennemføres. Det skal være entydigt, hvem der kontakter transportteamet, og hvem der aktiverer AMK. Derudover vil modtagende børnecenter kunne rådgive det lokale team, om yderligere behandlingstiltag i ventetid på ankomst af transportenhed.
Transporterende enhed
Transporten kan udføres af hentehold fra børnecentrets neonatale eller børneanæstesiologiske funktion, en præhospital enhed (akutlægebil eller HEMS) eller af det lokale henvisende team. Præhospitale enheder vil typisk kunne nå til patienten hurtigt, mens et specialiseret hentehold kan være flere timer undervejs. Anvendes et specialiseret hentehold, vil det ofte under fremkørslen kontakte henvisende afdeling, opdatere på forventet ankomst og stå for videre vejledning af det lokale team. Ved ankomst til patienten introduceres alle involverede med navn og rolle, og der hilses på familien. Der gøres struktureret overlevering. Det lokale team har nogle gange været presset. Det er væsentligt, at anerkende den store indsats og ikke fejlfinde på detaljer. Patienten tilses af den transporterende læge. Vitalparametre, pumpe og respiratorindstillinger noteres. Transporterende læge vurderer om patienten kan flyttes, eller om yderligere stabiliserende tiltag skal forsøges. Skønt transporterende læge nu overtager ansvaret, er det fortsatte samarbejde vigtigt, og det lokale team bør forblive tilgængeligt. De har historikken og lokalkendskabet til sygehuset.
Transportklar? Faktaboks 2 Væsentlige mål for klargøring
Airway
- intubation undervejs er ikke hensigtsmæssigt – intubér ved tvivl
- tuberelaterede problemer ses hyppigt. Røntgen af thorax anbefales til kontrol af placering før transport
- tube forsvarligt fixeret
- waveform kapnografi tilsluttet
- sug tjekket og katetre klar, der passer til tuben
Breathing
- det intuberede barn bør være optimeret på respirator inden afgang
- ved neurokritisk tilstand bør forskellen i ETCO2 og pCO2 dokumenteres og anvendes til at guide ventilation under transport. Kapillær eller venøs prøve kan anvendes såvel som arteriel
- pleuradræn tilsluttet ensretterventil (Heimlich) eller trevejshane til intermitterende sug. Større drænboks uhensigtsmæssig
- ventrikel-sonde til passivt overløb hos børn, der er intuberede eller i NCPAP
Circulation
- sufficient væskeresuscitation udført, og hvis relevant, påbegyndt eller klargjort inotropi/vasopressor
- tilstrækkeligt antal fungerende adgange til infusioner
- ledig adgang til bolusmedicin
- CVK kan undtagelsesvist være nødvendig før afgang
Disability
- sufficient smertestillet
- sikker krampekontrol og neuroprotektiv behandling, hvor indiceret
- det intuberede barn skal være sederet og kan undertiden med fordel paralyseres under transport for at undgå dyssynkroni med påvirkning af oxygenering og ventilation
- blodsukker-kontrol
Exposure
- der bør være taget relevante dyrkninger og startet indiceret empirisk antibakteriel / antiviral behandling og dosis/tidspunkt journaliseret
- termokontrol er vigtig. Sørg for at måle temperatur
Det interhospitale transportmiljø er udfordret af vanskelige og risikofyldte arbejdsbetingelser.
Der skal sikres bedst opnåelige stabilisering af barnet inden transport, for at undgå at skulle udføre interventioner undervejs. Væsentlige mål for klargøring ses i ovenstående faktaboks 2. Procedurer, som kunne blive nødvendige en route, skal overvejes udført inden afgang. Intubation kan være indiceret hos børn, man i det mere sikre hospitalsmiljø ville se an. Det er vigtigt at forholde sig til mulig klinisk udvikling på transporten. Filosofien er “det, der kan gå galt, vil gå galt” og “et stort problem er et lille problem, der ikke blev håndteret rettidigt”. Kliniske forværringer som desaturation, hypotension, kramper og ICP-stigning skal kunne håndteres hurtigt. Der er undtagelser af udtalt tidskritisk karakter, hvor patienten grundlæggende ikke kan stabiliseres, og alle interventioner skal afvejes i forhold til tidsforbrug. Denne afvejning er dynamisk, og bygger på klinisk erfaring og kompetencerne hos teamet. Der kan efter behov konfereres med modtagende børnecenter om disse valg.
Når patienten vurderes klar til transporten, skiftes monitorering, infusioner og ventilation til transportteamets udstyr. Tubefiksering og intravenøse adgange kontrolleres. Der sikres passende ekstra kapacitet af medicin, infusioner, batteritid og ilt. Patienten flyttes til båre eller kuvøse. I.v.-adgange skal være nemt tilgængelige og kabler og slanger ligge i orden. Systematik og omhu er afgørende. Det anbefales, at man inden afgang fra hospitalets ”sikre ramme” gør status på klinisk tilstand, udstyr og plan. Tjekliste kan benyttes, og er vist at nedsætte antallet af adverse events.
Familien
Familien til det kritisk syge barn skal, uanset barnets tilstand, have mulighed for at være tæt på barnet under stabilisering. Der bør allokeres personale alene til, at stå med familien og forklare hvad der sker. Inden transport skal det sikres, at familien forstår, hvorfor og hvorhen barnet transporteres. Transporterende læge bør stå for dette, så familien får et ansigt på den, som tager vare på barnet under adskillelsen. Om muligt medbringes en eller begge forældre i ambulancen.
Hvis familien vælger at køre selv, skal det vurderes, om det er forsvarligt. Der skal sikres ro omkring kontakt og ”på gensyn” inden afgang.
Transport og overlevering
Udrykningskørsel er forbundet med øget risiko for uheld, og ambulancer har dårlig sikkerhed ved kollisioner. Samtidig er børn og særligt nyfødte fastspændt mindre effektivt end voksne. Af hensyn til alles sikkerhed, bør ambulancen kun undtagelsesvis køre hurtigere end den øvrige trafik. I så fald må politieskorte overvejes.
Under transport kontaktes modtagende afdeling med melding om ankomsttidspunkt og patientens tilstand. Ved ankomst prioriteres struktureret rapport til det modtagende team, inden fokus overtages af praktisk forflytning af patient og udstyr. Herefter overgår behandlingsansvaret til modtagende afdeling

