Kontaktperson
Sundhedsstyrelsen Islands Brygge 67, 2300 København S
NKRsekretariat@sst.dk
72 22 74 00 ww.sst.dk
Sponsorer / Finansiering
Sundhedsstyrelsen
Ansvarsfraskrivelse
Sundhedsstyrelsens nationale kliniske retningslinjer er systematisk udarbejdede udsagn med inddragelse af relevant sagkundskab. Nationale kliniske retningslinjer kan bruges af fagpersoner, når de skal træffe beslutninger om passende og god klinisk sundhedsfaglig ydelse i specifikke situationer. De nationale kliniske retningslinjer er offentligt tilgængelige, således at borgere og patienter også kan orientere sig i retningslinjerne.
Nationale kliniske retningslinjer klassificeres som faglig rådgivning, hvilket indebærer, at Sundhedsstyrelsen anbefaler relevante fagpersoner at følge retningslinjerne. De nationale kliniske retningslinjer er ikke juridisk bindende, og det vil altid være det faglige skøn i den konkrete kliniske situation, der er afgørende for beslutningen om passende og korrekt sundhedsfaglig ydelse. Der er ingen garanti for et succesfuldt behandlingsresultat, selvom sundhedspersoner følger anbefalingerne. I visse tilfælde kan en behandlingsmetode, som ikke er anbefalet, være at foretrække, fordi den passer bedre til patientens situation. Sundhedspersoner skal generelt inddrage patienten, når de vælger behandling.
ISBN elektronisk 2. udgave: 978-87-7014-219-9
Screening for delirium med psykometrisk værktøj (2016)

Forebyggelse af delirium med multikomponent non-farmakologisk intervention (2016)

Multikomponent non-farmakologisk behandling ved delirium (2016)

Skærmede omgivelser (2016)

Aktiv inddragelse og undervisning i delirium af pårørende (2016)

Medicingennemgang og -justering (2016)
Behandling med antipsykotika (2020)

Behandling med benzodiazepin og benzodiazepin-lignende stoffer (2016)

Behandling med melatonin (2016)

Behandling med elektro-konvulsiv terapi (ECT) (2016)

Læsevejledning
Retningslinjen er bygget op i to lag:
1. Lag – Anbefalingen
![]()
Der gives en stærk anbefaling for, når der er evidens af høj kvalitet, der viser, at de samlede fordele ved interventionen er klart større end ulemperne. Det betyder, at alle, eller næsten alle, patienter vil ønske den anbefalede intervention.
![]()
Der gives en stærk anbefaling imod, når der er evidens af høj kvalitet, der viser, at de samlede ulemper ved interventionen er klart større end fordelene. Der anvendes også en stærk anbefaling imod, når gennemgangen af evidensen viser, at en intervention med stor sikkerhed er nyttesløs.
![]()
Der gives en svag/betinget anbefaling for interventionen, når det vurderes, at fordelene ved interventionen er større end ulemperne, eller den tilgængelige evidens ikke kan udelukke en væsentlig fordel ved interventionen, samtidig med at det vurderes, at skadevirkningerne er få eller fraværende. Denne anbefaling anvendes også, når det vurderes, at patienters præferencer varierer.
![]()
Der gives en svag/betinget anbefaling imod interventionen, når det vurderes, at ulemperne ved interventionen er større end fordelene, men hvor dette ikke er underbygget af stærk evidens. Denne anbefaling anvendes også, hvor der er stærk evidens for både gavnlige og skadelige virkninger, men hvor balancen mellem dem er vanskelige at afgøre. Ligeledes anvendes den også, når det vurderes, at patientens præferencer varierer.
![]()
God praksis anvendes, når der ikke foreligger relevant evidens, og bygger således på faglig konsensus blandt medlemmerne af arbejdsgruppen, der har udarbejdet den kliniske retningslinje. Anbefalingen kan være enten for eller imod interventionen. Da der er tale om faglig konsensus, er denne type anbefaling svagere end de evidensbaserede anbefalinger, uanset om de evidensbaseret er stærke eller svage.
Se bilag “Beskrivelse af anbefalingernes styrke og implikationer” for mere information
2. Lag – Grundlaget for anbefalingen
Klik på anbefalingen, hvis du vil vide mere om grundlaget for anbefalingen
Evidensprofilen: De samlede effektestimater samt referencer til studierne.
Sammenfatning: Overblik over samt kort gennemgang af den tilgrundliggende evidens
Kvaliteten af evidensen:
Høj: Vi er meget sikre på, at den sande effekt ligger tæt på den estimerede effekt
Moderat: Vi er moderat sikre på den estimerede effekt. Den sande effekt ligger sandsynligvis tæt på denne, men der er en mulighed for, at den er væsentligt anderledes
Lav: Vi har begrænset tiltro til den estimerede effekt. Den sande effekt kan være væsentligt anderledes end den estimerede effekt
Meget lav: Vi har meget ringe tiltro til den estimerede effekt. Den sande effekt vil sandsynligvis være væsentligt anderledes end den estimerede effekt.
Nøgleinformation: Kort beskrivelse af gavnlige og skadelige virkninger, kvaliteten af evidensen og overvejelser om patientpræferencer.
Rationale: Beskrivelse af hvorledes de ovenstående elementer blev vægtet i forhold til hinanden og resulterede i den aktuelle anbefalings retning og styrke.
Praktiske oplysninger: Praktisk information vedrørende behandlingen og oplysninger om eventuelle særlige patientovervejelser.
Adaption: Såfremt anbefalingen er adapteret fra en anden retningslinje, findes her en beskrivelse af eventuelle ændringer.
Diskussion: Hvis du er logget ind som bruger, kan du her komme med kommentarer til specifikke anbefalinger.
Referencer: Referenceliste for anbefalingen.
Den anvendte graduering af evidensens kvalitet og anbefalingsstyrke baseres på GRADE (Grading of Recommendations Assessment, Development and Evaluation). For en hurtig og informativ intriduktion til GRADE anbefales følgende artikel G.Goldet, J.Howick. Understanding GRADE: an introduction. Journal of Evidence-Based Medicine 6 (2013) 50-54. Se også: http://www.gradeworkinggroup.org.
Desuden henvises der til Sundhedsstyrelsens metodehåndbog for en overordnet introduktion til metoden bag udarbejdelsen af de Nationale Kliniske Retningslinjer.
Indledning
Formål
Formålet med de nationale kliniske retningslinjer er at sikre en evidensbaseret indsats af ensartet høj kvalitet på tværs af landet, medvirke til hensigtsmæssige patientforløb og vidensdeling på tværs af sektorer og faggrupper samt prioritering i sundhedsvæsenet.
En national klinisk retningslinje indeholder alene konkrete handlingsanvisninger indenfor udvalgte, velafgrænsede kliniske problemstillinger (dvs. hvad der skal gøres og hvem er det relevant for). Den har ikke som primært formål at afklare visitation og organisering af indsatsen (hvem skal tilbydes indsatsen, hvem der skal tilbyde indsatsen) eller samfundsøkonomiske konsekvenser (hvad er den afledte effekt på ressourcerne og er disse til stede). Disse typer af problemstillinger kan eksempelvis håndteres i en visitationsretningslinje, et pakkeforløb, et forløbsprogram, et referenceprogram eller en medicinsk teknologivurdering (MTV).
Denne retningslinjes formål er at sikre relevant opsporing, forebyggelse og behandling af organisk delirium. Patienter med delirium har en dårlig prognose med markant øget risiko for død, funktionstab og længerevarende kognitive problemer. Relevant udredning og behandling af udløsende årsager er derfor afgørende og det forudsættes, at der hos alle delirøse patienter foretages relevant udredning. Udredningen skal tage sigte på at identificere udløsende årsager. Det forudsættes også, at der sikres behandling af disse samtidig med understøttende behandling og somatisk stabilisering. Så længe patienten er midlertidigt inhabil, kan behandling foretages i henhold til sundhedsloven § 19. Fyldestgørende information til patienten og de pårørende er væsentlig i henhold til sundhedslovens § 20.
Denne retningslinje er en opdatering af den oprindelige retningslinje fra 2016 og erstatter den tidligere version af retningslinjen for forebyggelse og behandling af organisk delirium.
Afgrænsning af patientgruppe
Den primære patientgruppe er ældre (>65år) med delirium eller risiko for at udvikle delirium, som er indlagt på somatisk afdeling. Risikofaktorer for udvikling af delirium er høj alder, demens eller kognitiv dysfunktion, funktionsnedsættelse og akut sygdom samt skrøbelighed.
Da delirium også forekommer i andre patientgrupper, herunder plejehjemsbeboere i primær sektor, terminale patienter og intensivpatienter, er retningslinjen også målrettet dem. Ved de enkelte PICO-spørgsmål er beskrevet hvilke patientgrupper, der er inkluderet i evidens-søgningen.
Delirøse tilstande i relation til psykiske sygdomme eller tilstande, som er forårsaget af misbrug og abstinenser, er ikke behandlet i denne retningslinje, da disse tilstande er af anden genese og behandles anderledes end organisk delirium, der udløses af fysisk sygdom eller påvirkning.
Litteraturen i denne NKR bygger på kriterierne i DSM-III-R eller DSM-IV (Diagnostic and Statistical Manual of Mental Disorders (6)) som guldstandard for diagnostik af delirium, vurderet ved interview af psykiatrisk specialist.
Målgruppe/brugere
Den nationale kliniske retningslinje for delirium er primært henvendt til sundhedspersonale, der diagnosticerer, behandler samt varetager pleje- og omsorg for patienter med delirium eller risiko for udvikling af delirium.
Retningslinjen er også relevant for patienter med delirium og deres pårørende i samråd med behandlende sundhedspersonale.
Emneafgrænsning
Den nationale kliniske retningslinje indeholder handlingsanvisninger for udvalgte og velafgrænsede kliniske problemstillinger (’punktnedslag i patientforløbet’). Disse problemstillinger er prioriteret af den faglige arbejdsgruppe som de områder, hvor det er vigtigst at få afklaret evidensen. Arbejdsgruppen har valgt at fokusere på effekten af opsporing og tidlig diagnostik af delirium, samt belyse evidensen af forebyggende tiltag og de mest brugte behandlinger af delirøse patienter.
Følgende ti fokuserede spørgsmål er udvalgt til retningslinjen:
- Bør alle akut syge nyindlagte patienter over 65 år screenes for delirium med psykometrisk værktøj (b-CAM eller CAM)?
- Bør patienter med risiko for delirium have non-farmakologisk multikomponent behandling?
- Bør patienter med delirium have non-farmakologisk multikomponent behandling?
- Bør patienter med delirium have skærmede omgivelser?
- Bør pårørende aktivt inddrages i behandling af patienter med delirium?
- Bør patienter med delirium få pauseret ikke-livsvigtig medicin?
- Bør patienter med delirium behandles med antipsykotika?
- Bør patienter med delirium behandles med benzodiazepiner eller benzodiazepinlignende midler?
- Bør patienter med delirium behandles med melatonin?
- Bør patienter med behandlingsrefraktært delirium behandles med ECT?
Rationale for valg af opdatering i 2020
Beslutningen om at opdatere retningslinjen blev truffet, da arbejdsgruppen vurderede, at der var kommet ny evidens på området, siden den første retningslinje udkom i 2016. Det har som udgangspunkt ikke været muligt at stille nye fokuserede spørgsmål i opdateringen, hvorfor der kun tages stilling til de eksisterende fokuserede spørgsmål fra 2016, og på baggrund af disse er der søgt efter ny litteratur. Der kan være foretaget layoutmæssige ændringer i de fokuserede spørgsmål samt tilhørende kapitler, der ikke er opdateret i 2020.
Følgende fokuserede spørgsmål blev valgt ud til opdatering, da der var udkommet flere metaanlyser og systematiske reviews:
PICO 7: Bør patienter med delirium behandles med antipsykotika?
Patient perspektivet
Det er vigtigt, at patientens værdier og præferencer løbende inddrages i patientforløbet.
I den oprindelige retningslinje fra 2016 blev patientperspektivet repræsenteret via Ældre Sagen og Danske Patienter, som udpegede medlemmer til den nedsatte referencegruppe. Derudover har de haft mulighed for at afgive høringssvar til udkastet til den færdige retningslinje.
I opdateringsfasen i 2020 blev selskaber fra den oprindelige arbejdsgruppe inviteret til at deltage i en ny arbejdsgruppe, ligesom den opdaterede version blev sendt i offentlig høring med opfordring til udvalgte organisationer, selskaber og foreninger til at afgive høringssvar, herunder Ældre Sagen og Danske Patienter.
Se medlemmerne af referencegruppen i afsnittet “arbejdsgruppen og referencegruppen”.
Screening for delirium med psykometrisk værktøj (2016)
Ældre patienter med akut sygdom er i høj risiko for at udvikle delirium. Delirium kan vise sig i flere former, herunder hyperaktive, hypoaktive og blandede former, hvor særligt de hypoaktive kan overses i den kliniske hverdag. Patienter med uopdaget delirium har markant øget dødelighed i forhold til diagnosticerede delirøse patienter 30,8% vs. 11,8% (38).
Der findes mange psykometriske tests, hvoraf Confusement Assesssment Method (CAM) er den mest udbredte i klinikken (41). Den findes i to former, long-CAM (10 kriterier), der er et omfattende værktøj til identifikation af kognitive problemer og short-CAM (4 kriterier), der er specifikt målrettet identifikation og erkendelse af delirium og, den hyppigst anvendte i klinisk sammenhæng. CAM-ICU og B-CAM repræsenterer korte udgaver af CAM til henholdsvis kritisk syge intuberede patienter og ikke-kritisk syge patienter (35). CAM-ICU er valideret i dansk sammenhæng, mens B-CAM aktuelt er under validering. Long-CAM er p.t. ikke valideret i en dansk kontekst.
Patienten vurderes i forbindelse med samtale. Der er mistanke om delirium, hvis patienten opfylder kriterium 1 og 2 samt enten 3 eller 4:
1. Akut indsættende og fluktuerende forløb
2. Uopmærksomhed
3. Uorganiseret tankegang
4. Ændret bevidsthedsniveau
Uddannelse og træning i brug af diagnostisk værktøj er essentielt for at sikre høj diagnostisk sikkerhed (73).

Nøgleinformationer


Rationale
Arbejdsgruppen vægtede i anbefalingen, at delirium ofte ikke er erkendt, når der ikke bruges et systematisk værktøj, særligt hos patienter med hypoaktivt delirium (38). CAM, især B-CAM, er relativt hurtige tests at udføre. Der er høj diagnostisk sikkerhed hos trænet personale. Da testen ikke er forbundet med betydende ubehag for patienten eller alvorlige skadevirkninger, forventer arbejdsgruppen, at de fleste patienter vil tage imod tilbud om test. Der blev ikke fundet brugbar evidens på området, så arbejdsgruppen har på baggrund af klinisk erfaring formuleret en god praksis anbefaling.
Idet delirium er en fluktuerende tilstand, anbefaler arbejdsgruppen at gentage eventuelt negative tests hos patienter med risiko for delirium nogle timer eller dage efter første test for at sikre korrekt diagnostik.
Fokuseret Spørgsmål
Population: Akut indlagte patienter (på hospital eller plejeafsnit i primærsektor) over 65 år. Ekskluderede patienter: patienter indlagt på intensivafdeling og palliative patienter
Intervention: Screening med Confusement Assessment Method (CAM) eller Brief Confusement Assessment Method (bCAM)
Sammenligning: Ingen screening med psykometrisk værktøj

Referencer
35. Han JH, Wilson A, Vasilevskis EE, Shintani A, Schnelle JF, Dittus RS, et al. : Diagnosing delirium in older emergency department patients: validity and reliability of the delirium triage screen and the brief confusion assessment method. Annals of emergency medicine 2013;62(5):457-65 Pubmed Journal
38. Kakuma R., du Fort GG, Arsenault L., Perrault A., Platt RW, Monette J., et al. : Delirium in older emergency department patients discharged home: effect on survival. Journal of the American Geriatrics Society 2003;51(4):443-450
41. LaMantia MA, Messina FC, Hobgood CD, Miller DK : Screening for delirium in the emergency department: a systematic review. Annals of Emergency Medicine 2014;63(5):551-560.e2 Journal
73. Wong CL, Holroyd-Leduc J., Simel DL, Straus SE : Does this patient have delirium?: value of bedside instruments. Jama 2010;304(7):779-786 Journal
Forebyggelse af delirium med multikomponent non-farmakologisk intervention (2016)
Udvikling af delirium skyldes samspil mellem risikofaktorer hos den skrøbelige patient samt fysiske stressfaktorer i forbindelsen med akut og/eller alvorlig sygdom, som bør udredes og behandles (54).
Multikomponent non-farmakologisk forebyggende behandling sigter efter at reducere kendte risikofaktorer for delirium så delirium undgås eller at varighed og sværhedsgrad reduceres. Arbejdsgruppen har i dette spørgsmål valgt at fokusere på følgende risikofaktorer:
- Svækkede sanser, fx. nedsat syn og hørelse.
- Orienteringsbesvær og forvirring, som kan udvikle sig til vrangforestillinger.
- Immobilisering, enten som følge af den somatiske sygdom eller som forekommer ved hypoaktivt delirium.
- Nedsat føde- og væskeindtag og/eller øget behov.
- Forstyrret døgnrytme/manglende nattesøvn.

Nøgleinformationer

Rationale
Der er ved formulering af anbefalingen lagt vægt på, at forebyggende behandling med non-farmakologisk multikomponent intervention overvejende viste positiv effekt på alle outcomes, og ikke vurderes at have skadelige virkninger. Arbejdsgruppen har moderat tiltro til effekten af interventionen på delirium forekomst, delirium varighed og forekomst af tryksår. Der er dog lav tiltro til effekten på mortalitet (både under indlæggelse og efter 12 måneder), forbedring af ADL-funktion, fald og udskrivelse til vanlig bolig. Interventionen vurderes til ikke at være præferencefølsom.
Fokuseret Spørgsmål
Population: Akut indlagte (på hospital eller plejeafsnit i primær sektor) patienter over 65 år med somatisk sygdom samt mindst en af nedenstående risikofaktorer: Demens, Mb, Parkinson, Tidligere apopleksi, Tidligere delirium, Lav funktionsevne eller flere kroniske sygdomme.
Intervention: Multikomponent non-farmakologisk intervention som indeholder to eller flere af følgende: Skemalagt fysisk aktivitet flere gange dagligt, fx i forbindelse med måltider og pleje. Sanseoptimering, eksempelvis briller, høreapparat, lys på stuen. Reorientering, eksempelvis information om tid, sted og egne data. Ernæring med fokus på at sikre nødvendigt væske/føde indtag. Struktureret døgnrytme med fokus på, at patienten er vågen om dagen samt pleje, undersøgelser mm. i videst muligt omfang foregår i dagtid, og der er ro og mørke på stuen om natten.
Sammenligning: Vanlig behandling


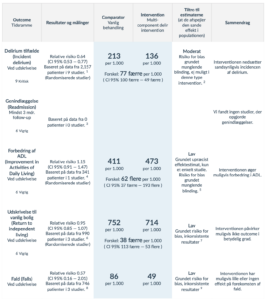

1. Systematisk oversigtsartikel [77] med inkluderede studier: Martinez 2012, Lundstrom 2007, Jeffs 2013, Abizanda 2011, Hempenius 2013, Guo 2016, Bonaventura 2007, Avendano Cespedes 2016, Moon 2015. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
2. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
3. Systematisk oversigtsartikel [77] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
4. Systematisk oversigtsartikel [77] med inkluderede studier: Abizanda 2011. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
5. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Only data from one study. Publikationsbias: Ingen betydelig.
6. Systematisk oversigtsartikel [77] med inkluderede studier: Lundstrom 2007, Jeffs 2013, Hempenius 2013. Baselinerisiko/ komparator: Kontrolarm i reference brugt til interventionen.
7. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Alvorligt. The direction of the effect is not consistent between the included studies. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
8. Systematisk oversigtsartikel [77] med inkluderede studier: Martinez 2012, Lundstrom 2007, Hempenius 2013. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
9. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Alvorligt. The direction of the effect is not consistent between the included studies. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
10. Systematisk oversigtsartikel [77] med inkluderede studier: Hempenius 2013, Lundstrom 2007. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
11. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
12. Systematisk oversigtsartikel [77] med inkluderede studier: Lundstrom 2007, Hempenius 2013, Avendano Cespedes 2016, Abizanda 2011, Moon 2015. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
13. Risiko for bias: Ingen betydelig. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Alvorligt. The direction of the effect is not consistent between the included studies. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
14. Systematisk oversigtsartikel [77] med inkluderede studier: Lundstrom 2007. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
15. Risiko for bias: Ingen betydelig. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Meget alvorligt. Only data from one study, Low number of events, Wide confidence intervals. Publikationsbias: Ingen betydelig.
16. Systematisk oversigtsartikel [77] med inkluderede studier: Guo 2016, Avendano Cespedes 2016, Lundstrom 2007, Jeffs 2013, Martinez 2012. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
17. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
18. Systematisk oversigtsartikel [77] med inkluderede studier: Avendano Cespedes 2016, Jeffs 2013, Hempenius 2013. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
19. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
20. Systematisk oversigtsartikel [77] med inkluderede studier: Abizanda 2011, Martinez 2012, Jeffs 2013, Hempenius 2013, Lundstrom 2007. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
21. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Manglende blinding. Inkonsistente resultater: Alvorligt. The confidence interval of some of the studies do not overlap with those of most included studies/ the point estimate of some of the included studies., Konfidenintervallerne i de inkluderede studier overlapper ikke. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
Referencer
1. Abizanda P., Leon M., Dominguez-Martin L., Lozano-Berrio V., Romero L., Luengo C., et al. : Effects of a short-term occupational therapy intervention in an acute geriatric unit. A randomized clinical trial. Maturitas 2011;69(3):273-278 Journal
7. Avendano-Cespedes A, Garcia-Cantos N, Gonzalez-Teruel M, Martinez-Garcia M, Villarreal-Bocanegra E, Oliver-Carbonell J, et al. : Pilot study of a preventive multicomponent nurse intervention to reduce the incidence and severity of delirium in hospitalized older adults: MID-Nurse-P. Maturitas 2016;86 86-94
11. Bonaventura M., Zanotti R. : Effectiveness of IPD treatment for delirium prevention in hospitalized elderly. A controlled randomized clinical trial. Professioni infermieristiche 2007;60(4):230-236
32. Guo Y, Sun L, Li LI, Jia P, Zhang J, Jiang H, et al. : Impact of multicomponent, nonpharmacologic interventions on perioperative cortisol and melatonin levels and postoperative delirium in elderly oral cancer patients. Archives of Gerontology and Geriatrics 2016;62 112-7
36. Hempenius L., Slaets JP, van Asselt D., de Bock GH, Wiggers T., van Leeuwen BL : Outcomes of a Geriatric Liaison Intervention to Prevent the Development of Postoperative Delirium in Frail Elderly Cancer Patients: Report on a Multicentre, Randomized, Controlled Trial. PloS One 2013;8(6):e64834 Journal
37. Jeffs KJ, Berlowitz DJ, Grant S, Lawlor V, Graco M, de Morton N, et al. : An enhanced exercise and cognitive programme does not appear to reduce incident delirium in hospitalised patients: a randomised controlled trial. BMJ open 2013;3(6):
47. Lundstrom M., Olofsson B., Stenvall M., Karlsson S., Nyberg L., Englund U., et al. : Postoperative delirium in old patients with femoral neck fracture: a randomized intervention study. Aging clinical and experimental research 2007;19(3):178-186
48. Martinez FT, Tobar C., Beddings CI, Vallejo G., Fuentes P. : Preventing delirium in an acute hospital using a nonpharmacological intervention. Age and Ageing 2012;41(5):629-634 Journal
52. Moon K-J, Lee S-M : The effects of a tailored intensive care unit delirium prevention protocol: A randomized controlled trial. International journal of nursing studies 2015;52(9):1423-32
54. National Institute for Health and Care Excellence (NICE) : Delirium: prevention, diagnosis and management (CG 103). NICE, 2010;Clinical Guideline 103 Link
77. NKR delir PICO 2 Multikomponent hos patienter med risiko for delir.
Multikomponent non-farmakologisk behandling ved delirium (2016)
Udvikling af delirium skyldes sandsynligvis et samspil mellem risikofaktorer hos den skrøbelige patient samt fysiske stressfaktorer i forbindelse med akut og/eller alvorlig sygdom (54). Multikomponent non-farmakologisk behandling sigter efter at reducere flere af disse risikofaktorer, så delirium tilstandens varighed og sværhedsgrad reduceres. Arbejdsgruppen har i dette spørgsmål valgt at fokusere på følgende risikofaktorer:
- Svækkede sanser, eksempelvis nedsat syn og hørelse.
- Orienteringsbesvær og forvirring, som kan udvikle sig til vrangforestillinger.
- Immobilisering, enten som følge af den somatiske sygdom eller som følge af hypoaktivt delirium.
- Nedsat føde- og væskeindtag.
- Forstyrrelse af døgnrytme og nattesøvn.

Nøgleinformationer
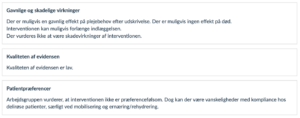
Rationale
I formuleringen af anbefalingen er der blevet lagt vægt på, at der muligvis er en gavnlig effekt på plejebehov efter udskrivelsen. Der er sandsynligvis lille eller ingen effekt på mortalitet, og muligvis let øget indlæggelsestid som følge af interventionen. Det blev ligeledes vægtet, at der ikke er alvorlige skadevirkninger af interventionen og interventionen ikke er præferencefølsom.
Fokuseret Spørgsmål
Population: Patienter over 65 år med delirium, inkl. intensiv patienter, patienter i primær sektor.
Intervention: Multikomponent non-farmakologisk intervention som indeholder to eller flere af følgende interventioner: Skemalagt fysisk aktivitet flere gange dagligt fx i forbindelse med måltider og pleje. Sanseoptimering, eksempelvis briller, høreapparat og lys på stuen. Reorientering, eksempelvis information om tid, sted og egne data. Ernæring medfokus på at sikre nødvendigt væske/føde indtag. Struktureret døgnrytme med fokus på, at patienten er vågen om dagen samt at pleje, undersøgelser mm. i videst muligt omfang foregår i dagtid, og der er ro og mørke på stuen om natten.
Sammenligning: Vanlig behandling

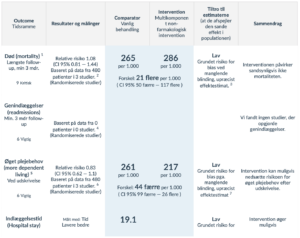

1. Obs. der er kun data for 8 ugers follow-up.
2. Systematisk oversigtsartikel [78] med inkluderede studier: Pitkala 2006, Cole 2002, Cole 1994. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
3. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Wide confidence intervals. Publikationsbias: Ingen betydelig.
4. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
5. Øget plejebehov defineret ved behov for øget hjælp eller flytning til anden bolig.
6. Systematisk oversigtsartikel [78] med inkluderede studier: Cole 2002, Cole 1994, Pitkala 2006. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
7. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Wide confidence intervals. Publikationsbias: Ingen betydelig.
8. Systematisk oversigtsartikel [78] med inkluderede studier: Pitkala 2006, Cole 2002. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
9. Risiko for bias: Alvorligt. Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias. Inkonsistente resultater: Alvorligt. The magnitude of statistical heterogeneity was high, with I^2: 58 %.. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Publikationsbias: Ingen betydelig.
10. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
11. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
12. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
13. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
14. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
15. Systematisk oversigtsartikel [78] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
Referencer
19. Cole MG, McCusker J., Bellavance F., Primeau FJ, Bailey RF, Bonnycastle MJ, et al. : Systematic detection and multidisciplinary care of delirium in older medical inpatients: a randomized trial. CMAJ : Canadian Medical Association journal = journal de l’Association medicale canadienne 2002;167(7):753-759
20. Cole MG, Primeau FJ, Bailey RF, Bonnycastle MJ, Masciarelli F., Engelsmann F., et al. : Systematic intervention for elderly inpatients with delirium: a randomized trial. CMAJ : Canadian Medical Association journal = journal de l’Association medicale canadienne 1994;151(7):965-970
54. National Institute for Health and Care Excellence (NICE) : Delirium: prevention, diagnosis and management (CG 103). NICE, 2010;Clinical Guideline 103 Link
59. Pitkala KH, Laurila JV, Strandberg TE, Tilvis RS : Multicomponent geriatric intervention for elderly inpatients with delirium: a randomized, controlled trial. The journals of gerontology. Series A, Biological sciences and medical sciences. 2006;61(2):176-181
78. NKR delir PICO 3 Multikomponent behandling.
Skærmede omgivelser (2016)
Manglende søvn nedsætter kognitiv performance.Studier på raske søvn-depriverede og på delirøse viser lignende ændringer i cerebral perfusion og metabolisme (45), og søvnforstyrrelser betragtes som risikofaktor for udvikling af delirium. På en hospitalsafdeling for akutte sygdomme er der ofte uro/støj hele døgnet i forbindelse med pleje og behandling af patienter samt alarmer på monitoreringsudstyr. Dette opleves særligt på gangpladser og flersengsstuer og kan forstyrre patientens nattesøvn. Arbejdsgruppen ønskede derfor at undersøge evidensen for, hvorvidt skærmede omgivelser kan have en effekt på behandlingen af delirium. Skærmede omgivelser betragtes i denne sammenhæng som at undgå forstyrrende og uvedkommende stimuli, og kan opnås ad flere veje:
- Rolige omgivelser, fx. enestue
- Tilrettelæggelse af pleje, undersøgelser og behandling, så det foregår i patientens vågne timer.

Nøgleinformationer
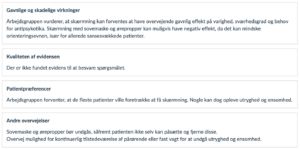
Rationale
Ved formulering af anbefalingen vægtede arbejdsgruppen, at der sandsynligvis ikke findes skadevirkninger af interventionen, og klinisk erfaring tyder på øget forekomst og forværring af delirium ved mange forstyrrelser og uvedkommende stimuli. Arbejdsgruppen vurderer, at interventionen ikke er præferencefølsom.
Aktiv inddragelse og undervisning i delirium af pårørende (2016)
Den pårørende er en vigtig samarbejdspartner omkring den akut syge patient, og er hos den ældre medicinske patient ofte en ægtefælle/partner eller voksne børn. At være pårørende til en patient med delirium kan være en skræmmende oplevelse, da pårørende tit ikke forstår årsagen til den ofte dramatiske ændring i patientens adfærd og ikke er vidende om, at tilstanden som hovedregel er reversibel (23). Som pårørende kan det være svært at håndtere en agiteret patient, og særligt hos den terminale patient kan delirium forhindre en meningsfuld og værdig afsked (15)
Belastningen af de pårørende til delirøse patienter menes at mindskes ved oplysning om tilstanden, og pårørende kan muligvis opdage symptomer på begyndende delirium hurtigere end personalet i kraft af deres nære kendskab til patienten (15)(34).
Arbejdsgruppen ønskede at belyse effekten af aktiv inddragelse af pårørende på patienter med delirium. Den aktive inddragelse kan eksempelvis bestå i:
- Oplysning om/undervisning i delirium
- Medinddragelse i beslutningstagen
- Indbydende omgivelser til besøg og samvær

Nøgleinformationer
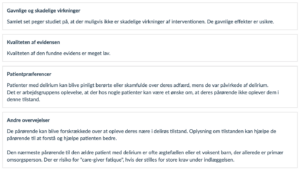
Rationale
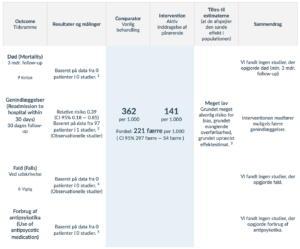
Ved formulering af anbefalingen vægtede arbjedsgruppen, at kvaliteten af evidensen er meget lav, men der tyder ikke på at være skadelige virkninger af interventionen.
Fokuseret Spørgsmål
Population: Patienter over 65 år med delirium
Intervention: Aktiv inddragelse af pårørende (fx inddragelse i daglige aktiviteter og gøremål, overnatningsmulighed)
Sammenligning: Vanlig behandling



1. Systematisk oversigtsartikel [79] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
2. Systematisk oversigtsartikel [79] med inkluderede studier: Boltz 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
3. Risiko for bias: Meget alvorligt. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Inadequate concealment of allocation during randomization process, resulting in potential for selection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Due to risk of confounding. Upræcist effektestimat: Alvorligt. Only data from one study. Publikationsbias: Ingen betydelig.
4. Systematisk oversigtsartikel [79] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
5. Systematisk oversigtsartikel [79] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
6. Systematisk oversigtsartikel [79] med inkluderede studier: Boltz 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
7. Risiko for bias: Meget alvorligt. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Inadequate concealment of allocation during randomization process, resulting in potential for selection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Differences between the intervention/comparator of interest and those studied. Upræcist effektestimat: Alvorligt. Only data from one study. Publikationsbias: Ingen betydelig.
8. Systematisk oversigtsartikel [79] med inkluderede studier: Boltz 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
9. Risiko for bias: Meget alvorligt. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Inadequate concealment of allocation during randomization process, resulting in potential for selection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Differences between the intervention/comparator of interest and those studied. Upræcist effektestimat: Alvorligt. Only data from one study. Publikationsbias: Ingen betydelig.
10. Systematisk oversigtsartikel [79] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
11. Systematisk oversigtsartikel [79] med inkluderede studier: Boltz 2014, Boltz 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
12. Risiko for bias: Meget alvorligt. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Inadequate concealment of allocation during randomization process, resulting in potential for selection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Differences between the intervention/comparator of interest and those studied. Upræcist effektestimat: Alvorligt. Only data from one study. Publikationsbias: Ingen betydelig.
13. Systematisk oversigtsartikel [79] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
14. Systematisk oversigtsartikel [79] med inkluderede studier: Boltz 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
15. Risiko for bias: Meget alvorligt. Inadequate sequence generation/ generation of comparable groups, resulting in potential for selection bias, Inadequate concealment of allocation during randomization process, resulting in potential for selection bias, Inadequate/lack of blinding of participants and personnel, resulting in potential for performance bias, Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Differences between the intervention/comparator of interest and those studied. Upræcist effektestimat: Alvorligt. Only data from one study. Publikationsbias: Ingen betydelig.
16. Systematisk oversigtsartikel [79].
17. Risiko for bias: Alvorligt. Risiko for confounding, det var forskelligt mellem grupperne hvem der var omsorgsperson. Cointervention blev ikke opgjort, det kan ikke udelukkes at der var forskellige rehabiliteringstilbud i de to grupper.. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Kun ca. 25% havde delir. Upræcist effektestimat: Meget alvorligt. Kun et dødsfald. Publikationsbias: Ingen betydelig.
Referencer
10. Boltz M, Resnick B, Chippendale T, Galvin J : Testing a family-centered intervention to promote functional and cognitive recovery in hospitalized older adults. Journal of the American Geriatrics Society 2014;62(12):2398-407
15. Carbone MK, Gugliucci MR : Delirium and the Family Caregiver: The Need for Evidence-based Education Interventions. The Gerontologist 2015;55(3):345-52
23. Day J, Higgins I : Adult family member experiences during an older loved one’s delirium: a narrative literature review. Journal of Clinical Nursing 2015;24(11-12):1447-56
34. Halloway S : A family approach to delirium: a review of the literature. Aging & mental health 2014;18(2):129-39
79. NKR delir PICO 5 Familie.
Medicingennemgang og -justering (2016)
Ældre har en højere risiko for medicinbivirkninger. Det kan skyldes ændret farmakokinetik, dvs. ændret evne til at metabolisere lægemidler -og/eller ændret farmakodynamik, dvs. ændret følsomhed for lægemidler. Ældre har også oftere flere kroniske lidelser og får flere lægemidler (69). I litteraturen er beskrevet polyfarmaci (5 eller flere præparater) hos 49,7% af europæiske plejehjemsbeboere, 24,3 % fik udskrevet 10 eller flere præparater (29).
Risikoen for medicinudløst delirium er højere hos skrøbelige ældre og patienter med demenssygdomme og menes at udgøre op mod 31% af alle delirium-tilfælde hos ældre. Særligt opioider, benzodiazepiner, antikolinerge lægemidler og antidepressiva er associeret med delirium, men de fleste farmaka kan medvirke til udvikling af delirium (16).
Arbejdsgruppen ønskede at vurdere evidensen for at foretage medicingennemgang og -pausering hos ældre med delirium. I søgeprocessen fandtes der dog kun litteratur for patienter med risiko for delirium. Arbejdsgruppen har derfor formuleret to anbefalinger for henholdsvis patienter med risiko for delirium og patienter med delirium.

Nøgleinformationer
Rationale
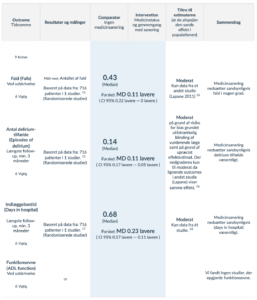
Der er ved formulering af anbefalingen lagt vægt på, at der ikke er fundet studier, der har undersøgt de kritiske outcomes: reboundeffekt og varighed af delirium, hvorfor kvaliteten af evidensen samlet set er lav.
Fokuseret Spørgsmål
Population: Plejehjemsbeboere over 65 år med risiko for delirium
Intervention: Medicinstatus og gennemgang med sanering
Sammenligning: Ingen medicinsanering



1. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014, Lapane 2011. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
2. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Ingen betydelig. Wide confidence intervals. Publikationsbias: Ingen betydelig.
3. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014. Baselinerisiko/komparator: Primærstudie.
4. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Meget alvorligt. Kun data fra ét studie, brede konfidensintervaller. Publikationsbias: Ingen betydelig.
5. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
6. Inkonsistente resultater: Ingen betydelig. Upræcist effektestimat: Alvorligt. Kun data fra ét studie. Publikationsbias: Ingen betydelig.
7. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
8. Risiko for bias: Alvorligt. Utilstrækkelig blinding af vurderende læge.. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Kun data fra ét studie, dog stor population.. Publikationsbias: Ingen betydelig.
9. Risiko for bias: Alvorligt. Inadequate/lack of blinding of outcome assessors, resulting in potential for detection bias. Upræcist effektestimat: Ingen betydelig. Only data from one study.
10. Systematisk oversigtsartikel [80] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
11. Systematisk oversigtsartikel [80] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
12. Systematisk oversigtsartikel [80] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
13. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
14. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Kun data fra ét studie.
15. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
16. Risiko for bias: Alvorligt. Utilstrekkelig/manglende blinding i evalueringen. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Kun data fra ét studie, dog viser lignende outcome i andet studie samme effekt..
17. Systematisk oversigtsartikel [80] med inkluderede studier: Garcia Gollarte 2014. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
18. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Upræcist effektestimat: Alvorligt. Kun data fra ét studie. Publikationsbias: Ingen betydelig.
19. Systematisk oversigtsartikel [80] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
Referencer
16. Catic AG : Identification and management of in-hospital drug-induced delirium in older patients. Drugs & aging 2011;28(9):737-748 Journal
22. Dansk Geriatrisk Selskab, O’Mahony D. : Screening of older persons’ prescriptions (STOPP) version 2 (Dansk oversættelse). Dansk Geriatrisk Selskab 2014;
29. Garcia-Gollarte F, Baleriola-Julvez J, Ferrero-Lopez I, Cuenllas-Diaz A, Cruz-Jentoft A : An educational intervention on drug use in nursing homes improves health outcomes resource utilization and reduces inappropriate drug prescription. Journal of the American Medical Directors Association 2014;15(12):885-91
42. Lapane KL, Hughes CM, Daiello LA, Cameron KA, Feinberg J : Effect of a pharmacist-led multicomponent intervention focusing on the medication monitoring phase to prevent potential adverse drug events in nursing homes. Journal of the American Geriatrics Society 2011;59(7):1238-45
66. Sundhedsstyrelsen. Seponeringslisten 2021 – forslag til seponering af hyppigt anvendte lægemidler hos voksne. Sundhedsstyrelsen, 2020. Opdateret: 20.11.2020. Senest hentet: 19.02.2021. Link
69. van der Cammen TJ, Rajkumar C, Onder G, Sterke CS, Petrovic M : Drug cessation in complex older adults: time for action. Age and Ageing 2014;43(1):20-5
80. NKR 42 Delir PICO 6 Gennemgang af medicin.
Nøgleinformationer

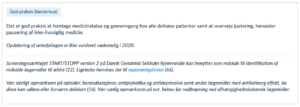
Rationale
Da der ikke er fundet evidens, der besvarer spørgsmålet om effekten af medicin gennemgang og pausering hos patienter med delirium, har arbejdsgruppen formuleret en god praksis anbefaling. Da en del lægemidler kan fremkalde eller forværre delirium hos allerede svækkede patienter, anbefales det at foretage medicin gennem gang og pausering af ikke-livsnødvendige lægemidler. Interventionen vurderes ikke at være præferencefølsom.
Behandling med antipsykotika (2020)
Patienter med delirium fremstår ofte psykotiske, urolige, apatiske og/eller udadreagerende. I behandling af delirøse patienter gives ofte antipsykotika for at mindske disse symptomer. Det er dog usikkert om den gavnlige effekt opvejer de potentielt skadelige. Årsag til delirium er som hovedregel somatisk sygdom og/eller medicinbivirkninger. Behandlingen af den/de udløsende årsager skal iværksættes før eller samtidig med start af antipsykotisk behandling. Den juridiske vejledning om behandling med antipsykotiske lægemidler til personer over 18 år med psykotiske lidelser (70) er rammesættende for behandlingen. Haloperidol er det eneste godkendte antipsykotika til personer med delirium.
Der er siden udgivelsen af retningslinjen i 2016 kommet flere metaanalyser og systematiske reviews, der beskriver patientrelaterede outcomes og sikkerhed af behandling med antipsykotisk medicin.

Nøgleinformationer
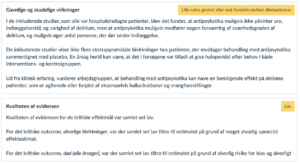

Rationale
Der blev i formuleringen af anbefalingen lagt vægt på, at behandling med antipsykotika muligvis ikke nedsætter varigheden af delirium eller uro i betydelig grad, men at antipsykotika muligvis øger dødeligheden under indlæggelse og medfører nogen forværring af delirium sværhedsgrad. De inkluderede studier viser ikke flere ekstrapyramidale bivirkninger hos patienter, der modtager behandling med antipsykotika sammenlignet med placebo. Tiltroen til evidensen er samlet set lav.
Arbejdsgruppen vurderer på denne baggrund, at der ikke rutinemæssigt kan anbefales behandling med antipsykotika til delirøse patienter. Arbejdsgruppen vurderer dog, at behandling med antipsykotika kan have en beroligende effekt på delirøse patienter, som er agiterede eller forpint af eksempelvis hallucinationer og vrangforestillinger. Ved at lindre denne uro, kan pleje og behandling af den/de underliggende årsag(er) udføres. I de tilfælde hvor behandling med antipsykotika overvejes, vil der være tale om alvorlige symptomer, og behandling af disse vil opveje risici og eventuelle bivirkninger.
Fokuseret Spørgsmål
Population: Patienter over 65 år med delirium uden aktuel antipsykotisk behandling.
Intervention: Behandling med antipsykotika (1. og 2. generation), fx haloperidol, olanzapin, risperidon og quetiapin, under pågående delirøse tilstand.
Sammenligning: Ingen behandling med antipsykotika.



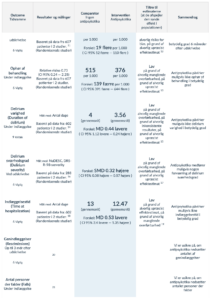
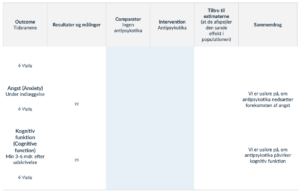
1. Opgjort som all cause mortality
2. Systematisk oversigtsartikel [86] med inkluderede studier: Agar 2017, Devlin 2010, Tahir 2010. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
3. Risiko for bias: Meget alvorligt. Afsluttet før tid grundet god effekt, Inkomplette data/eller Stort frafald. Inkonsistente resultater: Alvorligt. type 1 fejl, . Manglende overførbarhed: Ingen betydelig. Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Alvorligt. Brede konfidensintervaller. Publikationsbias: Ingen betydelig.
4. Systematisk oversigtsartikel [87] med inkluderede studier: Girard 2018. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
5. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Meget alvorligt. Kun data fra ét studie, Brede konfidensintervaller. Publikationsbias: Ingen betydelig.
6. Systematisk oversigtsartikel [86] med inkluderede studier: Agar 2017. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
7. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Forskelle mellem målpopulation og studiepopulation, Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Alvorligt. Kun data fra ét studie. Publikationsbias: Ingen betydelig.
8. Risk ratio
9. Systematisk oversigtsartikel [86] med inkluderede studier: Girard 2018, Tahir 2010. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
10. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Meget alvorligt. Brede konfidensintervaller, Få patienter (<100) /(100-300) inkluderet i studiene. Publikationsbias: Ingen betydelig.
11. Systematisk oversigtsartikel [86] med inkluderede studier: Girard 2018, Tahir 2010. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
12. Risiko for bias: Alvorligt. Selektiv rapportering af outcome, har forskellig tal på død. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Ingen betydelig. Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Alvorligt. Kun data fra ét studie. Publikationsbias: Ingen betydelig.
13. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Forskelle mellem målpopulation og studiepopulation. Upræcist effektestimat: Alvorligt. Brede konfidensintervaller. Publikationsbias: Ingen betydelig.
14. Systematisk oversigtsartikel [86] med inkluderede studier: Girard 2018, Devlin 2010. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
15. Inkonsistente resultater: Alvorligt. Konfidenintervallerne i de inkluderede studier overlapper ikke. Manglende overførbarhed: Alvorligt. Forskelle mellem målpopulation og studiepopulation, Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Alvorligt. Brede konfidensintervaller; arbejdsgruppen har valgt ikke at nedgradere for upræcist effekt estimat, da der allerede er nedgraderet for inkonsistente resultater. Publikationsbias: Ingen betydelig.
16. Systematisk oversigtsartikel [86] med inkluderede studier: Tahir 2010, Agar 2017 A, Agar 2017. Baselinerisiko/ komparator: Kontrolarm i reference brugt til interventionen.
17. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Forskelle mellem målpopulation og studiepopulation, Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Alvorligt. Brede konfidensintervaller. Publikationsbias: Ingen betydelig.
18. Systematisk oversigtsartikel [86] med inkluderede studier: Girard 2018, Devlin 2010. Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
19. Inkonsistente resultater: Ingen betydelig. Manglende overførbarhed: Alvorligt. Forskelle mellem målpopulation og studiepopulation, Der ved behov givet haloperidol og benzodizepiner i både interventionsgrupperne og placebogruppen. Upræcist effektestimat: Alvorligt. Brede konfidensintervaller. Publikationsbias: Ingen betydelig.
20. Systematisk oversigtsartikel [86] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
21. Systematisk oversigtsartikel [86] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
22. Systematisk oversigtsartikel [86] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
23. Systematisk oversigtsartikel [86] . Baselinerisiko/komparator: Kontrolarm i reference brugt til interventionen.
Referencer
3. Agar MR, Lawlor PG, Quinn S, Draper B, Caplan GA, Rowett D, et al. : Efficacy of Oral Risperidone, Haloperidol, or Placebo for Symptoms of Delirium Among Patients in Palliative Care: A Randomized Clinical Trial. JAMA Internal Medicine 2017;177(1):34-42
13. Burry L., Hutton B., Williamson D.R., Mehta S., Adhikari N.K.J., Cheng W., et al. : Pharmacological interventions for the treatment of delirium in critically ill adults. Cochrane Database of Systematic Reviews 2019;2019(9):CD011749 Journal
14. Burry L., Mehta S., Perreault M.M., Luxenberg J.S., Siddiqi N., Hutton B., et al. : Antipsychotics for treatment of delirium in hospitalised non-ICU patients. Cochrane Database of Systematic Reviews 2018;2018(6):CD005594 Journal
24. Devlin JW, Roberts RJ, Fong JJ, Skrobik Y., Riker RR, Hill NS, et al. : Efficacy and safety of quetiapine in critically ill patients with delirium: a prospective, multicenter, randomized, double-blind, placebo-controlled pilot study. Critical Care Medicine 2010;38(2):419-427 Journal
30. Girard TD, Exline MC, Carson SS, Hough CL, Rock P, Gong MN, et al. : Haloperidol and Ziprasidone for Treatment of Delirium in Critical Illness. New England Journal of Medicine 2018;379(26):2506-2516
65. Sundhedsloven : Lovbekendtgørelse LBK nr 903 af 26/08/2019. Sundheds- og Ældreministeriet, 2019. Link
67. Tahir TA, Eeles E., Karapareddy V., Muthuvelu P., Chapple S., Phillips B., et al. : A randomized controlled trial of quetiapine versus placebo in the treatment of delirium. Journal of psychosomatic research 2010;69(5):485-490 Journal
70. Vejledning om behandling med antipsykotiske lægemidler til personer over 18 år med psykotiske lidelser : VEJ nr 9276 af 06/05/2014. Sundheds- og Ældreministeriet, 2014. Link
87. NKR opdt. delir PICO 7 Behandling af delir med antiopsykotika.
Behandling med benzodiazepin og benzodiazepin-lignende stoffer (2016)
Brug af benzodiazepin og benzodiazepinlignende midler formodes udbredt i behandling af delirium med det mål at berolige agiterede delirøse patienter. Der er dog kendte skadevirkninger ved brugen af disse midler.

Nøgleinformationer

Rationale
Der er ikke fundet brugbar evidens på området. Da nogle patienter kan være urolige og angste, kan benzodiazepin og benzodiazepinlignende stoffer have en plads i behandlingen her. Grundet mulige skadevirkninger, bør der udvises forsigtighed ved ordination. Interventionen vurderes at være præferencefølsom.
Fokuseret Spørgsmål
Population: Patienter over 65 år med delirium
Intervention: Behandling med benzodiazepin eller benzodiazepin-lignende midler (BZ1-receptorligander) under pågående delirium
Sammenligning: Ingen behandling med benzodiazepin eller benzodiazepin-lignende midler

Behandling med melatonin (2016)
Melatonin er et naturligt forekommende hormon udskilt fra corpus pineale og menes at regulere den circadiane rytme (4). Behandling med melatonin-agonister bruges ofte til regulering af døgnrytme ifm. jetlag og indsovningsbesvær. Det er kun beskrevet få og ikkealvorlige bivirkninger (68).
Et studie har undersøgt urinmetabolitter af melatonin hos delirøse patienter både i akut fase samt efterfølgende, og mener at vise en sammenhæng mellem for højt eller for lavt naturligt forekommende melatoninniveau hos henholdsvis hypo- og hyperaktive delirøse patienter (8). Flere studier har udpeget mulig sammenhæng mellem ændringer i plasma-melatonin og deliriumudvikling (17) (72).
Arbejdsgruppen ønskede at undersøge evidensen for effekt af behandling med melatonin-agonister på patienter med delirium.
Nøgleinformationer

Rationale
Der er ikke fundet brugbare studier til at formulere en evidensbaseret anbefaling for melatoninbehandling af delirøse patienter. Effekten er ikke dokumenteret, ej heller på forebyggende behandling for delirium (62).
Fokuseret Spørgsmål
Population: Patienter over 65 år med delirium på hospitaler og plejehjem
Intervention: Behandling med tablet melatonin om aftenen
Sammenligning: Ingen behandling med melatonin


Referencer
4. Al-Aama T., Brymer C., Gutmanis I., Woolmore-Goodwin SM, Esbaugh J., Dasgupta M. : Melatonin decreases delirium in elderly patients: a randomized, placebo-controlled trial. International journal of geriatric psychiatry 2011;26(7):687-694 Journal
8. Balan S., Leibovitz A., Zila SO, Ruth M., Chana W., Yassica B., et al. : The relation between the clinical subtypes of delirium and the urinary level of 6-SMT. The Journal of neuropsychiatry and clinical neurosciences 2003;15(3):363-366 Journal
17. Chakraborti D., Tampi DJ, Tampi RR : Melatonin and melatonin agonist for delirium in the elderly patients. American Journal of Alzheimer’s Disease and Other Dementias 2015;30(2):119-129 Journal
62. Siddiqi N, Harrison JK, Clegg A, Teale EA, Young J, Taylor J, et al. : Interventions for preventing delirium in hospitalised non-ICU patients. The Cochrane database of systematic reviews 2016;3 CD005563
68. Tsuda A., Nishimura K., Naganawa E., Otsubo T., Ishigooka J. : Ramelteon for the treatment of delirium in elderly patients: a consecutive case series study. International journal of psychiatry in medicine 2014;47(2):97-104 Journal
72. Walker CK, Gales MA : Melatonin Receptor Agonists for Delirium Prevention. The Annals of Pharmacotherapy 2016;
Behandling med elektro-konvulsiv terapi (ECT) (2016)
I Danmark anvendes undtagelsesvist ECT af protraherede refraktære delirøse tilstande (26)(25)(40)(56)(64). Behandling med ECT betragtes som en rimelig sikker behandlingsform hos ældre patienter grundet få bivirkninger i forhold til farmakologisk behandling med antipsykotika (39).
Arbejdsgruppen ønskede at undersøge evidensen for ECT-behandling af svære refraktære delirium-tilfælde.

Nøgleinformationer

Rationale
Der blev i formuleringen af anbefalingen lagt vægt på, at ECT kan være en mulighed i svære tilfælde af behandlingsrefraktært delirium, når alle udløsende årsager er grundigt udredt og behandlet samt andre øvrige non-farmakologiske og farmakologiske behandlingsmuligheder er udtømte. Risikoen ved at lægge en svært syg patient i fuld anæstesi må opvejes mod følgerne af pågående delirium. ECT bør kun foretages efter vurdering af psykiatrisk specialist. Der er ikke fundet brugbar evidens på området, men klinisk erfaring tyder på, at der kan være en effekt på akut delirøse tilstande (26).
Implementering
Regionerne og regionernes sygehuse spiller en vigtig rolle i at understøtte implementeringen af den nationale kliniske retningslinje gennem formidling af retningslinjens indhold og ved at understøtte retningslinjens anvendelse i praksis. For at understøtte retningslinjens anvendelse lokalt er det hensigtsmæssigt, at den nationale kliniske retningslinje samstemmes med eller integreres i de forløbsbeskrivelser, instrukser og vejledninger, som allerede anvendes her. Regionerne bør således sikre, at de anbefalinger, som må være relevante for specialiserede afdelinger på sygehusniveau, indarbejdes i instrukser og vejledninger i den pågældende region. Herudover kan der med fordel indsættes et link til den nationale kliniske retningslinje i lægehåndbogen. Regionernes praksiskonsulenter kan desuden have en rolle i at tage stilling til den konkrete implementering.
De faglige selskaber er en vigtig aktør i at udbrede kendskabet til retningslinjen. Sundhedsstyrelsen foreslår således, at den nationale kliniske retningslinje omtales på de relevante faglige selskabers hjemmeside, evt. med orientering om, hvad den indebærer for det pågældende speciale og med et link til den fulde version af retningslinjen. Her tænkes særligt på Dansk Psykiatrisk Selskab, Dansk Selskab for Geriatri, Dansk Selskab for Farmakoepidemiologi, Dansk Selskab for Intensiv Terapi og Medicin, Dansk Selskab for Apopleksi og Dansk Sygepleje Selskab. Da delirium rammer meget bredt, vil retningslinjen dog være relevant for de fleste faglige selskaber. Sundhedsstyrelsen foreslår ligeledes, at retningslinjen præsenteres på årsmøder i regi af de faglige selskaber og på lægedage. Information kan også formidles via medlemsblade og elektroniske nyhedsbreve.
Sundhedsstyrelsen foreslår desuden, at retningslinjens indhold formidles til patienterne, og at relevante patient-foreninger kan spille en rolle heri.
Implementering af national klinisk retningslinje for delirium er som udgangspunkt et regionalt ansvar. Dog ønsker Sundhedsstyrelsen at understøtte implementeringen. I foråret 2014 publicerede Sundhedsstyrelsen således en værktøjskasse med konkrete redskaber til implementering. Den er tilgængelig som et elektronisk opslagsværk på Sundhedsstyrelsens hjemmeside. Værktøjskassen bygger på evidensen for effekten af interventioner, og den er tænkt som en hjælp til lederen eller projektlederen, der lokalt skal arbejde med implementering af forandringer af et vist omfang.
Foruden den fulde retningslinje udgives en quick guide. Quick guiden er en kort version på 1-2 A4-ark. Den gengiver alene retningslinjens anbefalinger og evt. centrale budskaber med angivelse af evidensgraduering og anbefalingens styrke.
Baggrund
Delirium er hyppigt forekommende hos akut syge og ses hos op mod halvdelen af ældre indlagte patienter (43). Særligt hos patienter indlagt på intensivafdelingen, som modtager respirator behandling, ses incidensrater op mod 80 % (9) og hos terminale patienter omkring 90% (12). På både kort og lang sigt har patienter med delirium en dårlig prognose. De har markant øget 1-års mortalitet (62%) (43), forlænget indlæggelsestid, øget forekomst af komplikationer under indlæggelsen samt funktionstab, øget plejebyrde og kognitiv dysfunktion i efterforløbet (28). Nogle patienter oplever desuden at have vedvarende delirium (31).
Delirium er en akut indsættende (timer til dage) og fluktuerende tilstand med opmærksomhedsforstyrrelse samt påvirkning af kognition eller tankemønster (6)(74). Det er ikke nødvendigt, at patienten fremstår med hallucinationer for at få diagnosen delirium. Der er ofte udtalt døgnvariation med forværring om aftenen og natten. Der skelnes mellem tre subtyper: hyperaktivt, hypoaktivt og blandet delirium. Ved den hyperaktive form kan patienten være pillende eller motorisk urolig, højtråbende, eventuelt udadreagerende samt senge-og afdelingsflygtig. I svære tilfælde er patienten til fare for sig og sin egen behandling. Ved den hypoaktive form kan patienten være sløv, somnolent, apatisk og der kan ses nedsat mimik og psykomotorisk hæmning. Den blandede form indeholder elementer af både den hypoog hyperaktive form. Diagnostisk kan særligt de overvejende hypoaktive tilstande let overses i den kliniske hverdag, hvis der ikke er en systematisk screening for delirium. Manglende erkendelse af delirium kan forsinke behandling af de udløsende årsager og øge risikoen for komplikationer og død.
De patofysiologiske årsager til udvikling af delirium er komplekse og ikke endeligt klarlagte. Dog står det helt klart, at delirium udløses af somatisk sygdom eller den behandling, der gives mod den, hvorfor udredning og behandling skal målrettes disse. Alle akutte medicinske og kirurgiske lidelser kan udløse delirium, herunder infektioner, dehydrering, elektrolyt- og syrebaseforstyrrelser. Mange typer af lægemidler øger risikoen for delirium, både enkeltvis og i kombination. Også manglende væske- og fødeindtag, sansedeficits, uhensigtsmæssige omgivelser og forstyrret døgnrytme kan disponere til udvikling af delirium. Alle mennesker kan udvikle delirium, men ældre, svækkede samt demente patienter er særligt disponerede for udvikling af delirium. Patienter med bestående hjernesygdom, eksempelvis demens, samt patienter med tidligere tilfælde af delirium er i højrisiko.
Patienterne kan opleve den delirøse tilstand som en yderst skræmmende oplevelse af at blive jagtet, bortført, være indespærret eller på anden måde i livsfare (28). Nogle patienter føler sig efterfølgende skamfulde over deres adfærd. Pårørende kan naturligvis blive forfærdede over den pludselige psykotiske og forandrede tilstand hos patienten (28).
Behandlingen af delirium rettes primært mod den/de udløsende somatiske årsag(er) samtidig med sikring af understøttende behandling. Herudover bør foretages non-farmakologisk multikomponent intervention samt symptom-behandling ved behov. Det er vigtigt at sikre tilstrækkelig væske-/fødeindtag, mobilisering, optimering af sanser (briller/ høreapparat), sikring af døgnrytme med henblik på at opnå søvn, skabe ro, genkendelighed og hyppig reorientering. Ved tilfælde af behandlingsrefraktært delirium bør behandleren nøje overveje, om alle udløsende årsager er identificeret og behandlet.
Der anvendes sederende og antipsykotiske midler med henblik på symptom lindrende behandling af patienter med delirium. Her er Haloperidol det eneste godkendte antipsykotikum. Patienter med delirium kan være yderst vanskelige at behandle, da tilstanden i sig selv kan begrænse deres sygdomsindsigt og gøre dem non-kompliante. Grundet risici for komplikationer er der store samfundsøkonomiske omkostninger ved delirium, der forlænger indlæggelsestid, øger risiko for komplikationer under indlæggelse og medfører lavere funktionsniveau efter indlæggelsen. Behandling af en patient med delirium er vurderet til at koste over 2,5 gange mere end en patient uden delirium (44). Denne nationale kliniske retningslinje giver evidensbaserede anbefalinger for forebyggelse, opsporing og behandling af delirium. Retningslinjen bidrager til at understøtte korrekt og tidlig diagnostik af delirium med henblik på at sikre relevant behandling, hvilket skal medvirke til at højne standarden i håndteringen af organisk delirium og begrænse antal nye tilfælde af delirium og komplikationer hertil.
Monitorering
Proces- og effektindikatorer
Der findes aktuelt ikke egnede proces-indikatorer for delirium. Såfremt screening implementeres, kan data for dette opgøres. Ligeledes vil audit af journaler kunne være brugbart lokalt for at vurdere om anbefalingerne i retningslinjen bruges i praksis.
Datakilder
For at vurdere effekten af retningslinjens implementering kan data fra landspatientregistret samkøres med ICD-kodning for delirium. Det anbefales, at man ved opdatering af denne retningslinje vurderer, om der findes egnet data, der kan bruges som indikatorer.
Patientcases
Patientcase 1: Delirium case
En 67-årig mand, kendt med malign hæmatologisk sygdom, overflyttes til intensiv afdeling på grund af neutropen septisk shock. Man påbegynder bredspektret antibiotikabehandling, væskeresuscitation og noradrenalininfusion til blodtrykskontrol. Tilstanden stabiliseres, men patienten udvikler i løbet af de næste dage symptomer på delirium, der bl.a. omfatter skræmmende hallucinationer i form af tilstedeværelse af vilde dyr og onde mennesker på stuen.
Man starter på den baggrund behandling med haloperidol, 2,5 mg x 3. Efter et par dage har patienten fortsat delirium med hallucinationer, men er nu komfortabel, idet de vilde dyr er erstattet af en venlig Golden Retriever hund, der befinder sig i sengen, og de onde mennesker er nu venlige og omsorgsfulde.
Efter infektionskontrol normaliseres tilstanden.
Casen belyser, at antipsykotika kan fremkalde en såkaldt uspecifik dæmpning, dvs. at patienten bliver indifferent over for ydre stresspåvirkninger og indre ubehagelige impulser, der i dette tilfælde ændrer karakter men fortsat opfylder kriterierne for delirium. Samtidig vil der ofte også indtræde en dæmpning af emotionalitet og af spontan aktivitet og initiativ.
Patientcase 2: Delirium case fra ortopædkirurgisk afdeling
En 72-årig kvinde indlægges på ortopædkirurgisk afdeling med kompliceret brud i overarmen. Patienten behandles med et midlertidigt ekstern fixations-apparatur, indtil hun kan opereres. Patienten ligger på tosengsstue men er størstedelen af tiden alene på stuen. I en aftenvagt opleves patienten med enkelte kortvarige episoder med hallucinationer. Hun korrigeres og sufficient smertebehandling sikres. Patienten ligger alene på tosengsstue og kan derfor skærmes.
Senere i indlæggelsesforløbet udvikler patienten i en aftenvagt igen hallucinationer. Hun har oplevelser af, at der ligger søm og andre spidse genstande i sengen – hun forklares, at det nok er hendes eksterne apparatur. Hun ligger fortsat alene på stuen, og der spørges ind til smerter, da hun er i fast smertebehandling. Patienten skærmes yderligere, med markering ved indgang til stuen og korrigeres verbalt i vagten.
Senere findes patienten siddende i en stor blodpøl. Hun har fjernet det eksterne apparatur fra overarmen og opleves meget delirøs. Patienten kan ikke korrigeres og har ikke en forståelse af, hvad der er sket, men kan angive tid, sted og egne data. Patienten smertebehandles, og der opstartes behandling med haloperidol. Patienten falder efterfølgende til ro.
Patientcase 3: Delirium case fra ortopædkirurgisk afdeling
En 87-årig kvinde indlægges med acetabulum fraktur. Hun er kendt med begyndende demens. Patienten indlægges på enestue og screenes for delirium 2 gange i døgnet ved hjælp af CAM.
Patienten er sengeliggende med stræk på benet – dvs. hun kan kun ligge på ryggen, døgnet rundt frem til operationsdagen. Patienten udvikler under indlæggelsen delirium, hvilket giver sig til udtryk ved at hun bliver bange og mistroisk, og ikke kan korrigeres i tid, sted og egne data. Patienten skærmes på enestuen, med markering indtil stuen, der fokuseres på smertebehandling og undersøges for evt. urinvejsinfektion.
Patienten er meget mistroisk overfor personalet og ønsker at ringe til politiet. Hun er forpint af sit delirium og sover meget afbrudt om natten. Der forsøges med optimering af døgnrytmen, og der opstartes behadnling med haloperidol samt fortsættes med CAM screening 2 gange i døgnet. Den fagprofessionelle vurdering er, at patienten har kortvarig effekt af haloperidol.
Patientcase 4: Delirium case med non-farmakologisk håndtering
En 75-årig mand med KOL indlægges efter styrt på elcykel. CT-scanning af cerebrum viser lille kontusionsblødning frontalt på højre side og ganske lille traumatisk SAH parietalt på højre side. Han indlægges i neurologisk regi. Han er forslået, og har en del skrammer og costafraktur. Patienten udvikler pneumoni og delirium og overflyttes til geriatrisk sengeafsnit.
Mens patienten er delirøs, falder han men kommer ikke yderligere til skade. Han behandles med antibiotika for pneumoni, får morfin mod smerter og udvikler obstipation, hvilket behandles med laksantia. Ud over behandling af evt. disponerende årsager behandles delirium nonfarmakologisk, hvor patienten skærmes på enestue, og der anvendes deliriumblomst*. Ægtefællen kommer hyppigt på besøg. Patienten har grundet fraktur svært ved at ligge i en almindelig seng men har god effekt af hjælp fra fysioterapeut ift. lejring.
Ved udskrivelsen er patienten oppegående med aftagende smerter, intakt døgnrytme og uden forvirring men er humørmæssigt påvirket af forløbet, der også har været hårdt for ægtefællen. Han kan gå med rollator, men hans funktionsniveauet er ikke på vanligt niveau. Der er taget kontakt til hjemmepleje med henblik på hjælp i hjemmet efter udskrivelse. Opfølgende besøg ved geriatrisk team er også iværksat med fokus på delirium, smerter, obstipation, almen tilstand og hjemlige forhold.
*En figur som kan udfyldes af pårørende med information om f.eks. fødeby, tidligere arbejde, interesser, børn, forældre, kæledyr.
Patientcase 5: Palliativ patient i eget hjem
Case fra Dansk Selskab for Palliativ Medicin
En 80-årig mand tilknyttes palliativt team pga. symptomer fra en udbredt prostatacancer med spredning til knogler og lunger. Patienten har comorbiditet i form af hjerteinsufficiens, tidligere apoplexi og type 2 diabetes. Patienten bliver ligeså stille bedre smertelindret efter langsom optrapning i oxycontin. Patienten har fået en stabil opioid-dosis i nogle uger, uden at udvise tegn på uacceptable bivirkninger til opioid, da han får tiltagende forstyrret nattesøvn med livlige drømme og mareridt. Efter nogle dage med urolige nætter, så frembyder patienten delirium symptomer både dag og nat. Hjemmesygeplejen stixer urinen og finder urinvejsinfektion. Der findes ikke umiddelbart andre forklaringer på delirium end nytilkommen urinvejsinfektion. Behandling for urinvejsinfektionen iværksættes samtidig med opstart af tablet serenase 1,25 mg x 3 dagligt. Der er hyppige daglige tilsyn ved hjemmesygeplejen, og patienten forbliver i eget hjem med massiv støtte fra datter og ægtefælle. Patientens kognitive tilstand stabiliseres gradvist over nogle dage. Efter at infektionen er saneret, så er patientens delirium symptomer forsvundet. Pga. tidligere tilfælde, hvor patienten har haft let til at få delir-symptomer, så aftrappes serenase-behandlingen gradvist over 10 dage.
Senere i sygdomsforløbet bliver det nødvendigt at indlægge patienten fordi der kommer en ny episode med delir, hvor patienten bliver så svækket alment at der er faldtendens, og hjemmesituationen dermed bliver uholdbar. Under indlæggelsen får patienten saneret en luftvejsinfektion infektion, bliver rehydreret og sættes i fast behandling med tbl. serenase 2,5 mg x 3. Patienten overflyttes herefter til kommunal aflastningsplads i en periode, mens almentilstanden bedres, og delirium behandlingen nedtrappes over to uger.
Patientcase 6: Indlagt terminal patient
Case fra Dansk Selskab for Palliativ Medicin
50-årig mand med diss. coloncancer med levertastaser diagnostiseret for 5 år siden, er tilknyttet palliativt team mhp. lindring af symptomer. Det har været et stabilt forløb med kræftsygdom, men nu er situationen præget af gentagne langvarige indlæggelser pga. fistulering fra galdeveje til pleurahule og komplikationer til dette. Patienten er plaget af åndenød som forværres af en massiv døds angst, i forbindelse med lufthunger ved dyspnøanfald. Patienten har ændret sig personlighedsmæssigt for 7-8 uger siden og beskrives ”kortluntet og uden filter” og taler i ”underlige billeder”. Patienten tør heller ikke falde i søvn i sin seng til natten fordi han er bange for ikke at vågne igen. Han indlægges til symptomlindrende ophold på hospice for at få styr på angst symptomer, som er behandlet i hjemmet med en kombination af benzodiazepin, pregabalin og olanzapin til nat. Ved ankomst til hospice øges pregabalin til 75 mg x 3, og olanzapin øges til 10 mg nocte, og der gives benzodiazepin pn i form af inj. midazolam 5 mg subcutant. Patientens vanlige smertelindrende medicin øges til oxycontin 40 mg x 2. Patienten er initialt godt lindret mht angst, dyspnø og smerter, men bliver tiltagende respiratorisk dårlig efter nogle dage. Tilstanden tolkes som pneumoni, og behandles med antibiotika, og patienten forbliver på hospice. Da infektionen starter bliver patient delirøs og oplever en forværring af vrangforstillinger, hallucinationer og dødsangst. Medicineringen ændres til inj. olanzapin 20 mg subcutant nocte, og der suppleres med inj. midazolam 5 mg sc, hver 6. time for at lindre den motoriske uro. Efter et døgn er der fortsat ikke tilstrækkelig symptomkontrol og patienten lindres yderligere ved at tillægge inj. oxynorm 10 mg sc. hver 4. time sammen med inj. midazolam 5 mg sc hver 4. time, der fortsættes uændret med inj. olanzapin 20 mg sc. nocte. Herved opnås nogenlunde symptomkontrol over delirium, smerter og motorisk uro. Patienten retter sig ikke klinisk og går ad mortem efter to døgn på ovenstående behandling.
Opdatering og videre forskning
Opdatering
Som udgangspunkt bør retningslinjen opdateres 3 år efter udgivelsesdato, medmindre ny evidens eller den teknologiske udvikling på området tilsiger andet.
Ved gennemsyn af litteraturen er der fundet store mængder af studier og forsøg foretaget på forskellige patientgrupper med risiko for delirium. I en opdateret udgave af denne retningslinje kunne populationsdefinitionen af flere PICO-spørgsmål udvides således at evidensen for behandling af disse risikogrupper belyses.
Der er i høringssvar på 2021-udvidelsen fremsendt ønske om opdatering af anbefalingerne vedrørende systematisk screening og nonfarmakologiske interventioner, herunder brug af skærmning og enestuer. Der efterspørges desuden en opdeling af populationen, således at terminale patienter behandles som en subgruppe i retningslinjen og at der skelnes mellem hospitalsindlagte og ikke-hospitalsindlagte patienter.
Videre forskning
Denne retningslinje har påvist flere områder med manglende eller sparsom evidens. Særligt kunne effekten af systematisk screening og tidlig opsporing af deliriumtilfælde være interessant, herunder inklusion af screeningsværktøjet 4AT. Herudover mangler der også evidens på de nævnte typer af både farmakologisk og non-farmakologisk behandling af patienter med delirium. Der efterspørges også viden om effekten af skærmede omgivelser ved hospitalsindlæggelse.
Det anbefales, at fremtidige undersøgelser inddrager patientrelevante outcomes såsom sværhedsgraden af delirium og kognitiv funktion i efterforløbet. Ligeledes kunne fremtidig forskning om antipsykotika med fordel vurderere effekten på patienters forpinthed og uro fremfor tilstedeværeslen af delirium, da antipsykotikas ønskede effekt er at skabe komfort hos patienten med delirium.
Arbejdsgruppen foreslår at der kan oprettes et fagligt selskab/interesseselskab for delirium, der bl.a. kan skabe overblik over igangværende forskning og bidrage til udbredelse af ny viden på området.
Beskrivelse af anvendt metode
Den anvendte graduering af evidensens kvalitet og anbefalingsstyrke baserer sig på GRADE (Grading of Recommendations Assessment, Development and Evaluation). Se også: http://www.gradeworkinggroup.org.
Sundhedsstyrelsen har udarbejdet en metodehåndbog for nationale kliniske retningslinjer. Metodehåndbogen indeholder en beskrivelse af den metodiske tilgang og processen for udarbejdelse af evidensbaserede nationale kliniske retningslinjer. Metodehåndbogen kan tilgås her.
Fokuserede spørgsmål
Dette afsnit indeholder en oversigt over de fokuserede spørgsmål for denne nationale kliniske retningslinje.
PICO 1: Bør alle akut syge nyindlagte patienter over 65 år screenes med psykometrisk værktøj (b-CAM eller CAM?)
Baggrund for valg af spørgsmål:
Ældre patienter med akut sygdom er i risiko for at udvikle delirium (herefter kaldet delir i teksten). Delir kan vise sig i flere former, herunder hyperaktive, hypoaktive og blandede former. Særligt de hypoaktive kan overses i den kliniske hverdag, og gives derfor ikke nødvendigvis samme behandling og pleje som de øvrige delir-patienter.
Population: Akut indlagte (på hospital eller plejeafsnit i primær sektor) patienter over 65 år. Ekskl. intensiv patienter, palliative patienter.
Intervention: Screening med b-CAM eller CAM.
Comparison (sammenligning): Ingen screening med b-CAM eller CAM.

PICO 2: Bør patienter med risiko for delir have multikomponent non-farmakologisk behandling?
Baggrund for valg af spørgsmål:
Ved delir optræder flere problemstillinger for patienterne, herunder forstyrret døgnrytme med søvn/hvile om dagen og uro/aktivitet om natten, problemer med at orientere sig som kan udvikle sig til vrangforestillinger, nedsat føde/væske indtag og immobilisering. Desuden har denne patientgruppe ofte svækkede sanser, her tænkes særligt på syn og hørelse, hvilket yderligere kan bidrage til forvirring. I plejen af risiko-patienter kan derfor fokuseres på nedenstående interventioner for at undgå delir.
Population: Akut indlagte (på hospital eller plejeafsnit i primær sektor) patienter over 65 år med somatisk sygdom samt mindst en af nedenstående risikofaktorer:
- Demens
- Mb. Parkinson
- Tidligere apopleksi
- Tidligere delir
- Lav funktionsevne**
- 2 eller flere kroniske sygdomme.
Intervention: Multikomponent non-farmakologisk intervention som indeholder to eller flere af følgende:
- Skemalagt fysisk aktivitet***: Flere gange dagligt fx i forbindelse med måltider og pleje.
- Sanseoptimering: Briller, høreapparat, lys på stuen
- Re-orientering: Information om tid, sted og egne data
- Ernæring: Sikre nødvendigt væske/føde indtag
- Struktureret døgnrytme: Fokus på at patient er vågen om dagen samt pleje, undersøgelser mm. i videst muligt omfang foregår i dagtid, og der er ro og mørke på stuen om natten.
Comparison (sammenligning): Treatment as usual.

PICO 3: Bør patienter med delir have multikomp onent non farmakologisk intervention?
Baggrund for valg af spørgsmål:
Ved delir optræder flere problemstillinger for patienterne, herunder forstyrret døgnrytme med søvn/hvile om dagen og uro/aktivitet om natten, problemer med at orientere sig som kan udvikle sig til vrangforestillinger, nedsat føde/væske indtag og immobilisering. Desuden har denne patientgruppe ofte svækkede sanser, her tænkes særligt på syn og hørelse, hvilket yderligere kan bidrage til forvirring.
Population: Patienter over 65 år med delir, inkl. intensiv patienter, patienter i primær sektor.
Intervention: Multikomponent non-farmakologisk intervention som indeholder to eller flere af følgende:
- Skemalagt fysisk aktivitet***: Flere gange dagligt fx i forbindelse med måltider og pleje.
- Sanseoptimering: Briller, høreapparat, lys på stuen
- Re-orientering: Information om tid, sted og egne data
- Ernæring: Sikre nødvendigt væske/føde indtag
- Struktureret døgnrytme: Fokus på at patient er vågen om dagen samt pleje, undersøgelser mm. i videst muligt omfang foregår i dagtid, og der er ro og mørke på stuen om natten.
Comparison (sammenligning): Treatment as usual.
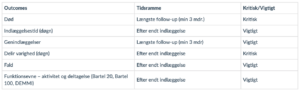
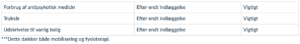
PICO 4: Bør patienter med deli r have skærmede omgivelser?
Baggrund for valg af spørgsmål:
På en hospitalsafdeling kan der være uro/støj hele døgnet ifm. pleje og behandling af patienter og medpatienter, særligt på gangpladser og flersengsstuer. Dette kan forstyrre døgnrytmen og muligvis medvirke til udvikling og/eller forværring af delir.
Population: Indlagte patienter over 65 år med delir.
Intervention: Afskærmning mod uvedkommende forstyrrende stimuli, fx enestue, sovemaske, ørepropper.
Comparison (sammenligning): Ingen afskærmning og flersengsstue eller gangplads, flytning til anden sengestue.

PICO 5: Bør pårørende aktivt inddrages i behandling af patienter med delir?
Baggrund for valg af spørgsmål:
Idet delir giver en forvirringstilstand, kan pårørende inddrages således patientens dagligdag og rutiner bibeholdes bedst muligt samt der er kendte ansigter omkring patienten, som kan styrke reorientering.
Population: Patienter over 65 år med delir.
Intervention: Aktiv inddragelse af pårørende (fx inddragelse i daglige aktiviteter og gøremål, overnatningsmulighed).
Comparison (sammenligning): Treatment as usual.


PICO 6: Bør patienter med delir få pauseret ikke livsvigtig medicin?
Baggrund for valg af spørgsmål:
Mange forskellige almindelig brugte farmaka kan medvirke til udvikling af delir. Polyfarmaci er ligeledes en risikofaktor.
Population: Indlagte patienter over 65 år med delir.
Intervention: Medicinstatus og gennemgang med pausering (indtil endt delir) af medicin, som kan forværre patientens tilstand.
Comparison (sammenligning): Ingen pausering af patientens medicin.

PICO 7: Bør patienter med delirium behandles med antipsykotika?
Baggrund for valg af spørgsmål i 2016
Patienter med delirium fremstår ofte psykotiske og kan være apatiske og/eller udadreagerende. I behandling af delirøse patienter gives ofte antipsykotika for at mindske disse symptomer og give patienten ro og søvn.
Baggrund for valg af spørgsmål til opdatering i 2020
Patienter med delirium fremstår ofte psykotiske, urolige, apatiske og/eller udadreagerende. I behandling af delirøse patienter gives ofte antipsykotika for at mindske disse symptomer. Der er de senere år kommet flere metaanalyser og systematiske reviews, der beskriver patientrelaterede outcomes og sikkerhed af behandling med antipsykotisk medicin og det er usikkert om den gavnlige effekt opvejer de potentielt skadelige.
Årsag til delirium er som hovedregel somatisk sygdom og/eller medicinbivirkninger. Behandlingen af den/de udløsende årsager skal iværksættes før eller samtidig med start af antipsykotisk behandling. Den juridiske vejledning om behandling med antipsykotiske lægemidler til personer over 18 år med psykotiske lidelser er rammesættende for behandlingen.
Population: Patienter over 65 år med organisk delirium uden aktuel antipsykotisk behandling, hvor evt. udløsende årsag til delirium behandles og non-farmakologisk behandling af delirium ikke er tilstrækkelig. Delirøse tilstande i relation til psykiske sygdomme eller tilstande som er forårsaget af misbrug og abstinenser er ikke inkluderet, da disse tilstande er af anden genese og behandles anderledes end organisk delirium, der udløses af fysisk sygdom eller påvirkning.
Intervention: Behandling med antipsykotika (1. og 2. generation), fx haloperidol, olanzapin, risperidon og quetiapin, under pågående delirøse tilstand.
Comparison (sammenligning): Ingen behandling med antipsykotika. Eventuelt foretages subgruppeanalyser for at se om effekten afhænger af dosis eller antal timer under behandling.

PICO 8: Bør patienter med delir behandles med benzodiazepin eller benzodiazepin-lignende midler?
Baggrund for valg af spørgsmål:
Patienter med delir har ofte forstyrrelser i søvnen med gentagne opvågninger om natten, inverteret søvnrytme eller bortfald af den normale circadiane rytme. Ofte ses forværring af delir-symptomerne om natten.
Population: Patienter over 65 år med delir.
Intervention: Behandling med benzodiazepin eller benzodiazepin-lignende midler (BZ1-receptorligander) under pågående delir.
Comparison (sammenligning): Ingen behandling med benzodiazepin eller benzodiazepin-lignende midler.
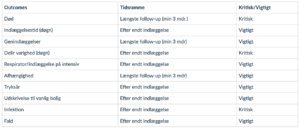
PICO 9: Bør patienter med delir behandles med melatonin?
Baggrund for valg af spørgsmål:
Patienter med delir har ofte forstyrrelser i søvnen med gentagne opvågninger om natten, inverteret søvnrytme eller bortfald af den normale circadiane rytme. Ofte er der forværring af delir-symptomerne om natten. Melatonin dannes i kroppen i aften/nattetimer og menes at regulere søvn/vågen-rytmen.
Population: Patienter over 65 år med delir på hospitaler og plejehjem
Intervention: Behandling med tablet melatonin om aftenen.
Comparison (sammenligning): Ingen behandling med melatonin.

PICO 10: Bør patienter med behandlingsrefraktært delir behandles med ECT?
Baggrund for valg af spørgsmål:
Delirium acutum betragtes som en livstruende tilstand med søvn-, drikke- og spisevægring, forhøjet puls, blodtryk og legemstemperatur, samt elektrolytforstyrrelser og dehydrering.
Population: Indlagte patienter over 65 år med behandlingsrefraktært**** delir i min. 3 døgn.
Intervention: Behandling med ECT.
Comparison (sammenligning): Ingen ECT-behandling

Beskrivelse af anbefalingernes styrke og implikationer
Formulering af evidensbaserede anbefalinger:
En anbefaling kan enten være for eller imod en given intervention. En anbefaling kan enten være stærk eller svag/betinget. Ved evidens vælges en af følgende fire typer af anbefalinger
![]()
Der gives en stærk anbefaling for, når der er pålidelig evidens, der viser, at de samlede fordele ved interventionen er klart større end ulemperne.
Det er klart, at fordelene opvejer ulemperne. Det betyder, at alle, eller næsten alle, patienter vil ønske den anbefalede intervention.
Ordlyd: Giv/brug/anvend…
Følgende vil trække i retning af en stærk anbefaling for:
Høj eller moderat tiltro til de estimerede effekter.
Stor gavnlig effekt og ingen eller få skadevirkninger.
Patienternes værdier og præferencer er velkendte og ensartede til fordel for interventionen.
Implikationer:
De fleste patienter vurderes at ønske interventionen.
Langt de fleste klinikere vil tilbyde interventionen.
![]()
Der gives en stærk anbefaling imod, når der er høj tiltro til, at de samlede ulemper er klart større end fordelene. Det samme gælder, hvis der er stor tiltro til, at en intervention er nyttesløs.
Ordlyd: Giv ikke/brug ikke/anvend ikke/undlad at…
Følgende vil trække i retning af en stærk anbefaling imod:
Høj eller moderat tiltro til de estimerede effekter.
Der er stor tiltro til, at interventionen ikke gavner, eller at den gavnlige effekt er lille.
Der er stor tiltro til, at interventionen har betydelige skadevirkninger.
Patienternes værdier og præferencer er velkendte og ensartede imod interventionen.
Implikationer: De fleste patienter vurderes ikke at ville ønske interventionen.
Klinikeren vil meget sjældent tilbyde interventionen.
![]()
Der gives en svag anbefaling for interventionen, når det vurderes, at fordelene ved interventionen er marginalt større end ulemperne, eller den tilgængelige evidens ikke kan udelukke en væsentlig fordel ved en eksisterende praksis, samtidig med at skadevirkningerne er få eller fraværende. Der er større mulighed for variation i individuelle præferencer.
Ordlyd: Overvej at…
Følgende vil trække i retning af en svag anbefaling for:
Lav eller meget lav tiltro til de estimerede effekter.
Balancen mellem gavnlige og skadelige virkninger ikke er entydig.
Patienternes præferencer og værdier vurderes at variere væsentligt, eller de er ukendte.
Implikationer: De fleste patienter vurderes at ønske interventionen, men nogen vil afstå.
Klinikeren vil skulle bistå patienten med at træffe en beslutning, der passer til patientens værdier og præferencer.
![]()
Der gives en svag anbefaling imod interventionen, når ulemperne ved interventionen vurderes at være større end fordelene, men hvor man ikke har høj tiltro til de estimerede effekter. Den svage anbefaling imod anvendes også, hvor der er stærk evidens for både gavnlige og skadelige virkninger, men hvor balancen mellem dem er vanskelig at afgøre.
Ordlyd: Anvend kun … efter nøje overvejelse, da den gavnlige effekt er usikker og/eller lille, og der er dokumenterede skadevirkninger såsom…
Følgende vil trække i retning af en svag anbefaling imod:
Lav eller meget lav tiltro til de estimerede effekter. Balancen mellem gavnlige og skadelige virkninger ikke er entydig.
Skadevirkningerne vurderes at være marginalt større end den gavnlige effekt.
Patienternes præferencer og værdier vurderes at variere væsentligt, eller de er ukendte.
Implikationer:
De fleste patienter vurderes at ville afstå fra interventionen, men nogen vil ønske den. Klinikeren vil skulle bistå patienten med at træffe en beslutning, der passer til patientens værdier og præferencer.
Formulering af anbefaling ved mangel på evidens:
![]()
God praksis anvendes, når der ikke foreligger relevant evidens og bygger således udelukkende på faglig konsensus blandt medlemmerne af arbejdsgruppen. Anbefalingen kan være enten for eller imod interventionen. Da der udelukkende er tale om faglig konsensus, er denne type anbefaling svagere end de evidensbaserede anbefalinger, uanset om de evidensbaseret er stærke eller svage.
De to typer af anbefalinger til god praksis anbefalinger
Ordlyd:
For:
Det er god praksis at overveje….
Imod:
Det er ikke god praksis rutinemæssigt at…
Søgebeskrivelser
SØGEBESKRIVELSE FOR OPDATEREDE PICO 7 (2015-2020)
Litteratursøgning til denne kliniske retningslinje er foretaget i henhold til Metodehåndbogen for udarbejdelse af nationale kliniske retningslinjer. Databaserne er udvalgt til søgning efter nationale kliniske retningslinjer som defineret i Metodehåndbogen.
Der er foretaget tre systematiske søgninger:
- en søgning efter kliniske retningslinjer, guidelines og Cochrane Reviews fra 2015 til og med januar 2020;
- en opfølgende søgning efter sekundærlitteratur fra 2016 til juli 2020
- en opfølgende søgning efter supplerende primærlitteratur fra 2017 til august 2020.
Søgningerne er foretaget ved søgespecialist Birgitte Holm Petersen og søgespecialist Kirsten Birkefoss i samarbejde med fagkonsulent Marie Oxenbøll Collet.
Søgeprotokollerne med søgestrategier for de enkelte databaser er tilgængelige på Sundhedsstyrelsens hjemmeside.
Generelle søgetermer
Engelske: Delirium, acute confusion
Danske: Delirium, delir, konfusion
Norske: Delirium, delir, konfusjon, akutt forvirring, forvirringstilstand
Svenske: Delirium, konfusion, akut förvirring, förvirringstillstånd
For den opfølgende søgning er der søgt med individuelle søgetermer for hvert PICO-spørgsmål. Se søgeprotokoller for de opfølgende søgninger på Sundhedsstyrelsens hjemmeside for denne guideline.
Generelle søgekriterier
Publikationsår: 2015 – august 2020
Sprog: Engelsk, dansk, norsk og svensk
Dokumenttyper: Guidelines, clinical guidelines, practical guidelines, MTV, Cochrane Reviews, randomiserede studier.
Guidelines søgningen
Den systematiske søgning efter kliniske retningslinjer, guidelines og MTV’er blev foretaget 16.-20. januar i følgende informationskilder: Guidelines International Network (G-I-N), NICE (UK), Trip Database (Intl), Scottish Intercollegiate Guidelines Network (SIGN), CRD/HTA database, SBU (Sverige), Socialstyrelsen (Sverige), Helsedirektoratet (Norge), Folkehelseinstituttet (Norge), Center for Kliniske Retningslinjer (Danmark), NHMRC (Australien), Canada Medical Association (Canada), CADTH (Canada) samt Medline, Embase og Cinahl.
De opfølgende søgninger
Der er foretaget to opfølgende søgninger, specifikt for PICO 7, først efter systematiske reviews og metaanalyser søgt 8. juli 2020 i databaserne Medline og Embase, dernæst søgt 14. august 2020 efter randomiserede studier i Medline og Embase.
Søgeprotokoller
Søgeprotokoller kan tilgås her og på Sundhedsstyrelsens hjemmeside
Flowcharts for opdaterede PICO 7 kan tilgås på Sundhedsstyrelsens hjemmeside.
SØGEBESKRIVELSE FOR PICO 1-10 (2016) Til denne kliniske retningslinje er søgningerne foretaget i en defineret gruppe databaser, der er udvalgt til søgning efter nationale kliniske retningslinjer, nærmere beskrevet i Metodehåndbogen. Der er lavet systematiske søgninger foretaget af Tove Faber Frandsen i samarbejde med fagkonsulenten Maria Bohr Dawids.
Først er der søgt internationalt på guidelines og medicinske teknologivurderinger (MTV) i følgende informationskilder: Guidelines International Network (G-I-N), NICE (UK), National Guideline Clearinghouse, Scottish Intercollegiate Guidelines Network (SIGN), HTA database (CRD database), SBU (Sverige), Socialstyrelsen (Sverige), Helsedirektoratet (Norge), Kunnskapssenteret (Norge), Netpunkt (Danmark), Medline og Embase.
Dernæst er der søgt mere specifikt med udgangspunkt i de fokuserede spørgsmål (PICOs). Her er der fremfundet sekundærlitteratur (systematiske reviews og metaanalyser). Databaser søgt er: Medline, Embase, PsycINFO, Cinahl og Cochrane Library.
Til sidst er der lavet en opdateret søgning på primærlitteratur i databaserne: Medline, Embase, PsycInfo og Cinahl. Søgningerne er foretaget i perioden 27. oktober 2015 til 8. juli 2016.
Generelle søgetermer
Engelske: Delirium, acute confusion
Danske: Delirium, delir, konfusion
Norske: Delirium, delir, konfusjon, akutt forvirring
Svenske: Delirium, konfusion, akut förvirring, förvirringstillstånd
Generelle inklusionskriterier
Publikationsår: Hele perioden til og med 2019
Sprog: Engelsk, dansk, norsk og svensk
Dokumenttyper: Guidelines, clinical guidelines, HTA, meta-analyser, systematiske reviews, RCT
Evidensvurderinger
Evidensprofiler med risiko for bias-vurderinger og meta-analyser samt beskrivelse af in- og ekskluderede studier kan tilgås via Sundhedsstyrelsens hjemmeside.
Arbejdsgruppens AMSTAR-vurderinger og AGREE-vurderinger kan ligeledes tilgås via Sundhedsstyrelsens hjemmeside.
Arbejdsgruppen og referencegruppen
Arbejdsgruppen 2020
Arbejdsgruppen vedr. opdatering af NKR for forebyggelse og behandling af organisk delirium består af følgende personer:
- Jens Nørbæk, overlæge, speciallæge i psykiatri, udpeget af Dansk Psykiatrisk Selskab
- Zoltan Barkanyi, overlæge, udpeget af Dansk Psykiatrisk Selskab
- Lise Fonsmark, overlæge, udpeget af Dansk Selskab for Anæstesiologi og Intern medicin
- Rasmus Wæhrens, Læge, udpeget af Dansk Selskab for Almen Medicin
- Michael Krasheninnikoff, overlæge, udpeget af Dansk ortopædisk selskab
- Hanne Pedersen, overlæge, udpeget af Dansk Selskab for Geriatri
- Susanne Stabel Gren, overlæge, udpeget af Dansk Selskab for Geriatri
- Tua Vinther-Jensen, Afdelingslæge, udpeget af Dansk Neurologisk Selskab
- Niels August Willer Strand, 1.Reservelæge, udpeget af Dansk Selskab for Klinisk Farmakologi
- Jakob Greve Carlsen, overlæge, udpeget af Dansk Selskab for Akutmedicin
- Helle Svenningsen, lektor, udpeget af Dansk Sygepleje Selskab
- Trine Ahlmann Pedersen, Klinisk sygepjerske, udpeget af Dansk Sygepleje Selskab
- Lars Peter Kammersgaard, overlæge, udpeget af Dansk Selskab for Apopleksi
Habilitetsforhold
En person, der virker inden for det offentlige, og som har en personlig interesse i udfaldet af en konkret sag, må ikke deltage i behandlingen af denne sag. Hvis en person er inhabil, er der risiko for, at han eller hun ikke er uvildig ved vurderingen af en sag. Der foreligger habilitetserklæringer for alle arbejdsgruppemedlemmer. Habilitetserklæringerne kan tilgås her.
Sundhedsstyrelsens sekretariat
- Marie Oxenbøll Collet, fagkonsulent
- Marie Louise Kirkegaard Mikkelsen, projektleder
- Simon Tarp, formand
- Jeanett Friis Rohde, metodekonsulent
- Kirsten Birkefoss, søgespecialist
- Birgitte Holm Petersen, søgespecialist
Peer review og offentlig høring
Den nationale kliniske retningslinje for forebyggelse og behandling af organisk delirium har forud for udgivelsen været i høring blandt følgende høringsparter:
- Danske Regioner
- Kommunernes Landsforening
- Socialstyrelsen
- Sundheds- og Ældreministeriet
- Danske Patienter
- Ældre Sagen
- Dansk Sygepleje Selskab
- Dansk Selskab for Almen Medicin
- Dansk Selskab for Geriatri
- Ergoterapeutforeningen
- Dansk Selskab for Fysioterapi
- Dansk Psykiatrisk Selskab
- Dansk Ortopædisk Selskab
- Dansk Selskab for Akutmedicin
- Dansk Selskab for Apopleksi
- Dansk Selskab for Klinisk Farmakologi
- Dansk Endokrinologisk Selskab
- Dansk Lungemedicinsk Selskab
- Dansk Selskab for Anæstesiologi og Intensiv Medicin
- Dansk Selskab for Palliativ Medicin
- DemensKoordinatorer i Danmark
- Kliniske Retningslinjers Implementering i MidtEPJ
- Center for Handicap og Psykisk Sårbarhed, Socialstyrelsen
- Janne Unkerskov, Thomas Gorlen og Anna Weibull, praktiserende læger • Janne Bække, overlæge
- Kristin Enevoldsen og Lars Henrik Jensen, overlæger
Høringssvar forefindes på Sundhedsstyrelsens hjemmeside for nationale kliniske retningslinjer
Retningslinjen er desuden i samme periode peer reviewet af:
- Bjørn Erik Neerland, overlæge, Olso Universitetssykehus
- Thomas Strøm, professor, Sygehus Sønderjylland
Arbejdsgruppen 2016
Arbejdsgruppen vedr. NKR for forebyggelse og behandling af organisk delirium består af følgende personer:
- Lars Weywadt (formand), overlæge, udpeget af Sundhedsstyrelsen
- Jens Nørbæk, overlæge, speciallæge i psykiatri, udpeget af Dansk Psykiatrisk Selskab, Liaison og tilsyn, Psykiatrisk Center Hvidovre
- Lise Fonsmark, overlæge, udpeget af Dansk Selskab for Anæstesiologi og Intern medicin
- Jakob Greve Carlsen, overlæge, udpeget af Dansk Selskab for Akutmedicin, Akutafdelingen, Holbæk Sygehus
- Anne Henckel Johansen, Ergoterapeut, udpeget af Ergoterapeutforeningen, Helsingør Rehabilitering og Træningscenter
- Hanne Pedersen, overlæge, udpeget af Dansk Selskab for Geriatri, Medicinsk Afdeling Glostrup Hospital
- Susanne Stabel Gren, overlæge, udpeget af Dansk Selskab for Geriatri, Medicinsk afdeling O, Herlev Hospital
- Michael Krasheninnikoff, overlæge, Udpeget af Dansk Ortopædisk Selskab, Hvidovre Hospital
- Helle Svenningsen, Adjunkt, MKS, ph.d., udpeget af Dansk Sygepleje Selskab, VIA Sundhed, Sygeplejerskeuddannelsen Aarhus
- Mette Friis, Sygeplejerske, udpeget af Dansk Sygepleje Selskab, Odense Kommune, Lysningen ? Birgit Villadsen, oversygeplejerske, udpeget af Dansk Sygepleje Selskab, Bispebjerg Hospital
- Anette Davidsen, speciallæge i almen medicin, udpeget af Dansk Selskab for Almen Medicin
- Yasmin Hassan Hamid, udpeget af Dansk Endokrinologisk Selskab, Bispebjerg Hospital
- Merete Almind, læge, Udpeget af Dansk Lungemedicinsk Selskab, Bispebjerg Hospital
- Kirstine Moll Harboe, læge, Udpeget af Dansk Selskab for Klinisk Farmakologi
- Karen Ægidius, overlæge, udpeget af Dansk Selskab for Apopleksi, Neurologisk Afdeling, Bispebjerg Hospital
Fagkonsulenten Maria Bohr Dawids har som en del af sekretariatet, jf. nedenfor, været overordnet ansvarlig for litteraturgennemgangen og for at udarbejde udkast til retningslinjen til drøftelse i arbejdsgruppen.
Habilitetsforhold
En person, der virker inden for det offentlige, og som har en personlig interesse i udfaldet af en konkret sag, må ikke deltage i behandlingen af denne sag. Hvis en person er inhabil, er der risiko for, at han eller hun ikke er uvildig ved vurderingen af en sag. Der foreligger habilitetserklæringer for alle arbejdsgruppemedlemmer. Habilitetserklæringerne kan tilgås her.
Referencegruppen
Referencegruppen er udpeget af regioner, kommuner, patientforeninger og andre relevante interessenter på området, og dens opgave har bestået i at kommentere på afgrænsningen af og det faglige indhold i retningslinjen.
Referencegruppen vedr. NKR for forebyggelse og behandling af organisk delirium består af følgende personer:
- Lars Weywadt (formand), overlæge, udpeget af Sundhedsstyrelsen
- Mette Lund Jespersen, 1.reservelæge, Udpeget af Region Hovedstaden, Enhed for Hospitalsplanlægning, Region Hovedstaden
- Linea Ohm Søndergaard, konsulent, udpeget af Danske Regioner
- Lisa Jakobsen, afdelingslæge, Udpeget af Region Syd, Geriatrisk Afdeling G OUH Odense Universitetshospital
- Per Fabæch Knudsen, faglig konsulent, Udpeget af Socialstyrelsen og Social- og Indenrigsministeriet
- Sophie Leth-Møller, konsulent, udpeget af KL
- Rikke Green Skaarup, konsulent, udpeget af KL
- Anne Birgitte L. Pedersen, overlæge, Udpeget af Region Midt, Medicinsk Afdeling, Medicinsk Modtageafsnit, Hospitalsenheden Vest
- Michael Lau Bech-Hansen, ledende overlæge, udpeget af Region Sjælland, Psykiatrien Roskilde
- Bodil Gramkow Andersen, overlæge, udpeget af Region Nordjylland, Ældrepsykiatrien
- Katrine Astrup Sørensen, fysioterapeut, udpeget af Dansk Selskab for Fysioterapi, Intensivt Afsnit, Aarhus Universitetshospital
- Birgitte Gram Blendstrup, specialkonsulent, Sundheds- og Ældreministeriet, Center for Psykiatri og Lægemiddelpolitik
- Mirjana Saabye, chefkonsulent, Ældre Sagen
- Dorthe Wiinholdt Christensen, videnskabelig medarbejder, Enhed for Sygepleje Forskning og Evidensbasering (ESFE), Bispebjerg og Frederiksberg Hospitaler
Sekretariat
Sekretariatet for begge grupper:
- Maria Herlev Ahrenfeldt, projektleder, specialkonsulent, Sundhedsstyrelsen
- Maria Bohr Dawids, fagkonsulent, læge, Sundhedsstyrelsen
- Britta Tendal, metodekonsulent, specialkonsulent, Sundhedsstyrelsen
- Tove Frandsen, søgekonsulent, Sundhedsstyrelsen
Peer review og offentlig høring
Den nationale kliniske retningslinje for forebyggelse og behandling af organisk delirium har forud for udgivelsen været i bred offentlig høring samt sendt i høring blandt følgende høringsparter:
- Dansk Sygepleje Selskab
- Dansk Psykiatrisk Selskab
- Ergoterapeutforeningen
- Dansk Selskab for Geriatri
- Dansk Selskab for Almen Medicin
- Dansk Selskab for Fysioterapi
- Dansk Ortopædisk Selskab
- Dansk Selskab for Anæstesiologi og Intensiv Medicin
- Dansk Endokrinologisk Selskab
- Dansk Selskab for Lungemedicin
- Dansk Neurologisk Selskab
- Dansk Selskab for Akutmedicin
- Dansk Selskab for Klinisk Farmakologi
- Dansk Apopleksi Selskab
- Ergoterapeutforeningen
- Danske Patienter
- Ældresagen
- Danske Regioner
- KL
- Socialstyrelsen
- Sundheds- og Ældreministeriet
Retningslinjen er desuden i samme periode peer reviewet af:
- Bjørn Erik Neerland, læge, lektor, Geriatrisk avdeling, Universitetet i Oslo
- Jens-Ulrik Rosholm, Overlæge, Geriatrisk afdeling G, OUH
Forkortelser og begreber
Referencer
1. Abizanda P., Leon M., Dominguez-Martin L., Lozano-Berrio V., Romero L., Luengo C., et al. : Effects of a short-term occupational therapy intervention in an acute geriatric unit. A randomized clinical trial. Maturitas 2011;69(3):273-278 Journal
2. Abraha I, Trotta F, Rimland JM, Cruz-Jentoft A, Lozano-Montoya I, Soiza RL, et al. : Efficacy of Non-Pharmacological Interventions to Prevent and Treat Delirium in Older Patients: A Systematic Overview. The SENATOR project ONTOP Series. PloS one 2015;10(6):e0123090
3. Agar MR, Lawlor PG, Quinn S, Draper B, Caplan GA, Rowett D, et al. : Efficacy of Oral Risperidone, Haloperidol, or Placebo for Symptoms of Delirium Among Patients in Palliative Care: A Randomized Clinical Trial. JAMA Internal Medicine 2017;177(1):34-42
4. Al-Aama T., Brymer C., Gutmanis I., Woolmore-Goodwin SM, Esbaugh J., Dasgupta M. : Melatonin decreases delirium in elderly patients: a randomized, placebo-controlled trial. International journal of geriatric psychiatry 2011;26(7):687-694 Journal
5. American Geriatrics Society Expert Panel on Postoperative Delirium IO : Postoperative delirium in older adults: best practice statement from the American Geriatrics Society. Journal of the American College of Surgeons 2015;220(2):136-48.e1 Journal
6. American Psychiatric Association : Diagnostic and statistical manual of mental disorders, DSM-IV-TM. 1994;4. ed. xxv, 886 s.
7. Avendano-Cespedes A, Garcia-Cantos N, Gonzalez-Teruel M, Martinez-Garcia M, Villarreal-Bocanegra E, Oliver-Carbonell J, et al. : Pilot study of a preventive multicomponent nurse intervention to reduce the incidence and severity of delirium in hospitalized older adults: MID-Nurse-P. Maturitas 2016;86 86-94
8. Balan S., Leibovitz A., Zila SO, Ruth M., Chana W., Yassica B., et al. : The relation between the clinical subtypes of delirium and the urinary level of 6-SMT. The Journal of neuropsychiatry and clinical neurosciences 2003;15(3):363-366 Journal
9. Barr J., Fraser GL, Puntillo K., Ely EW, Gelinas C., Dasta JF, et al. : Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical Care Medicine 2013;41(1):263-306 Journal
10. Boltz M, Resnick B, Chippendale T, Galvin J : Testing a family-centered intervention to promote functional and cognitive recovery in hospitalized older adults. Journal of the American Geriatrics Society 2014;62(12):2398-407
11. Bonaventura M., Zanotti R. : Effectiveness of IPD treatment for delirium prevention in hospitalized elderly. A controlled randomized clinical trial. Professioni infermieristiche 2007;60(4):230-236
12. Brajtman S., Wright D., Hogan DB, Allard P., Bruto V., Burne D., et al. : Developing guidelines on the assessment and treatment of delirium in older adults at the end of life. Canadian geriatrics journal 2011;14(2):40-50
13. Burry L., Hutton B., Williamson D.R., Mehta S., Adhikari N.K.J., Cheng W., et al. : Pharmacological interventions for the treatment of delirium in critically ill adults. Cochrane Database of Systematic Reviews 2019;2019(9):CD011749 Journal
14. Burry L., Mehta S., Perreault M.M., Luxenberg J.S., Siddiqi N., Hutton B., et al. : Antipsychotics for treatment of delirium in hospitalised non-ICU patients. Cochrane Database of Systematic Reviews 2018;2018(6):CD005594 Journal
15. Carbone MK, Gugliucci MR : Delirium and the Family Caregiver: The Need for Evidence-based Education Interventions. The Gerontologist 2015;55(3):345-52
16. Catic AG : Identification and management of in-hospital drug-induced delirium in older patients. Drugs & aging 2011;28(9):737-748 Journal
17. Chakraborti D., Tampi DJ, Tampi RR : Melatonin and melatonin agonist for delirium in the elderly patients. American Journal of Alzheimer’s Disease and Other Dementias 2015;30(2):119-129 Journal
18. Clegg A, Siddiqi N, Heaven A, Young J, Holt R : Interventions for preventing delirium in older people in institutional long-term care. The Cochrane database of systematic reviews 2014;1 CD009537
19. Cole MG, McCusker J., Bellavance F., Primeau FJ, Bailey RF, Bonnycastle MJ, et al. : Systematic detection and multidisciplinary care of delirium in older medical inpatients: a randomized trial. CMAJ : Canadian Medical Association journal = journal de l’Association medicale canadienne 2002;167(7):753-759
20. Cole MG, Primeau FJ, Bailey RF, Bonnycastle MJ, Masciarelli F., Engelsmann F., et al. : Systematic intervention for elderly inpatients with delirium: a randomized trial. CMAJ : Canadian Medical Association journal = journal de l’Association medicale canadienne 1994;151(7):965-970
21. Collinsworth AW, Priest EL, Campbell CR, Vasilevskis EE, Masica AL : A Review of Multifaceted Care Approaches for the Prevention and Mitigation of Delirium in Intensive Care Units. Journal of intensive care medicine 2016;31(2):127-41
22. Dansk Geriatrisk Selskab, O’Mahony D. : Screening of older persons’ prescriptions (STOPP) version 2 (Dansk oversættelse). Dansk Geriatrisk Selskab 2014;
23. Day J, Higgins I : Adult family member experiences during an older loved one’s delirium: a narrative literature review. Journal of Clinical Nursing 2015;24(11-12):1447-56
24. Devlin JW, Roberts RJ, Fong JJ, Skrobik Y., Riker RR, Hill NS, et al. : Efficacy and safety of quetiapine in critically ill patients with delirium: a prospective, multicenter, randomized, double-blind, placebo-controlled pilot study. Critical Care Medicine 2010;38(2):419-427 Journal
25. Fink M. : ECT in delirious states. Journal of electroconvulsive therapy 1999;15(3):175-177
26. Fink M. : The interaction of delirium and seizures. Seminars in clinical neuropsychiatry 2000;5(2):93-97
27. Friedman JI, Soleimani L, McGonigle DP, Egol C, Silverstein JH : Pharmacological treatments of non-substance-withdrawal delirium: a systematic review of prospective trials. The American Journal of Psychiatry 2014;171(2):151-9
28. Gage L, Hogan DB. 2014 CCSMH Guideline Update: The Assessment and Treatment of Delirium. Toronto: Canadian Coalition for Seniors’ Mental Health (CCSMH), 2014.
29. Garcia-Gollarte F, Baleriola-Julvez J, Ferrero-Lopez I, Cuenllas-Diaz A, Cruz-Jentoft A : An educational intervention on drug use in nursing homes improves health outcomes resource utilization and reduces inappropriate drug prescription. Journal of the American Medical Directors Association 2014;15(12):885-91
30. Girard TD, Exline MC, Carson SS, Hough CL, Rock P, Gong MN, et al. : Haloperidol and Ziprasidone for Treatment of Delirium in Critical Illness. New England Journal of Medicine 2018;379(26):2506-2516
31. Girard TD, Thompson JL, Pandharipande PP, Brummel NE, Jackson JC, Patel MB, et al. : Clinical phenotypes of delirium during critical illness and severity of subsequent long-term cognitive impairment: a prospective cohort study. The Lancet. Respiratory medicine 2018;6(3):213-222 Pubmed Journal
32. Guo Y, Sun L, Li LI, Jia P, Zhang J, Jiang H, et al. : Impact of multicomponent, nonpharmacologic interventions on perioperative cortisol and melatonin levels and postoperative delirium in elderly oral cancer patients. Archives of Gerontology and Geriatrics 2016;62 112-7
33. Hakim SM, Othman AI, Naoum DO : Early treatment with risperidone for subsyndromal delirium after on-pump cardiac surgery in the elderly: a randomized trial. Anesthesiology 2012;116(5):987-997 Journal
34. Halloway S : A family approach to delirium: a review of the literature. Aging & mental health 2014;18(2):129-39
35. Han JH, Wilson A, Vasilevskis EE, Shintani A, Schnelle JF, Dittus RS, et al. : Diagnosing delirium in older emergency department patients: validity and reliability of the delirium triage screen and the brief confusion assessment method. Annals of emergency medicine 2013;62(5):457-65 Pubmed Journal
36. Hempenius L., Slaets JP, van Asselt D., de Bock GH, Wiggers T., van Leeuwen BL : Outcomes of a Geriatric Liaison Intervention to Prevent the Development of Postoperative Delirium in Frail Elderly Cancer Patients: Report on a Multicentre, Randomized, Controlled Trial. PloS One 2013;8(6):e64834 Journal
37. Jeffs KJ, Berlowitz DJ, Grant S, Lawlor V, Graco M, de Morton N, et al. : An enhanced exercise and cognitive programme does not appear to reduce incident delirium in hospitalised patients: a randomised controlled trial. BMJ open 2013;3(6):
38. Kakuma R., du Fort GG, Arsenault L., Perrault A., Platt RW, Monette J., et al. : Delirium in older emergency department patients discharged home: effect on survival. Journal of the American Geriatrics Society 2003;51(4):443-450
39. Kerner N, Prudic J : Current electroconvulsive therapy practice and research in the geriatric population. Neuropsychiatry 2014;4(1):33-54 Pubmed
40. Kramp P., Bolwig TG : Electroconvulsive therapy in acute delirious states. Comprehensive psychiatry 1981;22(4):368-371
41. LaMantia MA, Messina FC, Hobgood CD, Miller DK : Screening for delirium in the emergency department: a systematic review. Annals of Emergency Medicine 2014;63(5):551-560.e2 Journal
42. Lapane KL, Hughes CM, Daiello LA, Cameron KA, Feinberg J : Effect of a pharmacist-led multicomponent intervention focusing on the medication monitoring phase to prevent potential adverse drug events in nursing homes. Journal of the American Geriatrics Society 2011;59(7):1238-45
43. Leslie DL, Inouye SK : The importance of delirium: economic and societal costs. Journal of the American Geriatrics Society 2011;59(Suppl 2):S241-3
44. Leslie DL, Marcantonio ER, Zhang Y., Leo-Summers L., Inouye SK : One-year health care costs associated with delirium in the elderly population. Archives of Internal Medicine 2008;168(1):27-32 Journal
45. Litton E., Carnegie V., Elliott R., Webb SA : The Efficacy of Earplugs as a Sleep Hygiene Strategy for Reducing Delirium in the ICU: A Systematic Review and Meta-Analysis. Critical Care Medicine 2016;44(5):992-999 Journal
46. Lonergan E, Luxenberg J, Areosa Sastre A : Benzodiazepines for delirium. The Cochrane database of systematic reviews 2009;(4):CD006379
47. Lundstrom M., Olofsson B., Stenvall M., Karlsson S., Nyberg L., Englund U., et al. : Postoperative delirium in old patients with femoral neck fracture: a randomized intervention study. Aging clinical and experimental research 2007;19(3):178-186
48. Martinez FT, Tobar C., Beddings CI, Vallejo G., Fuentes P. : Preventing delirium in an acute hospital using a non-pharmacological intervention. Age and Ageing 2012;41(5):629-634 Journal
49. Martinez F, Tobar C, Hill N : Preventing delirium: should non-pharmacological, multicomponent interventions be used? A systematic review and meta-analysis of the literature. Age and Ageing 2015;44(2):196-204
50. Meagher DJ, McLoughlin L, Leonard M, Hannon N, Dunne C, O’Regan N : What do we really know about the treatment of delirium with antipsychotics? Ten key issues for delirium pharmacotherapy. The American Journal of Geriatric Psychiatry : Official Journal of the American Association for Geriatric Psychiatry 2013;21(12):1223-38
51. Menza MA, Murray GB, Holmes VF, Rafuls WA : Controlled study of extrapyramidal reactions in the management of delirious, medically ill patients: intravenous haloperidol versus intravenous haloperidol plus benzodiazepines. Heart & lung : the journal of critical care 1988;17(3):238-241
52. Moon K-J, Lee S-M : The effects of a tailored intensive care unit delirium prevention protocol: A randomized controlled trial. International journal of nursing studies 2015;52(9):1423-32
53. Nandi S., Harvey WF, Saillant J., Kazakin A., Talmo C., Bono J. : Pharmacologic risk factors for post-operative delirium in total joint arthroplasty patients: a case-control study. The Journal of arthroplasty 2014;29(2):268-271 Journal
54. National Institute for Health and Care Excellence (NICE) : Delirium: prevention, diagnosis and management (CG 103). NICE, 2010;Clinical Guideline 103 Link
55. Neufeld KJ, Yue J., Robinson TN, Inouye SK, Needham DM : Antipsychotic Medication for Prevention and Treatment of Delirium in Hospitalized Adults: A Systematic Review and Meta-Analysis. Journal of the American Geriatrics Society 2016;64(4):705-714 Journal
56. Nielsen RM, Olsen KS, Lauritsen AO, Boesen HC : Electroconvulsive therapy as a treatment for protracted refractory delirium in the intensive care unit–five cases and a review. Journal of critical care 2014;29(5):881.e1-6 Pubmed Journal
57. Page VJ, Ely EW, Gates S, Zhao XB, Alce T, Shintani A, et al. : Effect of intravenous haloperidol on the duration of delirium and coma in critically ill patients (Hope-ICU): a randomised, double-blind, placebo-controlled trial. The Lancet. Respiratory medicine 2013;1(7):515-23 Pubmed Journal
58. Pandharipande P., Shintani A., Peterson J., Pun BT, Wilkinson GR, Dittus RS, et al. : Lorazepam is an independent risk factor for transitioning to delirium in intensive care unit patients. Anesthesiology 2006;104(1):21-26
59. Pitkala KH, Laurila JV, Strandberg TE, Tilvis RS : Multicomponent geriatric intervention for elderly inpatients with delirium: a randomized, controlled trial. The journals of gerontology. Series A, Biological sciences and medical sciences. 2006;61(2):176-181
60. Rosenzweig AB, Sittambalam CD : A new approach to the prevention and treatment of delirium in elderly patients in the intensive care unit. Journal of community hospital internal medicine perspectives 2015;5(4):27950
61. Schrijver EJM, de Graaf K., de Vries OJ, Maier AB, Nanayakkara PWB : Efficacy and safety of haloperidol for in-hospital delirium prevention and treatment: A systematic review of current evidence. European journal of internal medicine 2016;27 14-23
62. Siddiqi N, Harrison JK, Clegg A, Teale EA, Young J, Taylor J, et al. : Interventions for preventing delirium in hospitalised non-ICU patients. The Cochrane database of systematic reviews 2016;3 CD005563
63. Stenvall M, Berggren M, Lundstrom M, Gustafson Y, Olofsson B : A multidisciplinary intervention program improved the outcome after hip fracture for people with dementia–subgroup analyses of a randomized controlled trial. Archives of Gerontology and Geriatrics 2012;54(3):e284-9
64. Stromgren LS : ECT in acute delirium and related clinical states. Convulsive therapy 1997;13(1):10-17
65. Sundhedsloven : Lovbekendtgørelse LBK nr 903 af 26/08/2019. Sundheds- og Ældreministeriet, 2019. Link
66. Sundhedsstyrelsen. Seponeringslisten 2021 – forslag til seponering af hyppigt anvendte lægemidler hos voksne. Sundhedsstyrelsen, 2020. Opdateret: 20.11.2020. Senest hentet: 19.02.2021. Link
67. Tahir TA, Eeles E., Karapareddy V., Muthuvelu P., Chapple S., Phillips B., et al. : A randomized controlled trial of quetiapine versus placebo in the treatment of delirium. Journal of psychosomatic research 2010;69(5):485-490 Journal
68. Tsuda A., Nishimura K., Naganawa E., Otsubo T., Ishigooka J. : Ramelteon for the treatment of delirium in elderly patients: a consecutive case series study. International journal of psychiatry in medicine 2014;47(2):97-104 Journal
69. van der Cammen TJ, Rajkumar C, Onder G, Sterke CS, Petrovic M : Drug cessation in complex older adults: time for action. Age and Ageing 2014;43(1):20-5
70. Vejledning om behandling med antipsykotiske lægemidler til personer over 18 år med psykotiske lidelser : VEJ nr 9276 af 06/05/2014. Sundheds- og Ældreministeriet, 2014. Link
71. Vejledning om ordination af afhængighedsskabende lægemidler : VEJ nr 9523 af 19/06/2019. Sundheds- og Ældreministeriet, 2019. Link
72. Walker CK, Gales MA : Melatonin Receptor Agonists for Delirium Prevention. The Annals of Pharmacotherapy 2016;
73. Wong CL, Holroyd-Leduc J., Simel DL, Straus SE : Does this patient have delirium?: value of bedside instruments. Jama 2010;304(7):779-786 Journal
74. World Health Organization : ICD-10 version 2010 : international statistical classification of diseases and related health problems 10th revision. Link
75. Søgeprotokol for opdatering af NKR Delirium: Guidelines – søgeperiode 2015-20. Sundhedsstyrelsen, 2020. Link
76. Søgeprotokol for opdatering af NKR Delirium: Sekundær- og primærlitteratur for PICO 7. Sundhedsstyrelsen, 2020.
77. NKR delir PICO 2 Multikomponent hos patienter med risiko for delir.
78. NKR delir PICO 3 Multikomponent behandling.
79. NKR delir PICO 5 Familie.
80. NKR 42 Delir PICO 6 Gennemgang af medicin.
81. NKR delir PICO 7 Behandling af delir med antiopsykotika.
82. NKR delir PICO 7 Behandling af delir med antiopsykotika.
83. NKR delir PICO 7 Behandling af delir med antiopsykotika.
84. NKR delir PICO 7 Behandling af delir med antiopsykotika.
85. NKR opdt. delir PICO 7 Behandling af delir med antiopsykotika.
86. NKR opdt. delir PICO 7 Behandling af delir med antiopsykotika.
87. NKR opdt. delir PICO 7 Behandling af delir med antiopsykotika.
